
- •Образования «национально-исследовательский томский политехнический университет»
- •Глава 1. Основы микробиологии
- •1.1. Морфология микроорганизмов .1.1. Систематика и номенклатура микроорганизмов
- •1.1.2. Формы бактерий
- •1.1.3. Структура бактериальной клетки и методы ее исследования
- •Включения Нефотоситезирцющие Основные
- •1.1.4. Морфология микробов-эукариотов: дрожжевых и плесневых грибов
- •Зкзоспоры
- •1.1.5. Методы микроскопического исследования микроорганизмов
- •Электронная микроскопия
- •1.2. Физиология микроорганизмов 1.2.1. Питание бактерий
- •1.2.2. Питательные среды
- •1.2.3. Условия культивирования бактерий
- •1.2.4. Дыхание бактерий
- •1.2.5.Ферменты бактерий
- •1.2.6. Культуральные свойства бактерий
- •1.2.6. Выделение чистых культур микроорганизмов
- •Глава 2. Химические основы жизни
- •2.1. Липиды
- •2.1.1. Жирные кислоты и родственные липиды
- •Глава 7. Сельскохозяйственная биотехнология 360
- •Глава 8. Экологическая биотехнология 368
- •2.1.2. Жирорастворимые витамины, стероиды и другие липиды
- •2.2. Сахара и полисахариды
- •2.2.2. Дисахариды и полисахариды
- •2.3. Белки
- •2.3.1. Биологические функции белков
- •2.3.2. Белковые аминокислоты и полипептиды
- •2.3.3. Структура белков
- •Первичная структура белков
- •Глава 7. Сельскохозяйственная биотехнология 360
- •Глава 8. Экологическая биотехнология 368
- •Глава 7. Сельскохозяйственная биотехнология 360
- •Глава 8. Экологическая биотехнология 368
- •2.4.5. Биосинтез нуклеиновых кислот и белков (матричные биосинтезы)
- •I I аденин
- •Глава 3. Технологические основы биотехнологических производств
- •3.1. Процессы в биотехнологии
- •3.4. Контроль и управление биотехнологическими процессами; моделирование и оптимизация
- •Глава 4. Генная инженерия
- •4.3. Получение фармакологических препаратов с помощью методов генной инженерии
- •4.3.1. Биосинтез инсулина человека в клетках кишечной палочки
- •4.3.2. Биосинтез соматотропина и других гормонов человека
- •4.3.3. Получение интерферонов
- •4.3.4. Получение иммуногенных препаратов и вакцин
- •4.3.5. Другие области применения генной инженерии
- •1. Новые методы диагностики и исследований
- •2. Генная инженерия и белковая инженерия ферментов
- •3. Получение бактерий для деградации токсикантов и ксенобиотиков
- •5. Биоматериалы
- •4.5. Преимущества и опасность генной инженерии
- •4.5. Меры безопасности
- •Глава 5. Промышленная микробиология
- •5.1. Производство первичных метаболитов
- •5.1.1. Производство аминокислот
- •5.1.2. Производство органических кислот
- •5.1.3. Получение витаминов
- •5.2. Производство вторичных метаболитов
- •5.3. Производство белков одноклеточных и многоклеточных
- •5.3.1. Производство белка одноклеточных организмов
- •5.3.2. Производство грибного белка (микопротеина)
- •5.3.3. Производство цианобактерий
- •Глава 6. Инженерная энзимология
- •6.1. Методы получения иммобилизованных ферментов
- •6.1.1. Физические методы иммобилизации
- •6.1.2. Химические методы иммобилизации ферментов
- •Носитель Вставка Фермент Иммобилизованный фермент
- •6.2. Применение иммобилизованных ферментов
- •6.3. Промышленные процессы с использованием иммобилизованных ферментов
- •6.3.1. Разделение рацемических смесей аминокислот
- •6.3.2. Производство кукурузного сиропа с высоким содержанием
- •Глава 7. Сельскохозяйственная биотехнология
- •7.1. Биопестициды
- •7.1.1. Технология получения бактериальных энтомопатогенных
- •7.1.2. Технология получения грибных энтомопатогенных
- •7.1.3. Технология получения вирусных энтомопатогенных препаратов
- •7.2. Биологические удобрения
- •7.2.1. Технология получения сухого нитрагина
- •7.2.2. Технология получения сухого азотобактерина
- •7.2.3. Технология получения фосфоробактерина
- •Глава 8. Экологическая биотехнология
- •8.1. Аэробная биологическая очистка сточных вод
- •8.1.1. Основные характеристики сточных вод
- •8.1.2. Процессы с участием активного ила
- •8.1.3. Аэробная обработка ила
- •8.1.4. Вторичная очистка сточных вод с помощью капельных биологических фильтров
- •8.2. Анаэробная переработка отходов
- •1Связь, a-мальтоза
2.3.2. Белковые аминокислоты и полипептиды
Мономерными звеньями полипептидов являются a-аминокислоты общей формулы
a O H2N-CHC-OH
^ I
R
Аминокислоты отличаются только природой группы R, связанной с a-углеродным атомом.
Все аминокислоты, кроме глицина, имеют хиральный атом Са и могут существовать в виде оптических изомеров (энантиомеров): L- изомер и D-изомер:
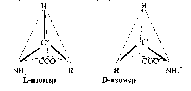
В состав всех изученных в настоящее время белков входят аминокислоты L-ряда, у которых, если рассматривать хиральный атом со стороны атома Н, группы NH3+, COO- и радикал R расположены по часовой стрелке. Необходимость при построении биологически значимой полимерной молекулы строить ее из строго определенного энантиомера оче- видн: из рацемической смеси двух энантиомеров получилась бы невообразимо сложная смесь диастереомеров. Вопрос, почему жизнь на Земле основана на белках, построенных именно из L-, а не D-a- аминокислот, до сих пор остается интригующей загадкой. Следует отметить, что D-аминокислоты достаточно широко распространены в живой природе и, более того, входят в состав биологически значимых оли- гопептидов.
Все белки построены из 20-ти аминокислот, 10 из которых являются незаменимыми.
Таблица
2.2
o
h2n-chc-oh
2
1 ch3
o
h2n-chc-oh
2
1 ch2
1
2 ch2 1
2 ch2 1
2 nh
C=nh
Nh2
o
h2n-chc-oh
2
1
ch2
1
2 c=o
Nh2
o
h2n-chc-oh
2
1
ch2
1
2 c=o
oh
o
h2n-chc-oh
2
1 ch2
1
sh
Аланин
Ala
Аргинин
Arg
Аспарагин
Asn
Аспарагиновая
кислота Asp
Цистеин
Cys
o
h2n-chC-oh
2
1
ch2
1
2 ch2 1
2 c=o
oh
o
h2n-chc-oh
2
1
ch2
1
2 ch2 1
2 c=o
Nh2
nh2
1
2
h-ch
1
c=o
oh
o
h2n-chc-oh
2
1
ch2
Mh
o
h2n-chc-o
лцлин
cnch^
1
3
ch2
1
ch3
Глутаминовая
кислота Glu
Глутамин
Gln
Глицин
Gly
Гистидин
His
Изолейцин
Ile
o
h2n-chc-oh
1
ch2
1
2
chch3
1
3 ch3
o
h2n-chc-oh
2
1 ch2
1
2 ch2 1
2 ch2 1
2 ch2 1
2 nh2
o
h2n-chc-oh
2
1
ch2
1
2
ch2
1
2
s
ch3
o
h2n-chC-oh
1
ch2
6
o
11
c-oh
HNb
Лейцин
Leu
Лизин
Lys
Метионин
Met
Фенилаланин
Phe
Пролин
Pro
o
h2n-chc-oh
1
ch2
1
2 oh
o
h2n-chc-oh
2
1
choh
ch3
o
h2n-chc-oh
2
1
ch2
Лтл
HN—\l
o
h2n-chc-oh
2
1
ch2
Ф
oh
o
h2n-chc-oh
2
1
choh3
1
3 ch3
Серин
Ser
Треонин
Thr
Триптофан
Try
Тирозин
Tyr
Валин
Val
*
- незаменимые аминокислоты подчеркнуты.
Аминокислоты,
встречающиеся в живых системах*
