
- •Часть I
- •Содержание
- •Аминокислоты
- •Ионные формы аминокислот
- •Химические свойства аминокислот
- •Реакции аминокислот, обусловленные одновременным присутствием карбоксильных и аминогрупп:
- •Реакции аминокислот, обусловленные присутствием карбоксильных групп:
- •Реакции аминокислот, связанные с присутствием аминогрупп:
- •Методы разделения и идентификации аминокислот
- •Пептиды
- •Тема I.
- •Химические свойства аминокислот.
- •Разделение смеси аминокислот методом хроматографии на бумаге.
- •Тема II.
- •Качественные реакции на аминокислоты.
- •Реакция с формальдегидом
- •Реакция Адамкевича
- •Реакция Гопкинса-Коле
- •Качественные реакции на пептиды и белки.
- •Физико-химические свойства белков
- •Определение изоэлектрической точки белков
- •Реакции осаждения белков
- •Фракционное осаждение белков методом высаливания
- •Сложные белки
- •Гемопротеиды
- •Гемоглобин
- •Выделение гемоглобина
- •Качественная реакция на гемовую группу. Бензидиновая проба
- •Фосфопротеиды
- •Выделение казеина
- •Определение фосфорной кислоты в казеине
- •Методы количественного определения белка
- •Абсорбционная спектроскопия
- •Тема I. Методы выделения белков в гомогенном состоянии
- •Тема II. Методы количественного определения белка
- •Построение калибровочных графиков Биуретовый метод Таблица 1
- •Метод Лоури Таблица 2
- •Метод Брэдфорд Таблица 3
- •Приложение Строение и номенклатура аминокислот
- •Протеиногенные аминокислоты
- •Практикум по общей и экологической биохимии
- •Часть I
- •220009 Минск
Реакции аминокислот, обусловленные присутствием карбоксильных групп:
образование солей;
2. образование ангидридов;
3. образование галогенангидридов;
4. образование амидов;
5. образование сложных эфиров;
6. реакции декарбоксилирования.
Реакции аминокислот, связанные с присутствием аминогрупп:
замещение в аминогруппе атома водорода на ацил (образование пептидов);
взаимодействие с азотистой кислотой;
замещение в аминогруппе атома водорода на остаток угольной кислоты;
взаимодействие с формальдегидом;
реакции окислительного, восстановительного и внутримолекуляр-ного дезаминирования.
Образование пептидных связей
Наиболее важной реакцией, в которой участвуют аминокислоты, является образование пептидных связей. При этом высвобождается одна молекула воды.
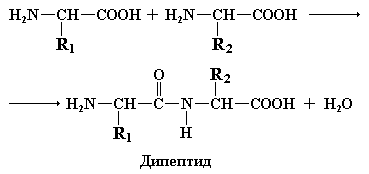
Равновесие реакции образования пептидной связи в обычных условиях сильно сдвинуто в сторону ее гидролиза. Поэтому для образования пептидных связей между аминокислотами их карбоксильные группы должны быть предварительно активированы. Химический синтез пептидов основан на предварительном получении хлорангидридов аминокислот. Биологическая активация аминокислот включает их взаимодействие с АТР.
Качественные реакции на аминокислоты
Структура радикалов аминокислот исключительно разнообразна. Это обстоятельство позволяет использовать многочисленные цветные реакции для обнаружения большинства аминокислот. Многие из них настолько чувствительны и высокоспецифичны, что позволяют обнаруживать ничтожные количества индивидуальных аминокислот в составе сложных смесей, биологических жидкостях, гидролизатах белков и т.п. Поэтому некоторые цветные реакции используются для количественного определения аминокислот.
Одной из наиболее чувствительных реакций на -аминогруппы аминокислот является их взаимодействие с нингидрином. Белки, полипептиды и аминокислоты при нагревании образуют с нингидрином соединения синего или сине-фиолетового цвета, исключение составляет пролин – продукты его реакции с нингидрином имеют ярко-желтую окраску. Суть реакции заключается в том, что -аминокислоты, реагируя с нингидрином, подвергаются окислительному дезаминированию и декарбоксилированию, одновременно.
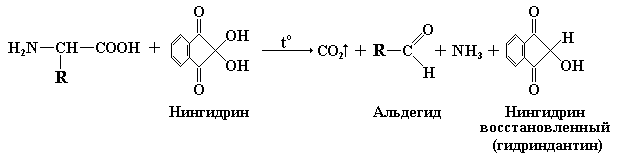
Один из продуктов реакции – гидриндантин взаимодействует с аммиаком и молекулой нингидрина с образованием окрашенного соединения – дикетогидриндилиден-дикетогидриндамина (ДИДА).
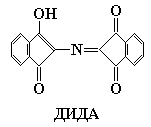
Нингидрин способен реагировать не только с -аминокислотами, но и с другими аминами – при этом развивается такая же окраска, но без выделения СО2. Следовательно, выделение СО2 является индикатором участия в нингидртновой реакции именно -аминокислот. Пептиды и NH3 также вступают в реакцию с нингидрином, но менее активно, чем -аминокислоты.
Ксантопреновая реакция специфична на радикалы ароматических аминокислот. Суть ее состоит в том, что при нагревании ароматических аминокислот или содержащих их белков и полипептидов с концентрированной азотной кислотой образуются нитросоединения желтого цвета. Реакция протекает в две стадии. На первой стадии бензольное кольцо аминокислоты подвергается нитрованию.
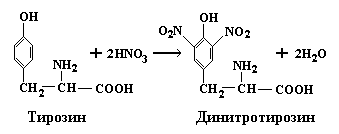
На второй стадии продукты нитрования реагируют с гидроксидом натрия или аммония с образованием натриевой или аммониевой соли, имеющей желто-оранжевое окрашивание.
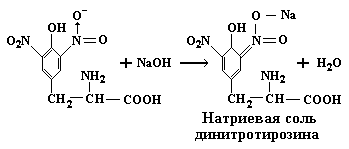
При проведении ксантопреновой реакции в качестве контроля используют желатин, который не содержит ароматических аминокислот.
Реакция Фоля специфична для серусодержащих аминокислот – цистеина, цистина, метионина или для белков, содержащих эти аминокислоты. Реакция протекает в два этапа. Сначала под действием гидроксида натрия при нагревании происходит отщепление SH-групп аминокислот и переход серы из органического соединения в неорганическое:
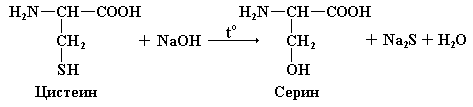
Затем сульфид натрия взаимодействует с уксуснокислым свинцом, в результате чего происходит образование сульфида свинца, который выпадает в виде осадка черного цвета:
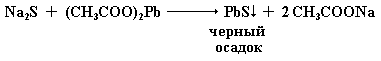
Качественные реакции на индивидуальные аминокислоты
Качественные реакции на триптофан
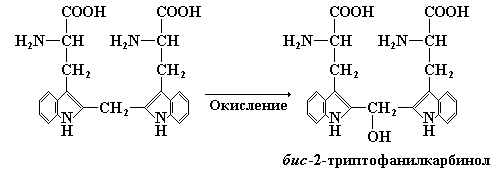
Реакция Адамкевича, реакция Гопкинса-Коле и реакция с формальдегидом основаны на способности триптофана взаимодействовать с альдегидами, в частности с формальдегидом. Эта аминокислота, конденсируясь с формальдегидом, дает соединение бис-2-триптофанилметан:
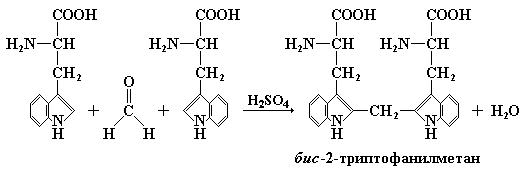
Продукт конденсации окисляется до бис-2-триптофанилкарбинола, имеющего красно-фиолетовую окраску:
В реакциях Адамкевича и Гопкинса-Коле исходным реагентом является глиоксиловая кислота (в реакции Адамкевича используют концентрированную уксусную кислоту, содержащую глиоксиловую кислоту в виде примеси). Под действием концентрированной серной кислоты глиоксиловая кислота декарбоксилируется с образованием формальдегида, вступающего в реакцию с триптофаном:
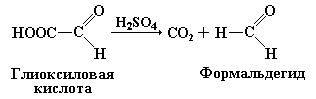
Следует указать, что в реакции Гопкинса-Коле конечным цветным продуктом являются медные соли бис-2-триптофанилкарбинола, придающие раствору сине-фиолетовую окраску. Эти соли образуются в присутствии ми-неральных кислот при добавлении в реакционную смесь сульфата меди (II).
Реакция Шульце-Распайля с 5-(оксиметил)фурфуролом основана на способности 5-(оксиметил)фурфурола, образующегося при дегидратации фруктозы (или других кетогексоз) под действием концентрированных неорганических кислот (H2SO4, HCl), формировать с триптофаном окрашенные продукты конденсации темно-красного цвета. Реакцию можно проводить как с фруктозой, так и с сахарозой, при гидролитическом расщеплении которой освобождаются равные количества глюкозы и фруктозы.
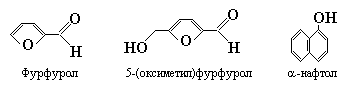
Качественная реакция на пролин
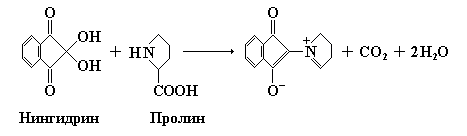
Выше указывалось, что нингидрин взаимодействует с пролином необычным для других аминокислот способом. В результате конденсации пролина с нингидрином происходит образование продукта, имеющего ярко-желтую окраску:
Качественная реакция на тирозин
Реакция Миллона. Реактив Миллона представляет собой смесь нитратов и нитритов оксида ртути (I) и (II) растворенных в концентрированной азотной кислоте. При их взаимодействии с фенильной группой тирозина образуется нитрозотирозин, ртутное соединение которого окрашено в красный цвет:

Качественная реакция на аргинин
Реакция Сакагучи основана на способности аргинина взаимодействовать с -нафтолом в присутствии окислителя – гипобромита натрия (NaBrO). Несмотря на то, что механизм реакции еще не до конца выяснен, ряд наблюдений свидетельствует в пользу следующей схемы. Сначала -нафтол в присутствии окислителя соединяется с гуанидиновой группировкой аргинина:
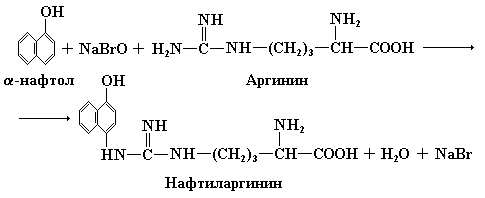
Затем, при дальнейшем окислении нафтиларгинина образуется соединение типа хинонимина:

Поскольку производные хинониминов (в данном случае нафтохинонимина), у которых водород иминогруппы замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина.
Качественная реакция на гистидин
Реакция Паули основана на способности гистидина реагировать с диазареактивом, основу которого составляет диазабензолсульфоновая кислота, образующаяся в реакции диазатирования при взаимодействии кислого раствора сульфаниловой кислоты с нитритом калия:
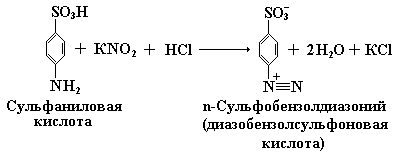
При реакции диазабензолсульфоновой кислоты с гистидином образуется соединение вишнево-красного цвета – 2,5-бис-n-сульфобензолазагистидин:
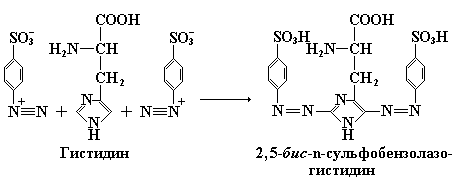
Качественная реакция на метионин
Реакция Мак-Карти и Салливана основана на взаимодействии производных метионина с комплексным соединением железа – нитропруссидом натрия (Na2[Fe(CN)5NO]) в присутствии концентрированных неорганических кислот, что сопровождается образованием продуктов, имеющих яркую красно-фиолетовую окраску.
Качественная реакция на глицин
Р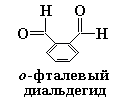 еакция
Циммермана основана на взаимодействии
глицина с о-фталевым диальдегидом
с образованием ярко-зеленных продуктов,
выпадающих в виде осадка.
еакция
Циммермана основана на взаимодействии
глицина с о-фталевым диальдегидом
с образованием ярко-зеленных продуктов,
выпадающих в виде осадка.
