
- •Содержание
- •Введение
- •Объекты анализа материалов микроэлектроники
- •1. Основы качественного анализа
- •Классификация анионов
- •2. Аналитические реакции катионов
- •Лабораторная работа № 1 Частные реакции катионов I - II групп Опыт 1. Обнаружение катиона калия
- •Опыт 2. Обнаружение катиона натрия
- •Опыт 3. Обнаружение магния в растворе
- •Опыт 4. Определение иона аммония
- •Реакции катионов I группы
- •Опыт 5. Обнаружение катиона бария
- •Опыт 6. Обнаружение катиона стронция
- •Опыт 6. Обнаружение катиона стронция
- •Опыт 7. Обнаружение катиона кальция
- •Лабораторная работа № 2 Анализ смеси катионов I и II групп
- •3. Аналитические реакции катионов III группы
- •Лабораторная работа № 3 Частные реакции катионов III группы Опыт 1. Обнаружение катиона алюминия
- •Опыт 2. Обнаружение хрома
- •Реакции хромат- и бихромат-ионов
- •Опыт 3. Обнаружение железа
- •Опыт 5. Обнаружение цинка в растворе
- •Опыт 6. Обнаружение кобальта
- •Опыт 7. Обнаружение никеля
- •Лабораторная работа № 4 Анализ смеси катионов III, II и I групп
- •4. Аналитические реакции катионов IV и V групп
- •Опыт 2. Обнаружение катионов кадмия
- •Опыт 3. Обнаружение катионов висмута
- •Подгруппа мышьяка Опыт 5. Обнаружение ионов мышьяка
- •Реакции катионов подгруппы меди
- •Обнаружение арсенит-ионов
- •Обнаружение арсенат-ионов
- •Опыт 6. Обнаружение ионов сурьмы
- •Обнаружение ионов сурьмы (III)
- •Обнаружение ионов сурьмы (V)
- •Опыт 7. Обнаружение ионов олова
- •Обнаружение ионов олова (II)
- •Обнаружение ионов олова (IV)
- •Лабораторная работа № 6 Анализ смеси катионов IV группы
- •Лабораторная работа № 7 Частные реакции катионов V группы Опыт I. Определение катионов серебра
- •Опыт 2. Обнаружение катионов свинца
- •Лабораторная работа № 8 Анализ смеси катионов V - I групп
- •Реакции катионов V группы
- •5. Аналитические реакции анионов
- •Опыт 2. Определение аниона со32–
- •Опыт 3. Определение аниона ро4–
- •Опыт 4. Определение аниона SiO32–
- •Опыт 5. Определение аниона f –
- •Вторая аналитическая группа анионов Опыт 6. Определение аниона с1–
- •Опыт 7. Определение аниона Вr –
- •Опыт 8. Определение аниона I –
- •Опыт 9. Определение аниона s2–
- •Третья аналитическая группа анионов Опыт 10. Определение аниона no3–
- •Опыт п. Определение анионов no2–
- •6. Количественный анализ
- •7. Гравиметрия
- •Весовые методы определения некоторых элементов
- •Лабораторная работа № 10 Весовое определение серы в сульфиде кадмия
- •Оборудование и реактивы
- •Описание определения
- •Определение серы
- •Лабораторная работа №11 Весовое определение никеля и железа в резистивных сплавах Определение никеля
- •Оборудование и реактивы
- •Описание определения
- •Определение железа
- •Оборудование и реактивы
- •Описание определения
- •8. Титриметрия
- •Растворение образца.
- •Описание определения
- •Лабораторная работа № 16 Определение стехиометрического состава сверх проводящей керамики ( система y-Ba-Cu )
- •Определение бария
- •Реактивы
- •Описание определения
- •Иодометрическое титрование
- •Стандартизация раствора тиосульфата натрия по бихромату калия
- •Реактивы
- •Описание определения
- •Определение меди
- •Реактивы
- •Описание определения
- •Определение иттрия комплексонометрическим титрованием
- •Реактивы
- •Описание определения
- •Расчет стехиометрии y1 Ва2 Cu3o7
- •9.Физико-химические методы анализа
- •А. Определение фосфора по желтой форме
- •Оборудование и реактивы
- •Описание определения
- •Б. Определение фосфора в виде фосфорномолибденовой сини
- •Оборудование и реактивы
- •Описание определения
- •В. Определение кремния
- •Оборудование и реактивы
- •Описание определения
- •Оборудование и реактивы
- •Описание определения
- •Б. Фотометрическое определение железа в виде роданидного комплекса
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 19 Экстракционно – фотометрическое определение германия в полупроводниковых халькогенидных стеклах системы Te–As-Si-Ge
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 20 Спектрофотометрическое определение хрома и марганца при совместном присутствии в контактных проводниковых сплавах
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 21 Спектрофотометрическое определение висмута в присутствии свинца
- •Оборудование и реактивы
- •Описание определения
- •11. Люминесцентный анализ
- •Оборудование и реактивы
- •Описание определения
- •12. Инфракрасная спектроскопия
- •Лабораторная работа № 23 Измерение толщины пленок диоксида и нитрида кремния методом икс
- •Применение икс для исследования материалов микроэлектроники
- •Оборудование и реактивы
- •Описание определения
- •В отчете долж ны быть представлены:
- •Пример расчета:
- •13.Эмиссионный спектральный анализ
- •Лабораторная работа № 24 Определение примесей металлов методом трех эталонов
- •А. Фотографирование спектров трех эталонов и образцов Оборудование и реактивы
- •Описание определения
- •Характерные группы линий железа на планшетах атласа
- •В. Измерение почернений линий примесей на микрофотометре и построение калибровочных графиков
- •Оборудование и реактивы
- •Описание определения
- •Форма записи результатов наблюдений
- •Последовательность фотографирования образцов
- •Форма записи результатов наблюдений
- •Длины волн определяемых примесей
- •14. Электрохимические методы анализа
- •15.Потенциометрия
- •Прямая потенциометрия (ионометрия)
- •Оборудование и реактивы
- •Описание определения
- •Результаты ионометрического определения ионов в воде
- •Б. Определение фторид-ионов
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 27 Определение рН в водных растворах
- •Оборудование и реактивы
- •Описание определения
- •Потенциометрическое титрование (пт)
- •Результаты титрования
- •Лабораторная работа № 28 Определение соляной кислоты в травильной ванне
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 29 Определение соляной и уксусной кислот в растворе при совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 30 Определение соляной и борной кислот в растворе при совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 31 Определение содержания кобальта (II) в растворе
- •Оборудование и реактивы
- •Описание определения
- •Лабораторная работа № 32 Определение концентрации хлорида железа (III)
- •Оборудование и реактивы
- •Описание определения
- •16. Кондуктометрическое титрование
- •Лабораторная работа № 33 Дифференцированное определение солей железа (п) и(ш) в травильных растворах
- •Оборудование и реактивы
- •Описание определения
- •17. Вольтамперометрия
- •Лабораторная работа № 34 Определение примеси цинка в фосфоре
- •18. Инверсионная вольтамперометрия
- •Лабораторная работа № 36 Определение примесей цинка, кадмия, свинца и меди методом инверсионной вольтамперометрии
- •Оборудование и реактивы
- •Описание определения
- •19. Хроматография
- •Раздельное вымывание примесей с катионита ку-2
- •Лабораторная работа № 37 Определение меди и цинка при их совместном присутствии на катионите ку-2
- •Оборудование и реактивы
- •Описание определения
- •Описание определения
- •Определение кадмия
- •Результаты хроматографического определения ионов кадмия
- •Определение теллура
- •20. Рекомендуемая литература
- •Реакции катионов III группы
- •Реакции ионов подгруппы мышьяка
Оборудование и реактивы
Спектрофотометр.
Кюветы 1 см, 3-4 шт.
Колбы мерные емкостью 100 мл, 12 шт.
Стандартный раствор перманганата калия, 0,1 н. раствор. Перед применением 9,1 мл раствора разбавляют водой до 100 мл. Этот раствор содержит 0,1 мг марганца в 1 мл.
Стандартный раствор бихромата калия. Навеску 0,2818 г K2Cr2O7 растворяют в мерной колбе емкостью 1 л. Этот раствор содержит 0,1 мг хрома в
1 мл.
Персульфат аммония.
Фосфорная кислота, d = 1,7.
Азотная кислота, d = 1,40.
Вода дистиллированная.
Смесь кислот готовят следующим образом: к 76 мл воды приливают тонкой струей при перемешивании 16 мл H2SO4( d = 1,84), после охлаждения приливают 8 мл H3PO4 (d = 1,7) и 55 мл HNO3 (d = 1.40).
Описание определения
Навеску сплава 0,1-0,2 г растворяют при нагревании в 3-5 мл азотной кислоты (1:1) и 2-3 мл серной кислоты (1:1), кипятят раствор до удаления окислов азота. Полученный раствор охлаждают, прибавляют 30 мл воды, нагревают до кипения и осаждают серебро горячей соляной кислотой плотностью 1,19. После непродолжительного кипячения раствор охлаждают, переносят в мерную колбу на 100 мл и доливают до метки 0,2 н. соляной кислотой.
Для анализа берут аликвотную часть 10,00 мл анализируемого раствора, содержащего перманганат- и дихромат-ионы в мерную колбу емкостью
100 мл, разбавляют водой до метки и тщательно перемешивают. Затем измеряют оптическую плотность раствора при 430 нм и 550 нм.
Построение калибровочного графика. В мерные колбы емкостью
100 мл помещают 1,0; 1,2; 1,4; 1,8; 2,0 мл стандартного раствора перманганата калия, а в ряд других мерных колб емкостью 100 мл –2,0; 1,5;2,8; 3,2; 3,5 мл стандартного раствора бихромата калия. Добавляют воды до метки и измеряют оптическую плотность перманганата калия при =430 нм и 550 нм и бихромата калия при =430 нм в кюветах толщиной слоя 1 см. по полученным данным строят калибровочные графики: для KMnO4 при 550 и 430 нм и для K2Cr2O7 при 430 нм (рис. 2).
Лабораторная работа № 21 Спектрофотометрическое определение висмута в присутствии свинца
Определение висмута в присутствии свинца при помощи ЭТДА, (трилона Б)) основано на использовании области спектра, в которой не наблюдается светопоглощения комплексонатом свинца.
Висмут и свинец образуют с ЭДТА устойчивые комплексы. максимумы поглощения которых находятся при различных длинах волн. PbNa2Y максимально поглощает при =240 нм, а BiNa2Y – при =265 нм (рис.3). Это позволяет определять висмут в присутствии свинца (определение проводят в УФ области).
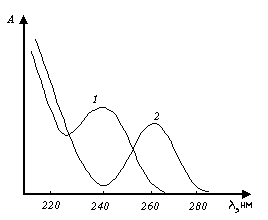
Рис 3. Спектры поглощения комплексонатов висмута (2) и свинца (1).
Для измерения выбирают спектральную область, соответствующую
λмакс= 265 нм, в которой определяемое вещество (комплексонат висмута) поглощает излучение, а второе вещество (комплексонат свинца) его не поглощает. Концентрацию висмута находят по калибровочной кривой или вычисляют по формуле:
![]()
Концентрацию свинца находят аналогично при λ = 240 нм.
Оборудование и реактивы
Спектрофотометр.
Кюветы 1 см, 4 шт.
Колбы мерные, 50 мл.
Стандартный раствор висмута, 0,1 мг/мл;( Навеску 0,1 г висмута обрабатывают HNO3, выпаривают с 5 мл H2SO4 (d = 1,84 г/см3), разбавляют 10%-ным раствором H2SO4 до 1 л, раствор содержит Bi - 0,1 мг/мл).
Стандартный раствор свинца, 0,1 мг/мл.
ЭТДА, трилон Б, 0,001 М раствор.
