
- •Глава 7. Вещества, экстрагируемые органическими растворителями из щелочной среды
- •7.1.Общая характеристика веществ основного характера.
- •7.2. Физико-химические свойства алкалоидов.
- •7.3. Факторы, влияющие на степень экстракции алкалоидов.
- •7.4. Общие методы анализа алкалоидов.
- •7.5. Подтверждающие методы анализа алкалоидов и синтетических азотистых оснований.
- •7.6. Количественное определение алкалоидов.
- •7.7. Классификация алкалоидов.
- •Глава 8. Химико-токсикологический анализ алкалоидов и синтетических лекарственных веществ основного характера.
- •8.1. Производные тропана.
- •8.2. Производные фенотиазина.
- •8.3. Алкалоиды, производные морфинана (фенантренизохиналина) и их синтетические аналоги.
- •8.4. Промедол.
- •8.5. Хинин.
- •8.6. Папаверин.
- •8.7. Стрихнин.
- •8.8. Эфедрин.
- •8.9. Пахикарпин.
- •8.10. Анабазин
- •8.11. Никотин.
- •8.12. Новокаин и новокаинамид.
- •Глава 9. . Тсх- скрининг лекарственных соединений
- •9.1. Общая схема обнаружения неизвестного яда.
- •Подтверждающие исследования
- •9.2. Исследования веществ кислотного и слабоосновного характера в общих системах растворителей.
- •9.4. Исследование веществ основного характера в общих системах растворителей.
- •Глава 10. Группа веществ, изолируемых из биологического материала неполярными растворителями (ядохимикаты).
- •10.1. Классификации ядохимикатов
- •10.2. Общая характеристика ядохимикатов
- •10.3. Схема систематического анализа биологических жидкостей на основные группы пестицидов
- •10.4. Схемы изолирования некоторых групп пестицидов из биологических тканей
- •10.5. Извлечение пестицидов из биологических тканей
- •10.6. Методы определения пестицидов, выделенных из биоматериала или экологических проб
- •10.7. Фосфорсодержащие пестициды. Общая характеристика, свойства, токсикологическое значение, изолирование, анализ.
- •10.8. Хлорорганические соединения. Экологические аспекты, пробоподготовка, особенности метаболизма.
- •10.9. Карбамилы.
- •10.10. Синтетические пиретроиды. Токсикологическое значение, особенности строения, изолирования и анализа
- •10.11. Полихлорированные бифенилы
- •Глава 11. Вещества, изолируемые настаиванием исследуемых объектов с водой.
- •11.1. Серная кислота.
- •11.2. Азотная кислота.
- •11.3. Хлороводородная кислота.
- •11.4. Щелочи и аммиак.
- •11.5. Соли щелочных металлов.
- •Глава 12. Вещества, требующие особых методов изолирования.
- •12.1. Фториды.
- •12.2. Кремнефториды.
- •Глава 13 вещества, определяемые непосредственно в биоматериале.
- •13.1.Отравления монооксидом углерода.
- •13.2. Методы обнаружения и количественного определения монооксида углерода.
- •Глава 14. Методы лабораторной диагностики острых отравлений.
- •14.1. Общая характеристика методов.
- •14.3. Хроматографические методы.
- •Глава 15. Анализ питьевых, сточных вод и пищевых продуктов.
- •15.1. Особенности анализа сточных вод.
- •15.2. Методы концентрирования микропримесей.
- •15.3. Отбор и консервирование проб.
- •15.4. Основные показатели качества вод.
- •15.5. Химическое и биохимическое потребление кислорода.
- •15.6. Определение металлов.
- •15.7. Определение органических веществ.
- •15.8. Анализ пищевых продуктов.
- •Литература
- •Вопросы тестового контроля знаний студентов по токсикологической химии
- •Оглавление
- •Токсикологическая химия
- •210602, Витебск, Фрунзе 27
- •210602, Витебск, Фрунзе 27
8.4. Промедол.
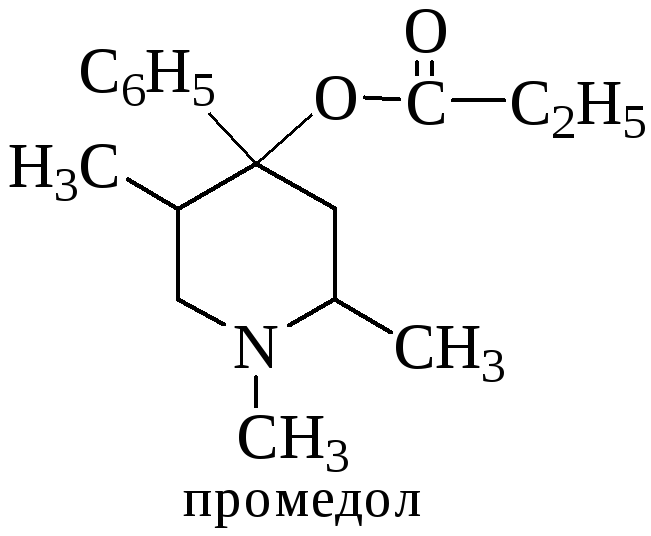
Промедол обладает сильной анальгезирующей активностью, быстро всасывается как при приеме внутрь, так и при парентеральном введении. Применяется как болеутоляющее средство при травмах и различных заболеваниях. Действие промедола на организм наступает через 10 – 20 мин после подкожного введения и продолжается в течение 3 – 4 часов. При длительном применении промедола развивается болезненное пристрастие к нему.
Промедол растворяется в воде, спирте, хлороформе, но не растворяется в эфире. Обладает основными свойствами (рКвн+ = 9).
Изолирование из тканей органов проводят подкисленной водой или подкисленным спиртом, экстрагируют хлороформом из растворов с рН 7 – 9. Промедол частично экстрагируется хлороформом и из кислых растворов.
Качественное обнаружение:
- с общеалкалоидными реактивами;
- с реактивом Марки (пурпурно-красное окрашивание);
- МКС – реакция с ализариновым красным (желтые игольчатые кристаллы).
Метаболизм.
Выделяют два основные пути метаболизма: 1) N- деметилирование и образование N- глюкуронида; 2) разрушение эфирной связи и образование O- глюкуронида.
8.5. Хинин.
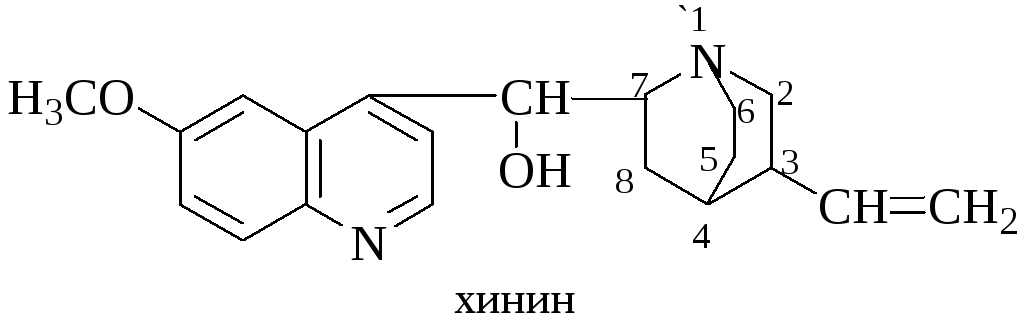
В молекуле хинина содержится хинолиновый и хинуклидиновый циклы, связанные группой –СНОН. Хинин содержится в коре различных видов хинного дерева.
Характерным свойством хинина является его противомалярийная активность. Применяется также в акушерской практике для возбуждения и усиления родовой деятельности.
Основание хинина хорошо растворяется в хлороформе, эфире, этаноле, слабо растворяется в воде (1:1560). Гидрохлорид хинина растворяется в этаноле (1:1), слабо растворяется в эфире. Сульфат хинина растворяется в этаноле (1:95), слабо растворяется в воде (1:810), хлороформе и эфире.
Хинин обладает
основными свойствами:
![]() = 8,5 (азот хинуклидинового кольца) и
= 8,5 (азот хинуклидинового кольца) и
![]() =
4,1. Оптимальные условия экстракции
хлороформом – рН 9 – 10.
=
4,1. Оптимальные условия экстракции
хлороформом – рН 9 – 10.
Обнаружение:
1. С общеалкалоидными реактивами.
2. Флуоресценция сернокислых растворов хинина.
3. Талейохинная проба: при взаимодействии хинина с бромной водой и аммиаком образуется талейохин, экстрагируемый хлороформом (зеленая окраска).
4. Эритрохинная реакция: появление розовой окраски при обработке пробы серной (уксусной) кислотой, бромной водой, раствором гексацианоферрата (III) калия и аммиаком.
Метаболизм.
Хинин связывается с белками на 70 – 90 %, период полувыведения составляет 4 – 15 часов. В результате окисления хинуклидинового и хинолинового циклов образуются 2- гидроксихинин и 2*- гидроксихинин. При метаболизме окисляется также винильная группа до эпоксида и диола. Выделен и продукт О- деметилирования (дезметилхинин). Метаболиты и часть несвязанного хинина (3 – 5%) выделяется с мочой и калом.
8.6. Папаверин.
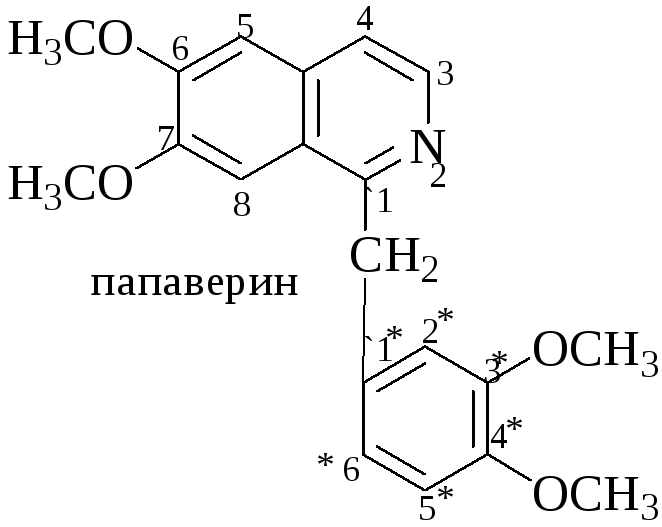
Папаверин содержится в опии (0,1 – 1,5%), понижает тонус и уменьшает сократительную деятельность гладкой мускулатуры, в связи с этим оказывает сосудорасширяющее и спазмолитическое действие. Входит в состав многих сложных лекарственных форм в сочетании с другими препаратами.
Гидрохлорид и сульфат папаверина растворяются в воде, этаноле, хлороформе, слабо растворяются в эфире. Основание папаверина не растворяется в воде, слабо растворяется в эфире и хлороформе. Папаверин – слабое основание (рКвн+ = 6), связывается с белками на 90%, период полувыведения составляет 4 –15 часов. Экстрагируется хлороформом из кислых и щелочных растворов.
Обнаружение:
1. Общеалкалоидные реактивы.
2. Цветные реакции с реактивами Марки, Фреде, Эрдмана.
3. МКС реакция с хлоридом кадмия (тонкие кристаллы, имеющие форму куба).
4. УФ- спектр (250, 284, 310 нм).
Метаболизм.
Основной путь метаболизма – О- деметилирование и образование глюкуронидов и сульфатов.
