- •Глава 7. Вещества, экстрагируемые органическими растворителями из щелочной среды
- •7.1.Общая характеристика веществ основного характера.
- •7.2. Физико-химические свойства алкалоидов.
- •7.3. Факторы, влияющие на степень экстракции алкалоидов.
- •7.4. Общие методы анализа алкалоидов.
- •7.5. Подтверждающие методы анализа алкалоидов и синтетических азотистых оснований.
- •7.6. Количественное определение алкалоидов.
- •7.7. Классификация алкалоидов.
- •Глава 8. Химико-токсикологический анализ алкалоидов и синтетических лекарственных веществ основного характера.
- •8.1. Производные тропана.
- •8.2. Производные фенотиазина.
- •8.3. Алкалоиды, производные морфинана (фенантренизохиналина) и их синтетические аналоги.
- •8.4. Промедол.
- •8.5. Хинин.
- •8.6. Папаверин.
- •8.7. Стрихнин.
- •8.8. Эфедрин.
- •8.9. Пахикарпин.
- •8.10. Анабазин
- •8.11. Никотин.
- •8.12. Новокаин и новокаинамид.
- •Глава 9. . Тсх- скрининг лекарственных соединений
- •9.1. Общая схема обнаружения неизвестного яда.
- •Подтверждающие исследования
- •9.2. Исследования веществ кислотного и слабоосновного характера в общих системах растворителей.
- •9.4. Исследование веществ основного характера в общих системах растворителей.
- •Глава 10. Группа веществ, изолируемых из биологического материала неполярными растворителями (ядохимикаты).
- •10.1. Классификации ядохимикатов
- •10.2. Общая характеристика ядохимикатов
- •10.3. Схема систематического анализа биологических жидкостей на основные группы пестицидов
- •10.4. Схемы изолирования некоторых групп пестицидов из биологических тканей
- •10.5. Извлечение пестицидов из биологических тканей
- •10.6. Методы определения пестицидов, выделенных из биоматериала или экологических проб
- •10.7. Фосфорсодержащие пестициды. Общая характеристика, свойства, токсикологическое значение, изолирование, анализ.
- •10.8. Хлорорганические соединения. Экологические аспекты, пробоподготовка, особенности метаболизма.
- •10.9. Карбамилы.
- •10.10. Синтетические пиретроиды. Токсикологическое значение, особенности строения, изолирования и анализа
- •10.11. Полихлорированные бифенилы
- •Глава 11. Вещества, изолируемые настаиванием исследуемых объектов с водой.
- •11.1. Серная кислота.
- •11.2. Азотная кислота.
- •11.3. Хлороводородная кислота.
- •11.4. Щелочи и аммиак.
- •11.5. Соли щелочных металлов.
- •Глава 12. Вещества, требующие особых методов изолирования.
- •12.1. Фториды.
- •12.2. Кремнефториды.
- •Глава 13 вещества, определяемые непосредственно в биоматериале.
- •13.1.Отравления монооксидом углерода.
- •13.2. Методы обнаружения и количественного определения монооксида углерода.
- •Глава 14. Методы лабораторной диагностики острых отравлений.
- •14.1. Общая характеристика методов.
- •14.3. Хроматографические методы.
- •Глава 15. Анализ питьевых, сточных вод и пищевых продуктов.
- •15.1. Особенности анализа сточных вод.
- •15.2. Методы концентрирования микропримесей.
- •15.3. Отбор и консервирование проб.
- •15.4. Основные показатели качества вод.
- •15.5. Химическое и биохимическое потребление кислорода.
- •15.6. Определение металлов.
- •15.7. Определение органических веществ.
- •15.8. Анализ пищевых продуктов.
- •Литература
- •Вопросы тестового контроля знаний студентов по токсикологической химии
- •Оглавление
- •Токсикологическая химия
- •210602, Витебск, Фрунзе 27
- •210602, Витебск, Фрунзе 27
10.8. Хлорорганические соединения. Экологические аспекты, пробоподготовка, особенности метаболизма.
В отличие от ФОС хлорорганические ядохимикаты химически инертные малополярные соединения, практически не растворимы в воде, характеризуются длительной сохраняемостью в окружающей среде (например, в почве от 2-15 лет до 50 лет) и организме животных и человека. Свойства некоторых ХОС приведены в таблице 3.
Таблица 3.
|
Название |
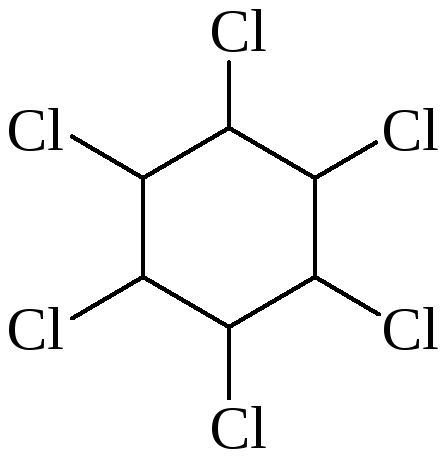
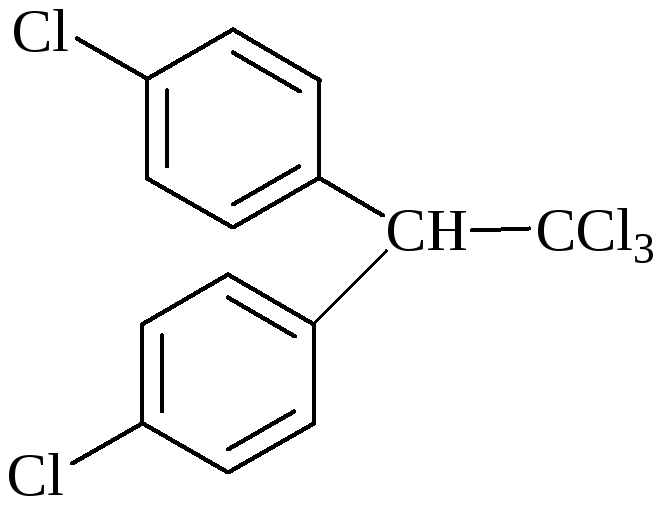
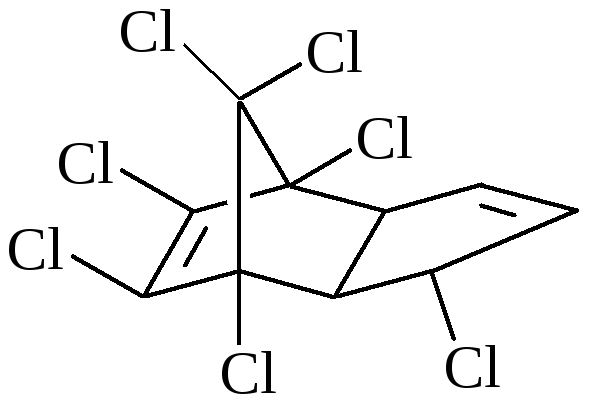
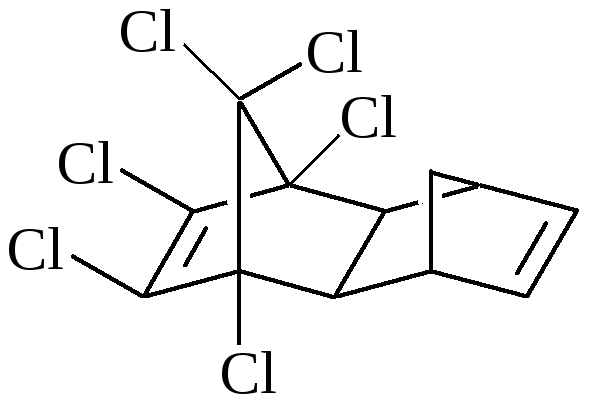
Химическая структура |
М, г/моль |
Растворимость |
LD50, мг/кг |
|
Гексахлорциклогексан (ГХЦГ) -ГХЦГ - линдан |
|
291 |
Н.р. –Н2О, х.р.Bz,ROH, С6Н14 |
125 (-ГХЦГ) |
|
4,4’ – ДДТ (4,4’-дихлордифенилтрихлорэтан) |
|
354 |
Н.р.-Н2О, х.р. –Et2O, Ац,Bz, хлф,EtOH |
250-400 |
|
Гептахлор |
|
373 |
н.р.- H2O, р. EtOH |
|
|
Альдрин |
|
365 |
н.р. – H2O, р.EtOH, Ац,Bz,CCl4 |
|
Поражающее действие ХОС связано с параличом нервной системы. Высоколипофильные ХОС нарушают структуру мембран нервных клеток и препятствуют прохождению нервных импульсов.
В настоящее время использование ХОС как инсектицидов в сельском хозяйстве запрещено практически во всех странах. Связано это в первую очередь с их чрезвычайно высокой устойчивостью как во внешней среде (почва, вода), так и в продуктах питания (даже после термической и кулинарной обработки). Из-за этого ХОС накапливаются в жировой ткани, печени и других богатых липидами органах человека и их содержание у здорового взрослого человека в жировой ткани может достигать десятков миллиграмм на килограмм. Таким образом, данные вещества могут быть обнаружены в органах при ненаправленном судебно-химическом (или ХТА) исследовании. Вероятность этого велика при анализе методом ГЖХ с ДЭЗ. Поэтому важно правильно интерпретировать полученные результаты и обязательно проводить количественное определение. Препараты хлорорганических инсектицидов много лет не производятся, поэтому острые отравления ХОС не встречаются.
Изолирование ХОС из биологических тканей проводят неполярными или малополярными растворителями – бензол, гексан, ацетон и др. Особенностью очистки при извлечении ХОС является то, что гексановое извлечение или сухой остаток после упаривания извлекателя обрабатывают концентрированной серной кислотой для разрушения эндогенных веществ (липидов и др. неполярных компонентов). При этом ХОС не разрушаются и после нейтрализации извлечения их определяют методами ТСХ и ГЖХ.
Разделение ХОС в тонких слоях силикагеля проводят с использованием малополярных элюентов (гексан-ацетон (4:1), гексан-бензол и другие). Проявление пятен проводят аммиачным раствором AgNO3.
Наиболее чувствительным и селективным методом определения ХОС является ГЖХ с ДЭЗ. Разделение проводится на малополярных силиконовых фазах – OV-17, режеSE-30, причем как на насадочных колонках (длина 1-2 метра), так и на более эффективных капиллярных колонках длиной до 50 метров. Поскольку ХОС имеют различные свойства (летучесть, число атомов галогена), то чаще всего при их разделении используется режим программирования температуры (от 150 до 250С). Высокая чувствительность ГЖХ с ДЭЗ, однако, может приводить к появлению ложноположительных результатов (т.е. могут обнаруживаться пики-артефакты из-за недостаточной чистоты реактивов, посуды, хроматографического шприца и т.д.).
М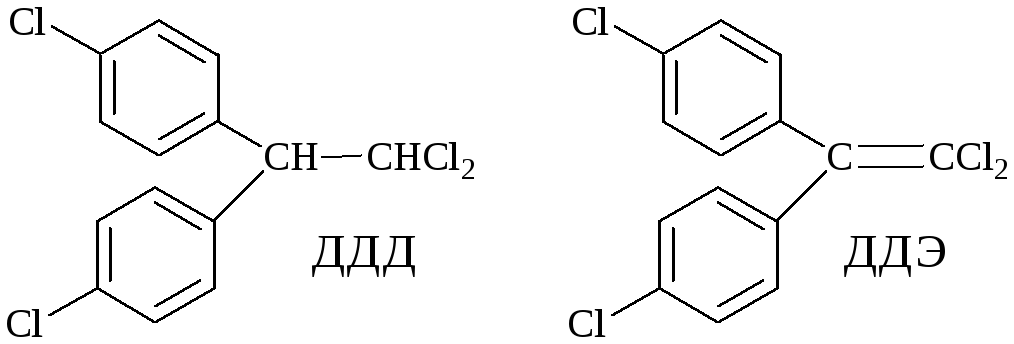 етаболические
превращения ХОС многообразны и связаны
в первую очередь с дегалогенированием
молекулы под действием ферментов.
Метаболизм ДДТ протекает с
дегидрохлорированием алифатической
цели трихлорэтана с образованием вначале
ДДД, а затем после дегидрохлорирования
– ДДЭ. Образовавшиеся метаболиты еще
более устойчивы, чем ДДТ, сохраняются
и накапливаются в организме человека.
Токсическая и смертельная концентрация
ХОС в крови значительно ниже, чем у
большинства ФОС и составляет 20-500 нг/мл
(линдан, альдрин). Значительно большие
концентрации этих веществ в жировой
ткани и печени (ДДТ – 40-650 мкг/г, 350 мкг/г
– линдан).
етаболические
превращения ХОС многообразны и связаны
в первую очередь с дегалогенированием
молекулы под действием ферментов.
Метаболизм ДДТ протекает с
дегидрохлорированием алифатической
цели трихлорэтана с образованием вначале
ДДД, а затем после дегидрохлорирования
– ДДЭ. Образовавшиеся метаболиты еще
более устойчивы, чем ДДТ, сохраняются
и накапливаются в организме человека.
Токсическая и смертельная концентрация
ХОС в крови значительно ниже, чем у
большинства ФОС и составляет 20-500 нг/мл
(линдан, альдрин). Значительно большие
концентрации этих веществ в жировой
ткани и печени (ДДТ – 40-650 мкг/г, 350 мкг/г
– линдан).