
- •Глава 7. Вещества, экстрагируемые органическими растворителями из щелочной среды
- •7.1.Общая характеристика веществ основного характера.
- •7.2. Физико-химические свойства алкалоидов.
- •7.3. Факторы, влияющие на степень экстракции алкалоидов.
- •7.4. Общие методы анализа алкалоидов.
- •7.5. Подтверждающие методы анализа алкалоидов и синтетических азотистых оснований.
- •7.6. Количественное определение алкалоидов.
- •7.7. Классификация алкалоидов.
- •Глава 8. Химико-токсикологический анализ алкалоидов и синтетических лекарственных веществ основного характера.
- •8.1. Производные тропана.
- •8.2. Производные фенотиазина.
- •8.3. Алкалоиды, производные морфинана (фенантренизохиналина) и их синтетические аналоги.
- •8.4. Промедол.
- •8.5. Хинин.
- •8.6. Папаверин.
- •8.7. Стрихнин.
- •8.8. Эфедрин.
- •8.9. Пахикарпин.
- •8.10. Анабазин
- •8.11. Никотин.
- •8.12. Новокаин и новокаинамид.
- •Глава 9. . Тсх- скрининг лекарственных соединений
- •9.1. Общая схема обнаружения неизвестного яда.
- •Подтверждающие исследования
- •9.2. Исследования веществ кислотного и слабоосновного характера в общих системах растворителей.
- •9.4. Исследование веществ основного характера в общих системах растворителей.
- •Глава 10. Группа веществ, изолируемых из биологического материала неполярными растворителями (ядохимикаты).
- •10.1. Классификации ядохимикатов
- •10.2. Общая характеристика ядохимикатов
- •10.3. Схема систематического анализа биологических жидкостей на основные группы пестицидов
- •10.4. Схемы изолирования некоторых групп пестицидов из биологических тканей
- •10.5. Извлечение пестицидов из биологических тканей
- •10.6. Методы определения пестицидов, выделенных из биоматериала или экологических проб
- •10.7. Фосфорсодержащие пестициды. Общая характеристика, свойства, токсикологическое значение, изолирование, анализ.
- •10.8. Хлорорганические соединения. Экологические аспекты, пробоподготовка, особенности метаболизма.
- •10.9. Карбамилы.
- •10.10. Синтетические пиретроиды. Токсикологическое значение, особенности строения, изолирования и анализа
- •10.11. Полихлорированные бифенилы
- •Глава 11. Вещества, изолируемые настаиванием исследуемых объектов с водой.
- •11.1. Серная кислота.
- •11.2. Азотная кислота.
- •11.3. Хлороводородная кислота.
- •11.4. Щелочи и аммиак.
- •11.5. Соли щелочных металлов.
- •Глава 12. Вещества, требующие особых методов изолирования.
- •12.1. Фториды.
- •12.2. Кремнефториды.
- •Глава 13 вещества, определяемые непосредственно в биоматериале.
- •13.1.Отравления монооксидом углерода.
- •13.2. Методы обнаружения и количественного определения монооксида углерода.
- •Глава 14. Методы лабораторной диагностики острых отравлений.
- •14.1. Общая характеристика методов.
- •14.3. Хроматографические методы.
- •Глава 15. Анализ питьевых, сточных вод и пищевых продуктов.
- •15.1. Особенности анализа сточных вод.
- •15.2. Методы концентрирования микропримесей.
- •15.3. Отбор и консервирование проб.
- •15.4. Основные показатели качества вод.
- •15.5. Химическое и биохимическое потребление кислорода.
- •15.6. Определение металлов.
- •15.7. Определение органических веществ.
- •15.8. Анализ пищевых продуктов.
- •Литература
- •Вопросы тестового контроля знаний студентов по токсикологической химии
- •Оглавление
- •Токсикологическая химия
- •210602, Витебск, Фрунзе 27
- •210602, Витебск, Фрунзе 27
10.4. Схемы изолирования некоторых групп пестицидов из биологических тканей
Основным отличием схем изолирования органических веществ из биотканей (органов) от изолирования из биологических жидкостей является наличие стадии настаивания (извлечения) веществ из твердых тканей печени, почки и др. В качестве извлекателей, как правило, используются малополярные или полярные органические растворители, однако, для изолирования отдельных веществ (хлорофос и др. ФОС) используют водно-ацетоновые смеси. После настаивания вытяжки подвергают очистке от жиров и др. эндогенных веществ методамигрубой очистки - вымораживание, фильтрование. Для тонкой очистки используют несколько вариантов:
1. Очистка в системе гексан (ГК)-ацетонитрил (MeCN). Сухой остаток после упаривания извлекателя или экстрагента обрабатывают гексаном, а затем прибавляютMeCNи встряхивают смесь. После чего слойMeCN(нижний) отделяют, гексановый слой отбрасывают. К ацетонитрильному экстракту прибавляют водный растворNa2SO4и экстрагируют ядохимикаты гексаном. Метод применим при изолировании ФОС, пиретроидов.
2. Сорбционная очистка может включать как адсорбцию целевых компонентов (сорбенты - активированный уголь, ХМК и др.) с последующим элюированием ядохимикатов, так и адсорбцию балластных веществ (полярные сорбенты - силоксид, диатомиты и др.).
Очистка методом ТСХ.
Очистка с использованием концентрированной серной кислоты (для ХОС).
Микровозгонка в вакууме (некоторые ФОС).
Перегонка с водяным паром (ГХЦГ).
После очистки извлечений проводится экстракция (или элюирование) ядохимикатов при помощи органических растворителей или их смесей. Органический экстракт затем упаривают на роторном испарителе (в вакууме), поскольку ФОС, пиретроиды и некоторые другие группы пестицидов легко разлагаются при нагревании в присутствии кислорода или гидролизуются. Затем сухой остаток растворяют в подходящем растворителе и анализируют.
Рассмотрим несколько схем выделения ФОС, пиретроидов и ХОС из биологического материала.
10.5. Извлечение пестицидов из биологических тканей
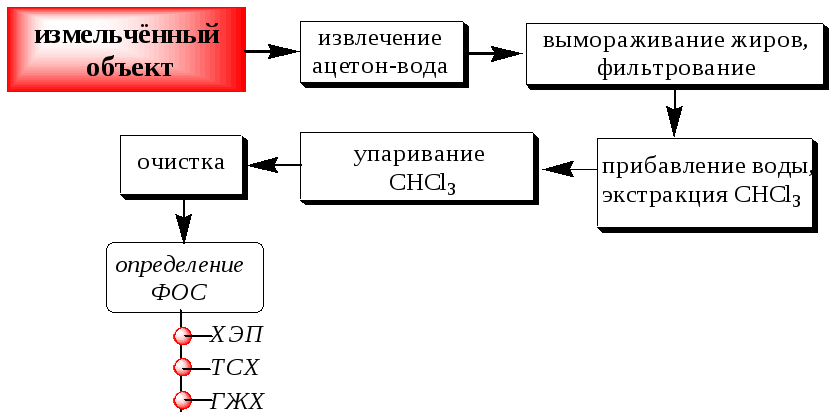
Схема извлечения ФОС включает настаивание измельченного органа со смесью вода-ацетон (есть варианты - ацетон-гексан, дихлорметан, ацетон, ацетонитрил (см. ниже)), вымораживание жиров, экстракцию хлороформом или гексаном, проведение дополнительной очистки (если необходимо) и анализ.
Похожая схема используется и для изолирования синтетических пиретроидов. Для извлечения используют хлороформ, затем проводят очистку от жиров, экстракцию гексаном, очистку экстракта от эндогенных веществ активированным углем и анализ.
Несколько сложнее проводится извлечение ХОС и ПХБ из жировой ткани. Вначале образец растирают с безводным сульфатом натрия, проводят извлечение гексаном, затем экстракт очищают при помощи концентрированной серной кислоты, отмывают экстракт от серной кислоты, сушат, упаривают и проводят анализ.
10.6. Методы определения пестицидов, выделенных из биоматериала или экологических проб
Для достоверного определения выделенных из биоматериала ядохимикатов в основном применяют два метода - один для обнаружения (например, ТСХ, холинэстеразная проба, иммуноферментный анализ), второй - для подтверждения и количественного определения. Второй метод должен быть более селективным и чувствительным, чем первый. Это чаще всего ГЖХ с селективными детекторами, ГХ/МС, реже фотометрия и ВЭЖХ. При анализе технических жидкостей используют также химический метод - элементный анализ и качественные реакции.
Химические методы анализа ядохимикатов. Эта группа методов включает элементный анализ (обнаружение атомов галогена, серы, фосфора или азота в органических веществах) и реакции качественного обнаружения (реакции на функциональные группы, реакции окрашивания с концентрированными кислотами или щелочами, реакции, используемые для проявления пестицидов после ТСХ-разделения). Химические методы чаще всего используют при анализе неизвестных образцов технических препаратов ядохимикатов, значительно реже – при судебно-химическом исследовании органов трупа (очевидно, из-за невысокой чувствительности и селективности этих методов).
Элементный анализ основан на разрушении молекулы органического (или элементорганического) вещества при действии различных химических (щелочные металлы, оксиды металлов, концентрированные кислоты и др.) и физических (нагревание) воздействий с последующим обнаружением соединения, содержащего анализируемый элемент.
По результатам элементного анализа можно определить групповую принадлежность пестицида. Например, если обнаружено наличие фосфора и доказано отсутствие хлора, то можно сделать вывод, что данный ядохимикат не относится к хлорорганическим соединениям, а относится к органическим соединениям фосфора.
Соединения, которые подвергаются элементному анализу должны быть достаточно чистыми, перед проведением анализа их следует освободить от примесей.
Обнаружение фосфора: обнаружение складывается из двух этапов: минерализация (разрушение молекулы исследуемого вещества и переведение фосфора вPO43-) и обнаружениеPO43-в минерализате.
Известно несколько способов минерализации, используемых при обнаружении фосфора:
минерализация с СаО:в платиновый тигель вносят немного СаО и несколько капель раствора исследуемого вещества. Смесь нагревают до выпаривания жидкости. Если анализируют твёрдое вещество, то его вносят в тигель и прибавляют СаО. После этого тигель постепенно нагревают на небольшом пламени газовой горелки, затем увеличивают пламя и продолжают нагревать до красного каления тигля. Затем тигель охлаждают и его содержимое растворяют в нескольких мл 2 М раствора азотной кислоты.
минерализация с карбонатом и пероксидом натрия:в платиновый или никелевый тигель вносят немного смеси, приготовленной из 0,2 г безводногоNa2CO3 и 0,5 гNa2O2, и небольшое количество исследуемого вещества (либо несколько капель раствора или вытяжки). Тигель осторожно нагревают до испарения жидкости. Затем увеличивают пламя и нагревают до расплавления смеси. Затем тигель охлаждают, его содержимое переносят в небольшую фарфоровую чашку, прибавляют немного карбоната натрия, 10 мл воды. Смесь тщательно растирают.
Перед обнаружением фосфат – ионов в минерализате из него необходимо предварительно удалить ионы AsO4-, которые дают сходные реакции и мешают проведению анализа. Для этого минерализат подкисляют хлороводородной кислотой до рН~0,5 и пропускают сероводород. Выделившийся осадок (As2S3+S) отфильтровывают. Арсенат-ионы можно также перевести в арсенит-ионы (добавлением сульфита натрия), которые не мешают обнаружению фосфата.
Для обнаружения фосфат-ионов используют реакцию образования молибденовой сини:
H3PO4 + 12(NH4)2MoO4 + 21HNO3 → (NH4)3[PMo12O40]∙6H2O↓ + 21NH4NO3 + 6H2O
К образовавшемуся осадку жёлтого цвета добавляют восстановитель (бензидин, аскорбиновая кислота и т.п.). Появляется синее окрашивание.
Обнаружение азота:исследуемое соединение минерализуют сплавлением с металлическим натрием или калием по Лассеню. Цианид-ионы обнаруживают по реакции образования берлинской лазури или бензидиновой сини.
Если в молекуле вещества присутствуют одновременно азот и сера, то при минерализации образуются роданид-ионы, которые можно обнаружить по реакции образования красного роданида железа (III).
Обнаружение серы:при сплавлении исследуемого вещества со щелочными металлами образуется ионыS2-, которые затем обнаруживают реакциями с хлоридом кадмия, нитропруссидом.
При сплавлении исследуемого вещества со смесью карбоната и пероксида натрия сера, входящая в состав его молекулы, окисляется до сульфат-иона, который можно затем обнаружить с солями бария.
Обнаружение хлора: органически связанный хлор переводят с помощью различных реагентов в ионное состояние и затем обнаруживают его в минерализате реакцией с нитритом серебра.
Для перевода хлора, содержащегося в молекуле исследуемого вещества, в хлорид-ион используют:
- сплавление с металлическим натрием или калием;
- взаимодействие с натрием и этанолом;
- нагревание со смесью азотной и серной кислот;
- нагревание со смесью дихромата калия и серной кислотой и др.
Химические реакции качественного обнаружения ядохимикатов в настоящее время актуальны при визуализации разделенных соединений на пластинах ТСХ. Среди наиболее употребляемых реактивов следует отметить о-толидиновый реактив (проявление ФОС), аммиачный раствор нитрата серебра с последующим облучением УФ-светом (проявление ХОС, синтетических пиретроидов, группы 2,4-Д и др.).
Широкое использование хроматографических методов в анализе пестицидов требует более подробного их рассмотрения.
1. ТСХ-анализ состоит изследующих этапов: нанесение пробы и стандартных веществ на пластину, элюирование (разделение) в камере с подвижной фазой, высушивание пластины, проявление разделенных компонентов, расчет величин удерживания (Rf), идентификация веществ. В качестве подвижных фаз для разделения ядохимикатов в тонких слоях силикагеля используют смеси органических растворителей - гексан-ацетон в различных соотношениях, толуол-ацетон, смеси хлороформа, гексана, ацетонитрила и др. Как уже отмечалось, для проявления ХОС, пиретроидов используют раствор нитрата серебра с последующим облучением УФ-светом. Для проявления ФОС используют обработку бромфеноловым синим и раствором лимонной кислоты, а также о-толидиновый реактив.
2. ГЖХ. Ядохимикаты в большинстве своем являются высококипящими жидкостями или твердыми веществами, поэтому для их разделения в ГХ используют термостойкие НЖФ - силиконовые фазы, реже - эфиры полиэтиленгликоля или ПЭГ-20000. В таблице1приведены некоторые типичные условия ГХ-определения некоторых ядохимикатов.
Таблица. Условия газохроматографического определения некоторых пестицидов
|
Пестициды |
НЖФ |
Температурный режим |
Детектор |
Предел обнаружения |
|
ХОС |
OV-17, SE-30 |
180-220С |
ДЭЗ, ДПР |
10-13 г в пробе (-ГХЦГ) |
|
ПХБ |
OV-17, SE-30 (капиллярная) |
230-270С (чаще программирование температуры) |
МС, ДЭЗ |
10-14 г в пробе |
|
Синтетические пиретроиды |
OV-17, OV-1 |
250-280С |
ДЭЗ, ДПР, МС |
10-11 г в пробе (карате) |
|
ФОС |
SE-30, OV-225, OV-210 |
150-200С |
ДТИ, МС, ПФД |
10-13 г в пробе (метафос) |
