
- •Глава 7. Вещества, экстрагируемые органическими растворителями из щелочной среды
- •7.1.Общая характеристика веществ основного характера.
- •7.2. Физико-химические свойства алкалоидов.
- •7.3. Факторы, влияющие на степень экстракции алкалоидов.
- •7.4. Общие методы анализа алкалоидов.
- •7.5. Подтверждающие методы анализа алкалоидов и синтетических азотистых оснований.
- •7.6. Количественное определение алкалоидов.
- •7.7. Классификация алкалоидов.
- •Глава 8. Химико-токсикологический анализ алкалоидов и синтетических лекарственных веществ основного характера.
- •8.1. Производные тропана.
- •8.2. Производные фенотиазина.
- •8.3. Алкалоиды, производные морфинана (фенантренизохиналина) и их синтетические аналоги.
- •8.4. Промедол.
- •8.5. Хинин.
- •8.6. Папаверин.
- •8.7. Стрихнин.
- •8.8. Эфедрин.
- •8.9. Пахикарпин.
- •8.10. Анабазин
- •8.11. Никотин.
- •8.12. Новокаин и новокаинамид.
- •Глава 9. . Тсх- скрининг лекарственных соединений
- •9.1. Общая схема обнаружения неизвестного яда.
- •Подтверждающие исследования
- •9.2. Исследования веществ кислотного и слабоосновного характера в общих системах растворителей.
- •9.4. Исследование веществ основного характера в общих системах растворителей.
- •Глава 10. Группа веществ, изолируемых из биологического материала неполярными растворителями (ядохимикаты).
- •10.1. Классификации ядохимикатов
- •10.2. Общая характеристика ядохимикатов
- •10.3. Схема систематического анализа биологических жидкостей на основные группы пестицидов
- •10.4. Схемы изолирования некоторых групп пестицидов из биологических тканей
- •10.5. Извлечение пестицидов из биологических тканей
- •10.6. Методы определения пестицидов, выделенных из биоматериала или экологических проб
- •10.7. Фосфорсодержащие пестициды. Общая характеристика, свойства, токсикологическое значение, изолирование, анализ.
- •10.8. Хлорорганические соединения. Экологические аспекты, пробоподготовка, особенности метаболизма.
- •10.9. Карбамилы.
- •10.10. Синтетические пиретроиды. Токсикологическое значение, особенности строения, изолирования и анализа
- •10.11. Полихлорированные бифенилы
- •Глава 11. Вещества, изолируемые настаиванием исследуемых объектов с водой.
- •11.1. Серная кислота.
- •11.2. Азотная кислота.
- •11.3. Хлороводородная кислота.
- •11.4. Щелочи и аммиак.
- •11.5. Соли щелочных металлов.
- •Глава 12. Вещества, требующие особых методов изолирования.
- •12.1. Фториды.
- •12.2. Кремнефториды.
- •Глава 13 вещества, определяемые непосредственно в биоматериале.
- •13.1.Отравления монооксидом углерода.
- •13.2. Методы обнаружения и количественного определения монооксида углерода.
- •Глава 14. Методы лабораторной диагностики острых отравлений.
- •14.1. Общая характеристика методов.
- •14.3. Хроматографические методы.
- •Глава 15. Анализ питьевых, сточных вод и пищевых продуктов.
- •15.1. Особенности анализа сточных вод.
- •15.2. Методы концентрирования микропримесей.
- •15.3. Отбор и консервирование проб.
- •15.4. Основные показатели качества вод.
- •15.5. Химическое и биохимическое потребление кислорода.
- •15.6. Определение металлов.
- •15.7. Определение органических веществ.
- •15.8. Анализ пищевых продуктов.
- •Литература
- •Вопросы тестового контроля знаний студентов по токсикологической химии
- •Оглавление
- •Токсикологическая химия
- •210602, Витебск, Фрунзе 27
- •210602, Витебск, Фрунзе 27
8.12. Новокаин и новокаинамид.
К производным пара-аминобензойной кислоты, имеющим токсикологическое значение, относятся новокаин (прокаин), дикаин, новокаинамид и др.
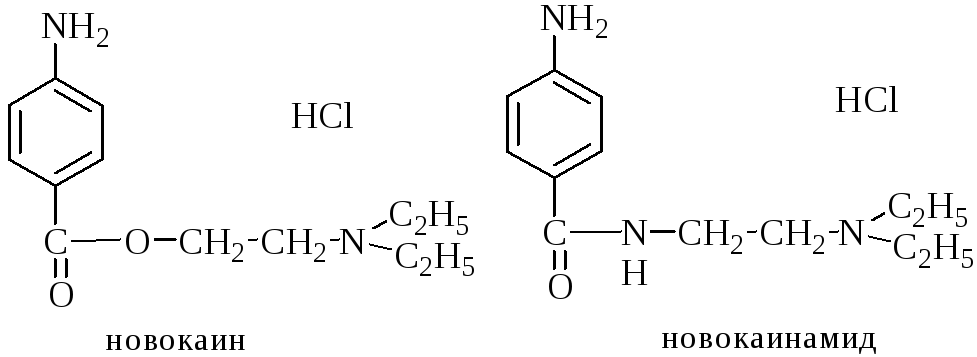
Никотин является местноанестезирующим препаратом, понижает возбудимость периферических холинореактивных систем, уменьшает спазмы гладкой мускулатуры.
Новокаинамид по химическому строению близок к новокаину, хотя по фармакологическим свойствам он применяется как антиаритмическое средство – способен понижать возбудимость и проводимость сердечной мышцы.
Новокаин и новокаинамид растворяются в воде и этаноле, не растворяются в эфире и хлороформе. Обладают основными свойствами (рКвн+=9 для новокаина и 9,24 - для новокаинамида). Имеют характерные интенсивные полосы поглощения в УФ- спектрах, формы спектров изменяются в зависимости от рН.
Изолирование из тканей трупов проводится подкисленной водой, экстракция – хлороформом из щелочных растворов.
Анализ экстрактов проводится методом ТСХ-скрининга в общих и частных системах растворителей. Для качественного обнаружения применяют реакции осаждения (реактив Драгендорфа, раствор бромида золота), окрашивания (образование азокрасителя с бета-нафтолом, оранжево-желтое окрашивание по реакции Витали-Морена), также УФ- спектрофотометрию.
Количественное определение: УФ- спектрофотометрия, фотометрия по реакции образования азокрасителя.
Метаболизм.
Новокаин быстро гидролизуется до пара-аминобензойной кислоты и диэтиламиноэтанола, только 2% этого препарата выделяется с мочой в неизмененном виде. Около 90% дозы новокаина выводится с мочой в виде ПАБК (в свободной форме и в виде коньюгатов). В свободном виде выводится и 30% диэтиламиноэтанола.
Максимальная концентрация новокаинамида обнаруживается в плазме через 15 – 60 минут после орального введения. Основным метаболитом является фармакологически активный N-ацетилновокаинамид. Около 50% новокаинамида выводится с мочой в неизмененном виде, 2-10% метаболизирует до ПАБК. Обнаружены также N- деметилированные метаболиты. Период полувыведения новокаинамида – 3 – 5 часов.
Глава 9. . Тсх- скрининг лекарственных соединений
9.1. Общая схема обнаружения неизвестного яда.
Огромный круг лекарственных веществ, представляющий токсикологический интерес, и постоянное совершенствование методов их анализа привели к формированию процесса идентификации неизвестного лекарственного вещества, ставшего причиной отравления. Этот процесс состоит из 2-х этапов: предварительного, позволяющего выявить принадлежность яда к определенной группе химических соединений, и подтверждающего исследования, которое позволяет идентифицировать конкретное вещество.
Проведение предварительного отбора или «скрининга» может быть основано на использовании разнообразных химических или физико-химических методов. В качестве примера можно привести химический скрининг алкалоидов с общеалкалоидными реактивами. Более совершенным и широко используемым в настоящее время является скрининг исследуемых веществ на основе ТСХ. Он позволяет за минимальное время с достаточно высокой чувствительностью выявить из большого круга лекарственных соединений одно или несколько веществ, чтобы затем целенаправленно выбрать схему химико-токсикологического анализа.
Качественной характеристикой определяемого вещества на данном сорбенте и в данной системе растворителей является величина Rf (отношение расстояния, пройденного веществом, к расстоянию, пройденному растворителем). В соответствии с определением Rf всегда < 1. Величина Rf зависит от техники эксперимента, активности и природы сорбента, толщины слоя сорбента, температуры, качества и толщины слоя сорбента, температуры, качества и природы растворителя, детектирования и др. Отношение величины Rf определяемого вещества к величине Rf стандарта (метчика) обозначают Rst. Воспроизводимые значения Rf и Rst получаются при соблюдении всех методических указаний.
Пробы наносят мерным капилляром, микрошприцом или обычным капилляром на линию старта на расстоянии не менее 1 см от нижнего края пластинки. Диаметр пятна не должен превышать 2-3 мм. Пластины с нанесенной пробой помещают в хроматографическую камеру, при этом слой подвижной фазы должен быть ниже линии старта на 0,5 – 1 см. Расстояние между соседними пробами на стартовой линии должно быть не менее 1 см.
В методе ТСХ используют различные сорбенты (оксид алюминия, силикагель, целлюлоза и др.), нанесенные на пластину.
В качестве хроматографической камеры используют стандартные камеры или стеклянные емкости любой формы, имеющие герметические крышки. В хроматографическую камеру помещают органические растворители или их смеси (подвижная фаза) и насыщают камеру парами растворителя в течении 30 мин. В качестве метчиков (свидетелей) используют субстанции анализируемых («подозреваемых») веществ. Следует иметь в виду, что в случае использования в качестве метчиков лекарственных веществ, извлеченных из таблеток и других лекарственных форм, наблюдается не полное соответствие Rf метчика и определяемого вещества. Обнаружение (детектирование) определяемых веществ на хроматограмме проводят в УФ- свете и после обработки хроматографических пластин специальными реагентами. Пятна, обнаруженные на хроматограмме, копируют и измеряют расстояние от центра пятна до стартовой линии, рассчитывают Rf.
При анализе биологических объектов обязательно проведение холостого и контрольного хроматографического разделения, чтобы выявить влияние фона.
Система ТСХ - скрининга предусматривает поэтапное исследование токсикологически важных соединений: на первом этапе проводится скрининг в общих системах растворителей и, при положительном результате, исследование элюатов в частной системе растворителей.
Критерием выбора общих систем растворителей является разделение определяемых веществ на определенные группы, локализованные в хроматографические зоны.
В основу выбора частных систем растворителей положена высокая эффективность разделения исследуемых соединений, входящих в ту или иную хроматографическую зону.
Обнаружение веществ на хроматограмме осуществляется на основе использования (последовательного или параллельного) реагентов, избирательно реагирующих с лекарственными веществами, входящими в определенную химическую группу.
Метод имеет отрицательное судебно-химическое значение. При положительном результате проводят исследование, включающее: химические реакции, ГЖХ, фотометрию и УФ- спектрофотометрию, фармакологические пробы.
Таким образом, общую схему обнаружения неизвестного яда можно представить следующим образом.
ПРЕДВАРИТЕЛЬНОЕ ИССЛЕДОВАНИЕ
ТСХ в общих системах растворителей
(при положительном результате)

ТСХ в частных системах растворителей
