
- •В.И. Гребенькова, н.Г. Осипенкова, Голубская и.Э., Козлова е.Е. Методические указания к лабораторному практикуму по курсу «Химия»
- •Работа № 1 свойства неорганических соединений различных классов
- •Названия кислотных остатков различных кислот
- •Опыт 1. Изучение окраски индикаторов в различных средах
- •Опыт 2. Оксиды и гидроксиды активных металлов
- •Опыт 3. Оксиды и гидроксиды неметаллов
- •Опыт 3. Изучение свойств оксидов и гидроксидов металлов
- •Опыт 3а). Изучение свойств оксида меди.
- •Опыт 3б. Получение и разложение гидроксида меди
- •Опыт 4. Изучение свойств гидроксидов металлов
- •Опыт 5. Изучение химической активности кислот
- •Опыт 6. Получение малорастворимых кислот и оснований
- •Опыт 7. Получение слабодиссоциирующих оснований и кислот
- •Примеры сильных и слабых оснований
- •Опыт 8. Реакция нейтрализации
- •Опыт 9. Свойства солей
- •Опыт 9а) Взаимодействие солей с кислотами
- •Опыт 10а). Получение солей методом нейтрализации и их взаимодействия
- •Опыт 10б). Получение малорастворимых солей
- •Опыт 11. Качественные реакции на хлорид-, сульфат- и фосфат-ионы
- •Опыт 12. Исследование окраски некоторых катионов и анионов
- •Работа № 2 скорость химических реакций.
- •Опыт 1. Зависимость скорости реакции от концентрации реагирующих веществ
- •Опыт 2. Влияние температуры на скорость химической реакции
- •Опыт 3. Влияние катализатора на скорость химической реакции
- •Работа № 3 Химическое равновесие
- •Опыт 1. Равновесие в растворе хлорида меди
- •Смещение химического равновесия
- •Опыт 2. Влияние концентрации веществ на смещение равновесия обратимой реакции
- •Опыт 3. Влияние температуры на химическое равновесие
- •Опыт 4. Влияние реакции среды на смещение химического равновесия.
- •Бихромат-ион (оранжевый)
- •Работа № 4 Процессы, протекающие при образовании растворов
- •Опыт 1. Изменение температуры при растворении
- •Опыт 2. Изменение объема при растворении
- •Опыт 3. Изменение окраски при растворении
- •Опыт 4.Влияние типа растворителя на процесс растворения.
- •Опыт 5. Зависимость растворимости солей от температуры. Получение пересыщенных растворов
- •При сдаче лабораторной работы ответьте на следующие вопросы
- •Работа № 5 Приготовление растворов заданной концентрации
- •Опыт 1. Приготовление раствора бихромата калия k2Cr2o7 с определенной массовой долей
- •Опыт 2. Приготовление растворов серной кислоты заданной молярной и нормальной концентраций
- •Опыт 3. Определение концентрации кислоты методом титрования
- •Работа № 6 Свойства растворов электролитов
- •Опыт 1. Исследование электропроводности растворов различных веществ
- •Опыт 2. Изучение зависимости степени диссоциации веществ в растворах от их концентрации
- •При сдаче лабораторной работы ответить на следующие вопросы
- •Работа №7 гидролиз
- •Опыт 1. Гидролиз солей, образованных различными по силе основанием и кислотой
- •Опыт 2. Ступенчатый гидролиз солей, образованных различными по силе основанием и кислотой
- •Опыт 3. Гидролиз солей, образованных слабым основанием и слабой летучей кислотой. Полный необратимый гидролиз
- •Количественные характеристики процесса гидролиза
- •Факторы, влияющие на степень гидролиза
- •Работа № 8 окислительно–восстановительные процессы
- •Опыт 1. Сравнительная характеристика окислительных свойств галогенов и восстановительной способности галогенидов
- •Опыт 2. Окислительно–восстановительные свойства соединений, содержащих элементы в различных степенях окисления.
- •Опыт 3. Окислительно–восстановительные свойства пероксида водорода.
- •Опыт 4б. Влияние концентрации кислоты на процесс окисления цинка серной кислотой
- •Опыт 5. Окисление меди разбавленной и концентрированной азотной кислотой
- •Опыт 6. Влияние среды на протекание окислительно–восстановительных реакций.
- •Типы овр
- •Опыт 8. Каталитическое диспропорционирование пероксида водорода.
- •Опыт 9. Реакция внутримолекулярного окисления–восстановления перманганата калия.
- •Опыт 10. Реакция межмолекулярного окисления восстановления между иодидом и иодатом калия.
- •Контрольные задания
- •Работа № 9 электрохимические процессы Химические источники тока. Опыт 1. Изготовление гальванического элемента и расчет его эдс.
- •Коррозия металлов.
- •Опыт 2. Влияние образования гальванических пар на течение химических процессов.
- •Опыт 3. Коррозия оцинкованного и луженого железа.
- •Электролиз водных растворов солей
- •Опыт 4. Электролиз раствора сульфата натрия.
- •Опыт 5. Электролиз раствора иодида калия.
- •Опыт 6. Электролиз раствора хлорида олова.
- •Опыт 7. Электролиз раствора сульфата меди.
- •Опыт 8. Электролиз раствора сульфата меди с активным (медным) анодом.
- •Работа № 10 получение комплексных соединений, изучение их свойств и методов разрушения
- •Опыт 1. Зависимость окраски аквакомплексов от типа комплексообразователя
- •Опыт 2. Зависимость окраски комплексов кобальта от типа лигандов
- •Опыт з. Ступенчатая диссоциация бромидных комплексов меди(II)
- •Получение комплексных соединений. Написание уравнений комплексообразования. Названия.
- •Опыт 4. Получение аммиаката никеля
- •Опыт 6. Получение соединения, содержащего комплексные катион и анион
- •Опыт 7. Влияние природы d–элемента на комплексообразование
- •Устойчивость комплексных соединений
- •Константы нестойкости некоторых комплексных ионов
- •Опыт 8. Влияние концентрации раствора на устойчивость комплексных соединений
- •Опыт 9. Сравнительная устойчивость хлоридных комплексов цинка и кобальта
- •Опыт 10. Сравнительная устойчивость роданидного и фторидного комплексов железа
- •Опыт 11. Разрушение комплексов
- •При сдаче лабораторной работы ответить на следующие вопросы
- •Плотность водных растворов k2Cr2o7
- •Константы диссоциации воды и некоторых слабых кислот и оснований в водных растворах при 18 c
- •Области перехода некоторых индикаторов
- •Степень гидролиза солей (в 0,1 м растворах при 25c)
- •Константы нестойкости некоторых комплексных ионов
- •Растворимость некоторых солей и оснований в воде
- •Приборы и реактивы
- •Содержание
Опыт 11. Качественные реакции на хлорид-, сульфат- и фосфат-ионы
Выполнение опыта. В три пробирки поместить по 5 капель 0.1н растворов хлорида, фосфата и сульфата натрия. В первую и вторую пробирки добавить по каплям раствор нитрата серебра, в третью – хлорида бария до выпадения осадков. Отметить цвета осадков. Результаты наблюдений внести в таблицу:
|
Исходные вещества |
Окраска |
Реагенты |
Продукты реакции |
Окраска |
|
NaCl |
|
AgNO3 |
|
|
|
Na3PO4 |
|
AgNO3 |
|
|
|
Na2SO4 |
|
BaCl2 |
|
|
Написать уравнения соответствующих реакций в молекулярном и ионном виде. Назвать полученные соединения.
Опыт 12. Исследование окраски некоторых катионов и анионов
Выполнение опыта. Найти в штативах пробирки с растворами солей никеля, кобальта, меди, марганца (II), железа (III), хрома (III), хромата калия K2CrO4, бихромата калия K2Cr2O7, перманганата калия KMnO4. Записать формулы солей и соответствующую им окраску.
Опыт 13. Качественное определение катионов Zn2+,Cd2+,Fe3+,Pb2+,Hg2+,Cr3+,Cu2+
Выполнение опыта. В cемь пробирок поместить по 5 капель 0.1н растворов растворимых солей цинка, кадмия, железа (III), свинца, ртути, хрома(III), меди. Отметить окраску исходных растворов. В первую и вторую пробирки добавить по каплям раствор сульфида натрия до выпадения осадков, в третью – роданида калия, в четвертую и пятую раствор иодида калия до выпадения осадков, в шестую и седьмую – избыток раствора щелочи. Отметить цвета осадков и изменение цвета растворов. Написать уравнения соответствующих реакций в молекулярном и ионном виде. Назвать полученные соединения. Результаты опыта внести в таблицу:
|
Ион соли |
Окраска |
Реагент |
Признаки реакции |
Уравнения реакций | |
|
окраска | |||||
|
осадка |
раствора | ||||
|
Zn 2+ |
|
Na2S |
|
|
|
|
Cd2+ |
|
Na2S |
|
|
|
|
Fe3+ |
|
KCNS |
|
|
|
|
Pb2+ |
|
KI |
|
|
|
|
Hg2+ |
|
KI |
|
|
|
|
Cr3+ |
|
NaOH |
|
|
|
|
Cu2+ |
|
NaOH |
|
|
|
Контрольные задания
Задание 1. Получить у преподавателя две пробирки с растворами солей цинка и кадмия. Имея в своем распоряжении только раствор щелочи, определить, в какой из пробирок находится соль цинка. Написать соответствующие уравнения реакций.
Задание 2. Получить у преподавателя две пробирки с растворами солей хрома и цинка. Имея в своем распоряжении только раствор щелочи, определить, в какой из пробирок находится соль цинка. Написать соответствующие уравнения реакций.
Задание 3. Получить у преподавателя две пробирки с растворами солей хрома и кадмия. Имея в своем распоряжении только раствор щелочи, определить, в какой из пробирок находится соль хрома. Написать соответствующие уравнения реакций.
Задание 4. Получить у преподавателя две пробирки с растворами солей хрома и железа. Имея в своем распоряжении только раствор щелочи, определить, в какой из пробирок находится соль железа. Написать соответствующие уравнения реакций.
Задание 5. Получить у преподавателя две пробирки с растворами солей меди и свинца. Имея в своем распоряжении только раствор щелочи, определить, в какой из пробирок находится соль меди. Написать соответствующие уравнения реакций.
Задание 6. Получить у преподавателя две пробирки с растворами солей ртути и цинка. Имея в своем распоряжении только раствор иодида калия, определить, в какой из пробирок находится соль ртути. Написать соответствующие уравнения реакций.
Задание 7. Получить у преподавателя три пробирки с растворами солей кадмия, железа и цинка. Определить, в какой из пробирок находится соль цинка. Написать соответствующие уравнения реакций.
Задание 8. Получить у преподавателя две пробирки с растворами солей хрома и ртути. Имея в своем распоряжении только раствор щелочи определить, в какой из пробирок находится соль хрома. Написать соответствующие уравнения реакций.
Задание 9. Получить у преподавателя две пробирки с растворами солей кадмия и свинца. Определить, в какой из пробирок находится соль кадмия. Написать соответствующие уравнения реакций.
Задание 10. Получить у преподавателя две пробирки с растворами хлорида и сульфата натрия. Определить, в какой из пробирок находится сульфат натрия. Написать соответствующие уравнения реакций.
Задание 11. Получить у преподавателя две пробирки с растворами сульфата и фосфата натрия. Определить, в какой из пробирок находится фосфат натрия. Написать соответствующие уравнения реакций.
При сдаче лабораторной работы ответить на следующие вопросы
1. Назовите основные классы неорганических веществ.
2. Как классифицируются оксиды? Дайте характеристику оксидов неметаллов и металлов в различных степенях окисления.
3. Напишите уравнения следующих реакций:
-
а) SiO2 + CaO

г) ZnO + SiO2

б) Al2O3 + P2O5

д) ZnO + NaOH
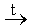
в) Al2O3 + KOH

е) CaO + CO2 →
4. Напишите формулы и названия кислот, соответствующих следующим оксидам:
SO2, CO2, SiO2, B2O3, P2O3, N2O5, P2O5, SO3, Cl2O7, NO2, Mn2O7, GeO2.
5. Напишите уравнения диссоциации следующих оснований:
NaOH, Ca(OH)2, Ba(OH)2, Fe(OH)3, Ni(OH)2.
Назовите основания и соответствующие им основные остатки.
6. Напишите уравнения реакций, доказывающих амфотерность следующих оксидов и гидроксидов:
1) Zn(OH)2, 2) Al2O3, 3) GeO, 4) Sn(OH)4, 5) GeO2.
7. Напишите в молекулярном и ионном видах уравнения следующих реакций:

8. Укажите, какие из следующих реакций невозможны:

Напишите уравнения возможных реакций в ионном и молекулярном видах. Назовите образующиеся соединения.
9. Укажите, какие из приведенных солей относятся к: а) средним;
б) основным; в) кислым:
![]() Назовите
эти соли, напишите уравнения их диссоциации
и соответствующие им условно-структурные
формулы.
Назовите
эти соли, напишите уравнения их диссоциации
и соответствующие им условно-структурные
формулы.
10. Укажите, какие типы солей можно получить при взаимодействии следующих гидроксидов:

Напишите уравнения реакций и назовите соли.
11. Назовите следующие соли и напишите уравнения их диссоциации:
![]()
12. Назовите следующие соединения и напишите их условно–структурные формулы:
![]()
13. Составьте уравнения реакций, с помощью которых можно осуществить указанные превращения:
![]()
![]()
![]()
![]()
