
- •Введение
- •Раздел первый
- •1.2. Определение химии
- •1.3. Атомно-молекулярное учение
- •1.4. Основные стехиометрические законы химии
- •1.5. Значение химии в развитии техники
- •Глава 2. Строение атомов. Периодический закон и периодическая система химических элементов д.И. Менделеева
- •2.1. Первые модели строения атома
- •2.2. Квантово-механическая модель атома водорода
- •2.3. Квантовые числа
- •2.4. Атомные орбитали
- •2.5. Многоэлектронные атомы
- •2.6. Распределение электронов по энергетическим уровням и подуровням у элементов малых периодов
- •2.7. Распределение электронов по энергетическим уровням и подуровням у элементов больших периодов
- •2.8. Периодический закон д. И. Менделеева
- •2.9. Структура периодической системы химических элементов д. И. Менделеева
- •2.10. Свойства атомов элементов в периодической системе
- •2.11. Закономерности изменения свойств элементов и их соединений в периодической системе
- •Глава 3. Химическая связь и строение молекул
- •3.1. Развитие теории химической связи
- •3.2. Ковалентная связь. Кривая потенциальной энергии
- •3.3. Основные количественные характеристики ковалентной связи
- •3.4. Квантово – механическая теория валентности
- •3.5. Донорно – акцепторный механизм образования ковалентной связи
- •3.6. Свойства ковалентной связи
- •3.7. Метод молекулярных орбиталей
- •3.8. Ионная связь
- •3.9. Водородная связь
- •3.10. Межмолекулярное взаимодействие
- •Глава 4. Кристаллическое состояние вещества
- •4.1. Макроскопические свойства кристаллов
- •4.2. Внутреннее строение кристаллов
- •4.3. Виды элементарных ячеек
- •4.4. Металлическая связь
- •4.5. Реальные кристаллы и нарушения кристаллической структуры
- •Раздел второй
- •5.2. Первый закон термодинамики
- •5.3. Энтальпия образования химических соединений
- •5.4. Энтропия. Второй закон термодинамики
- •5.5. Третий закон термодинамики
- •5.6. Энергия Гиббса. Направленность химических реакций
- •164,9 КДж; 172,41 Дж/моль∙к;
- •Глава 6. Скорость химических реакций. Химическое равновесие
- •6.1. Влияние внешних факторов на скорость химических реакций
- •6.2. Химическое равновесие
- •6.3. Цепные реакции
- •6.4. Фазовые равновесия
- •6.5. Катализаторы и каталитические системы
- •Раздел третий растворы
- •Глава 7. Общие свойства растворов
- •7.1. Механизм процессов растворения
- •7.2. Способы выражения количественного состава растворов
- •100 ∙ 10,91 Моль % h2so4
- •7.3. Энергетика растворения
- •7.4. Свойства растворов неэлектролитов
- •7.5. Свойства растворов электролитов
- •7.6. Электролитическая диссоциация воды. Водородный показатель
- •7.7. Произведение растворимости. Гидролиз солей
- •Глава 8. Окислительно-восстановительные реакции
- •8.1.Общие понятия об окислительно- восстановительных реакциях
- •8.2. Классификация окислителей и восстановителей
- •8.3. Количественная характеристика окислительно-восстановительных реакций
- •8.4. Методы составления уравнения окислительно-восстановительных реакций
- •8.5. Влияние факторов на характер и направление реакций
- •8.6. Типы окислительно-восстановительных реакций
- •Глава 9. Электрохимические процессы
- •9.1. Строение двойного электрического слоя
- •9.2. Гальванические элементы
- •9.3. Стандартный водородный электрод
- •9.4. Поляризационные явления в гальванических элементах
- •9.5. Химические источники тока
- •9.6. Аккумуляторы
- •9.7. Топливные элементы
- •9.8. Теоретические основы электролиза
- •9.9. Последовательность электродных процессов
- •9.10. Техническое применение электролиза
- •Глава 10. Коррозия и защита металлов
- •10.1. Общие сведения о коррозии
- •10.2. Классификация коррозионных процессов
- •10.3. Количественная и качественная оценка коррозии и коррозионной стойкости
- •10.4. Химическая коррозия
- •10.5. Электрохимическая коррозия
- •10.6. Методы защиты от электрохимической коррозии
- •Раздел четвертый
- •11.2. Электропроводность металлов, полупроводников и диэлектриков
- •11.3. Химические свойства металлов высокой проводимости
- •11.4. Электропроводимость металлов подгруппы меди
- •11.5. Химические свойства магнитных материалов
- •11.6. Магнитные свойства металлов семейства железа
- •Глава 12. Химическая идентификация и анализ вещества
- •12.1. Химическая идентификация вещества
- •12.2. Количественный анализ
- •12.3. Инструментальные методы анализа
- •Заключение
- •Библиографический список
- •Глава 1. Основные понятия химии. Предмет и задачи
- •Глава 2. Строение атомов. Периодический закон и
- •Глава 3. Химическая связь и строение молекул………..54
- •Глава 4. Кристаллическое состояние вещества………..103
- •Глава 12. Химическая идентификация и анализ
2.3. Квантовые числа
Волновая функция, являющаяся решением уравнения Шредингера, называется орбиталью. Для решения этого уравнения вводятся три квантовых числа (n, l и ml )
Главное квантовое число n. оно определяет энергию электрона и размеры электронных облаков. Энергия электрона главным образом зависит от расстояния электрона от ядра: чем ближе к ядру находится электрон, тем меньше его энергия. Поэтому можно сказать, что главное квантовое число n определя-
ет расположение электрона на том или ином энергетическом уровне. Главное квантовое число имеет значения ряда целых чисел от 1 до ∞. При значении главного квантового числа, равного 1 (n = 1), электрон находится на первом энергетическом уровне, расположенном на минимально возможном расстоянии от ядра. Общая энергия такого электрона наименьшая.
Электрон, находящийся на наиболее удаленном от ядра энергетическом уровне, обладает максимальной энергий. Поэтому при переходе электрона с более удаленного энергетического уровня на более близкий выделяется энергия. Энергетические уровни обозначают прописными буквами согласно схеме:
Значение n …. 1 2 3 4 5
Обозначение K L M N Q
Орбитальное квантовое число l. Согласно квантово-механическим расчетам электронные облака отличаются не только размерами, но и формой. Форму электронного облака характеризует орбитальное или побочное квантовое число. Различная форма электронных облаков обусловливает изменение энергии электрона в пределах одного энергетического уровня, т.е. ее расщепления на энергетические подуровни. Каждой форме электронного облака соответствует определенное значение механического момента движения электрона , определяемого орбитальным квантовым числом:
![]()
![]()
Определенной форме электронного облака соответствует вполне определенное значение орбитального момента количества движения электрона . Так как может принимать только дискретные значения, задаваемые квантовым числом l, то и формы электронных облаков не могут быть произвольными: каждому возможному значению l соответствует вполне определенная форма электронного облака.
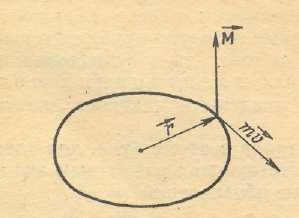
Рис.
5. Графическая интерпретация момента
движения электрона, где![]() μ
- орбитальный момент количества
μ
- орбитальный момент количества
движения электрона
Орбитальное квантовое число может иметь значения от 0 до n - 1, всего n – значений.
Энергетические подуровни обозначены буквами:
Значение l 0 1 2 3 4
Обозначение s p d f g
Магнитное квантовое число ml. Из решения уравнения Шредингера следует, что электронные облака ориентированы определенным образом в пространстве. Пространственная ориентация электронных облаков характеризуется магнитным квантовым числом.
Магнитное квантовое число может принимать любые целочисленные значения как положительные, так и отрицательные в пределах от –l до +l, а всего это число может принимать (2l+1) значений для данного l, включая нулевое. Например, если l = 1, то возможны три значения m (–1,0,+1) орбитальный момент , есть вектор, величина которого квантована и определяется значением l. Из уравнения Шредингера следует, что не только величина µ, но и направление этого вектора, характеризующее пространственную ориентацию электронного облака, квантовано. Каждому направлению вектора заданной
длины соответствует определенное значение его проекции на ось z, характеризующее некоторое направление внешнего магнитного поля. Значение этой проекции характеризует ml.
Спин электрона. Изучение атомных спектров показало, что три квантовых числа n, l и ml не являются полной характеристикой поведения электронов в атомах. С развитием спектральных методов исследований и повышением разрешающей способности спектральных приборов была обнаружена тонкая структура спектров. Оказалось, что линии спектров расщепляются. Для объяснения этого явления было введено четвертое квантовое число, связанное с поведением самого электрона. Это квантовое число было названо спином с обозначением ms и принимающее всего два значения +½ и –½ в зависимости от одной из двух возможных ориентаций спина электрона в магнитном поле. Положительное и отрицательное значения спина связаны с его направлением. Поскольку спин величина векторная, то его условно обозначают стрелкой, направленной вверх или ↑ или вниз ↓ .Электроны, имеющие одинаковое направление спина называются параллельными, при противоположных значениях спинов – антипараллельныи.
Наличие спина у электрона было доказано экспериментально в 1921 г., В. Герлахом и О. Штерном, которые сумели разделить пучок атомов водорода на две части, соответствующие ориентации электронного спина. Схема их эксперимента показана на рис. 6. Когда атомы водорода пролетают через область сильного магнитного поля, электрон каждого атома взаимодействует с магнитным полем, и это заставляет атом отклоняться от исходной прямолинейной траектории, Направление, в котором отклоняется атом, зависит от ориентации спина его электрона. Спин у электрона не зависит от внешних условий и не может быть уничтожен или изменен.
Таким образом, было окончательно установлено, что полностью состояние электрона в атоме характеризуется четырьмя квантовыми числами n, l, ml. и ms,
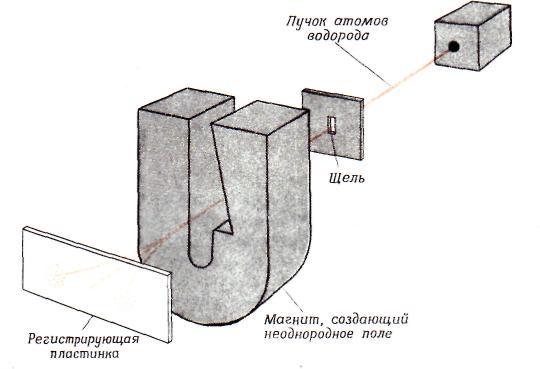
Рис. 6. Схема эксперимента Штерна - Герлаха
