
- •Введение
- •Раздел первый
- •1.2. Определение химии
- •1.3. Атомно-молекулярное учение
- •1.4. Основные стехиометрические законы химии
- •1.5. Значение химии в развитии техники
- •Глава 2. Строение атомов. Периодический закон и периодическая система химических элементов д.И. Менделеева
- •2.1. Первые модели строения атома
- •2.2. Квантово-механическая модель атома водорода
- •2.3. Квантовые числа
- •2.4. Атомные орбитали
- •2.5. Многоэлектронные атомы
- •2.6. Распределение электронов по энергетическим уровням и подуровням у элементов малых периодов
- •2.7. Распределение электронов по энергетическим уровням и подуровням у элементов больших периодов
- •2.8. Периодический закон д. И. Менделеева
- •2.9. Структура периодической системы химических элементов д. И. Менделеева
- •2.10. Свойства атомов элементов в периодической системе
- •2.11. Закономерности изменения свойств элементов и их соединений в периодической системе
- •Глава 3. Химическая связь и строение молекул
- •3.1. Развитие теории химической связи
- •3.2. Ковалентная связь. Кривая потенциальной энергии
- •3.3. Основные количественные характеристики ковалентной связи
- •3.4. Квантово – механическая теория валентности
- •3.5. Донорно – акцепторный механизм образования ковалентной связи
- •3.6. Свойства ковалентной связи
- •3.7. Метод молекулярных орбиталей
- •3.8. Ионная связь
- •3.9. Водородная связь
- •3.10. Межмолекулярное взаимодействие
- •Глава 4. Кристаллическое состояние вещества
- •4.1. Макроскопические свойства кристаллов
- •4.2. Внутреннее строение кристаллов
- •4.3. Виды элементарных ячеек
- •4.4. Металлическая связь
- •4.5. Реальные кристаллы и нарушения кристаллической структуры
- •Раздел второй
- •5.2. Первый закон термодинамики
- •5.3. Энтальпия образования химических соединений
- •5.4. Энтропия. Второй закон термодинамики
- •5.5. Третий закон термодинамики
- •5.6. Энергия Гиббса. Направленность химических реакций
- •164,9 КДж; 172,41 Дж/моль∙к;
- •Глава 6. Скорость химических реакций. Химическое равновесие
- •6.1. Влияние внешних факторов на скорость химических реакций
- •6.2. Химическое равновесие
- •6.3. Цепные реакции
- •6.4. Фазовые равновесия
- •6.5. Катализаторы и каталитические системы
- •Раздел третий растворы
- •Глава 7. Общие свойства растворов
- •7.1. Механизм процессов растворения
- •7.2. Способы выражения количественного состава растворов
- •100 ∙ 10,91 Моль % h2so4
- •7.3. Энергетика растворения
- •7.4. Свойства растворов неэлектролитов
- •7.5. Свойства растворов электролитов
- •7.6. Электролитическая диссоциация воды. Водородный показатель
- •7.7. Произведение растворимости. Гидролиз солей
- •Глава 8. Окислительно-восстановительные реакции
- •8.1.Общие понятия об окислительно- восстановительных реакциях
- •8.2. Классификация окислителей и восстановителей
- •8.3. Количественная характеристика окислительно-восстановительных реакций
- •8.4. Методы составления уравнения окислительно-восстановительных реакций
- •8.5. Влияние факторов на характер и направление реакций
- •8.6. Типы окислительно-восстановительных реакций
- •Глава 9. Электрохимические процессы
- •9.1. Строение двойного электрического слоя
- •9.2. Гальванические элементы
- •9.3. Стандартный водородный электрод
- •9.4. Поляризационные явления в гальванических элементах
- •9.5. Химические источники тока
- •9.6. Аккумуляторы
- •9.7. Топливные элементы
- •9.8. Теоретические основы электролиза
- •9.9. Последовательность электродных процессов
- •9.10. Техническое применение электролиза
- •Глава 10. Коррозия и защита металлов
- •10.1. Общие сведения о коррозии
- •10.2. Классификация коррозионных процессов
- •10.3. Количественная и качественная оценка коррозии и коррозионной стойкости
- •10.4. Химическая коррозия
- •10.5. Электрохимическая коррозия
- •10.6. Методы защиты от электрохимической коррозии
- •Раздел четвертый
- •11.2. Электропроводность металлов, полупроводников и диэлектриков
- •11.3. Химические свойства металлов высокой проводимости
- •11.4. Электропроводимость металлов подгруппы меди
- •11.5. Химические свойства магнитных материалов
- •11.6. Магнитные свойства металлов семейства железа
- •Глава 12. Химическая идентификация и анализ вещества
- •12.1. Химическая идентификация вещества
- •12.2. Количественный анализ
- •12.3. Инструментальные методы анализа
- •Заключение
- •Библиографический список
- •Глава 1. Основные понятия химии. Предмет и задачи
- •Глава 2. Строение атомов. Периодический закон и
- •Глава 3. Химическая связь и строение молекул………..54
- •Глава 4. Кристаллическое состояние вещества………..103
- •Глава 12. Химическая идентификация и анализ
10.6. Методы защиты от электрохимической коррозии
Коррозию металлов можно затормозить изменением потенциала металла, пассивированием металла, снижением концентрации окислителя, изменением состава металла и др. При разработке методов защиты от коррозии используют указанные способы снижения скорости коррозии, которые меняются в зависимости от характера коррозии и условий ее протекания. Выбор способа определяется его эффективностью, а также экономической целесообразностью. Все методы защиты условно делятся на следующие группы: а) легирование металлов;
б) защитные покрытия (металлические, неметаллические), электро - химическая защита; в) изменение свойств коррозионной среды; г) рациональное конструирование изделий.
Легирование металлов- эффективный (хотя и дорогой) метод повышения коррозионной стойкости металлов. При легировании в состав сплава вводят компоненты, вызывающие пассивацию металла. В качестве таких компонентов применяют хром, никель, вольфрам и др. Широкое применение нашло легирование для защиты от газовой коррозии. При этом используют сплавы, обладающие жаростойкостью и жаропрочностью.
Защитные покрытия- это слои, искусственно создаваемые на поверхности металлических изделий и сооружений для предохранения их от коррозии. Материалы для металлических защитных покрытий могут быть как чистые металлы (цинк, кадмий, алюминий, никель, медь, хром, серебро и др.), так и их сплавы (бронза, латунь и др.). По характеру поведения металлических покрытий при коррозии их можно разделить на катодные и анодные. К катодным покрытиям относятся покрытия, потенциалы которых в данной среде имеют более положительное значение, чем потенциал основного металла. В качестве примера катодных покрытий на стали можно привестиСu,Ni,Ag. При повреждении покрытия (или наличие пор) возникает коррозионный элемент, в котором основной материал в поре служит анодом и растворяется, а материал покрытия - катодом, на котором выделяется водород или поглощается кислород (рис. 71).
Следовательно, катодные покрытия могут защищать металл от коррозии лишь при отсутствии пор и повреждений покрытия. Анодные покрытия имеют более отрицательный потенциал, чем потенциал основного металла. Примером анодного покрытия сможет служить цинк на стали. В этом случае основной металл будет катодом коррозионного элемента, поэтому он не корродирует (рис. 72).
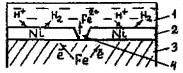
Рис. 71. Схема коррозии металла в кислом растворе при
нарушении катодного покрытия: 1- раствор,2- покрытие,
3- основной металл,4– пора.
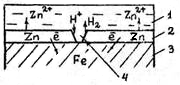
Рис. 72. Схема коррозии металла в кислом растворе при
нарушении анодного покрытия: 1- раствор,2- покрытие,
3- основной металл,4- пора
Потенциалы металлов зависят от состава растворов, поэтому при изменении состава раствора может меняться и характер покрытия. Так, покрытие стали оловом в растворе Н2SO4- катодное, а в растворе органических кислот – анодное.
Для получения
металлических защитных покрытий
применяются различные
способы: электрохимический (гальванические
покрытия), погружение в расплавленный
металл, металлизация термодиффузионная
и химическая.
Электрохимическаязащита основана на торможении анодных или катодных реакций коррозионного процесса. Электрохимическая защита осуществляется присоединением к защищаемой конструкции металла с более отрицательным значением электродного потенциала - протектора, а также катодной или анодной поляризацией за счет извне приложенного тока.
Защита от коррозии с использованием протектора называется протекторной. Она осуществляется следующим способом: защищаемое изделие (например,Fe) соединяется металлическим проводником с более активным металлом (например,Zn). Возникает гальванический элемент, гдеZnявляется анодом, растворяется,Fe- оказывается защищенным (катод).
Сущность катодной защиты заключается в том, что защищаемое изделие подключается к отрицательному полюсу внешнего источника тока, поэтому оно становится катодом, а анодом служит вспомогательный, обычно стальной электрод. Вспомогательный электрод растворяется на защищаемом сооружении (катоде) выделяется водород.
При анодной защите защищаемое изделие присоединяется к аноду внешнего источника тока. Подбирают определенную плотность тока, чтобы металл не растворялся, а на аноде в результате электролиза выделялся кислород. Защищаемый металл покрывается оксидной пленкой. анодная защита применяется к легкопассивирующим металлам (Al,Mg,Cr, и др.).
Эффективным способом защиты от коррозии является применение неметаллических покрытий. К этим покрытиям относятся:
а) Оксидные пленки. Нанесение оксидных пленок осуществляется электрохимическим и химическим путем.
б) Труднорастворимые химические пленки. Широко применим процесс форфатирования. На поверхности изделия создается фосфатная пленка, обладающая не только коррозионной устойчивостью, но и высокими электроизоляционными свойствами.
в) К неметаллическим покрытиям относятся всевозможные эмали, смазки, лаки, краски, высокомолекулярные соединения.
Для снижения скорости коррозии часто изменяют свойства коррозионной среды. Агрессивность среды снижают уменьшением концентрации опасных в коррозионном отноше-
нии компонентов, а также снижением концентрации ионов водорода. Для защиты от коррозии широко применяют ингибиторы коррозии- вещества, при добавлении которых в агрессивную среду, значительно уменьшается скорость коррозии металлов. Различают анодные и катодные ингибиторы. К анодным ингибиторам относятся те, которые замедляют действие коррозии, например, нитрит натрияNaNO2, дихромат натрияNa2Cr2O7. Их действие сводится к образованию пленки труднорастворимого соединения, либо к окислению поверхности металла, либо к адсорбции на поверхности металла.
Катодные замедлители уменьшают скорость коррозии за счёт снижения интенсивности катодного процесса или к сокращению площади катодных участков. К катодным ингибиторам относятся органические вещества, содержащие азот, серу и кислород, например, диэтиламин, уротропин, формальдегид и др.
Рациональное конструирование изделий должно исключать наличие или сокращать число и размеры особо коррозионноопасных участков в изделиях или конструкциях, а также предусматривать специальную защиту металла этих участков от коррозии.
