
- •Введение
- •Раздел первый
- •1.2. Определение химии
- •1.3. Атомно-молекулярное учение
- •1.4. Основные стехиометрические законы химии
- •1.5. Значение химии в развитии техники
- •Глава 2. Строение атомов. Периодический закон и периодическая система химических элементов д.И. Менделеева
- •2.1. Первые модели строения атома
- •2.2. Квантово-механическая модель атома водорода
- •2.3. Квантовые числа
- •2.4. Атомные орбитали
- •2.5. Многоэлектронные атомы
- •2.6. Распределение электронов по энергетическим уровням и подуровням у элементов малых периодов
- •2.7. Распределение электронов по энергетическим уровням и подуровням у элементов больших периодов
- •2.8. Периодический закон д. И. Менделеева
- •2.9. Структура периодической системы химических элементов д. И. Менделеева
- •2.10. Свойства атомов элементов в периодической системе
- •2.11. Закономерности изменения свойств элементов и их соединений в периодической системе
- •Глава 3. Химическая связь и строение молекул
- •3.1. Развитие теории химической связи
- •3.2. Ковалентная связь. Кривая потенциальной энергии
- •3.3. Основные количественные характеристики ковалентной связи
- •3.4. Квантово – механическая теория валентности
- •3.5. Донорно – акцепторный механизм образования ковалентной связи
- •3.6. Свойства ковалентной связи
- •3.7. Метод молекулярных орбиталей
- •3.8. Ионная связь
- •3.9. Водородная связь
- •3.10. Межмолекулярное взаимодействие
- •Глава 4. Кристаллическое состояние вещества
- •4.1. Макроскопические свойства кристаллов
- •4.2. Внутреннее строение кристаллов
- •4.3. Виды элементарных ячеек
- •4.4. Металлическая связь
- •4.5. Реальные кристаллы и нарушения кристаллической структуры
- •Раздел второй
- •5.2. Первый закон термодинамики
- •5.3. Энтальпия образования химических соединений
- •5.4. Энтропия. Второй закон термодинамики
- •5.5. Третий закон термодинамики
- •5.6. Энергия Гиббса. Направленность химических реакций
- •164,9 КДж; 172,41 Дж/моль∙к;
- •Глава 6. Скорость химических реакций. Химическое равновесие
- •6.1. Влияние внешних факторов на скорость химических реакций
- •6.2. Химическое равновесие
- •6.3. Цепные реакции
- •6.4. Фазовые равновесия
- •6.5. Катализаторы и каталитические системы
- •Раздел третий растворы
- •Глава 7. Общие свойства растворов
- •7.1. Механизм процессов растворения
- •7.2. Способы выражения количественного состава растворов
- •100 ∙ 10,91 Моль % h2so4
- •7.3. Энергетика растворения
- •7.4. Свойства растворов неэлектролитов
- •7.5. Свойства растворов электролитов
- •7.6. Электролитическая диссоциация воды. Водородный показатель
- •7.7. Произведение растворимости. Гидролиз солей
- •Глава 8. Окислительно-восстановительные реакции
- •8.1.Общие понятия об окислительно- восстановительных реакциях
- •8.2. Классификация окислителей и восстановителей
- •8.3. Количественная характеристика окислительно-восстановительных реакций
- •8.4. Методы составления уравнения окислительно-восстановительных реакций
- •8.5. Влияние факторов на характер и направление реакций
- •8.6. Типы окислительно-восстановительных реакций
- •Глава 9. Электрохимические процессы
- •9.1. Строение двойного электрического слоя
- •9.2. Гальванические элементы
- •9.3. Стандартный водородный электрод
- •9.4. Поляризационные явления в гальванических элементах
- •9.5. Химические источники тока
- •9.6. Аккумуляторы
- •9.7. Топливные элементы
- •9.8. Теоретические основы электролиза
- •9.9. Последовательность электродных процессов
- •9.10. Техническое применение электролиза
- •Глава 10. Коррозия и защита металлов
- •10.1. Общие сведения о коррозии
- •10.2. Классификация коррозионных процессов
- •10.3. Количественная и качественная оценка коррозии и коррозионной стойкости
- •10.4. Химическая коррозия
- •10.5. Электрохимическая коррозия
- •10.6. Методы защиты от электрохимической коррозии
- •Раздел четвертый
- •11.2. Электропроводность металлов, полупроводников и диэлектриков
- •11.3. Химические свойства металлов высокой проводимости
- •11.4. Электропроводимость металлов подгруппы меди
- •11.5. Химические свойства магнитных материалов
- •11.6. Магнитные свойства металлов семейства железа
- •Глава 12. Химическая идентификация и анализ вещества
- •12.1. Химическая идентификация вещества
- •12.2. Количественный анализ
- •12.3. Инструментальные методы анализа
- •Заключение
- •Библиографический список
- •Глава 1. Основные понятия химии. Предмет и задачи
- •Глава 2. Строение атомов. Периодический закон и
- •Глава 3. Химическая связь и строение молекул………..54
- •Глава 4. Кристаллическое состояние вещества………..103
- •Глава 12. Химическая идентификация и анализ
4.2. Внутреннее строение кристаллов
Связь между формой макро- или микрокристалла и его внутренним строением, определяемым распределением элементарных материальных частиц в пространстве, удалось установить после открытия рентгеновских лучей.
При прохождении через кристалл узкого параллельного пучкарентгеновских лучей наблюдаетсяих дифракция и интерференция(Лауэ, 1912). На регистрирующейфотопластинке кроме центрального пятна появляется большое количество пятен, расположение которых характерно для данного кристаллаи угла поворота его к направлению рентгеновского луча.
В 1913 г. У.Г. и У.Л. Брэгги предложили уравнение, связывающее расстояние между плоскостями в кристалле, вызывающими явление интерференции, длину волны рентгеновского луча и угол между направлением луча и плоскостью кристалла
![]() Ө,
Ө,
где λ - длина волны рентгеновского луча, d - расстояние между плоскостями, Ө - угол между лучом и плоскостью или угол скольжения, п - целое число (условие усиления лучей).
Длина волны рентгеновского луча зависит, как известно, от материала антикатода.
Восстановив по фигурам интерференционных пятен расположение в пространстве частиц, вызвавших дифракцию, можно сделать вывод о внутреннем строении кристалла.
Таким образом, внутреннее строение кристаллов представляется как система атомов, определенным образом расположенных в пространстве, - кристаллическая решетка.
Элемент кристаллической решетки или элементарная ячейка - геометрическая фигура, образованная материальными частицами, расположенными определенным образом в пространстве, мысленно выделенная из общего тела кристалла.
Последнее добавление в формулировке необходимо потому, что кристаллическая решетка не представляет собой сумму изолированных кристаллических ячеек (например, кубов), а каждая частица, входящая в данную ячейку, одновременно принадлежит и окружающим ее кристаллическим элементам.
Оказалось, что число форм кристаллических ячеек меньше, чем форм макрокристаллов, так как скорость распространения этих ячеек по осям симметрии может быть различной, что и приводит к построению различных по форме макрокристаллов. Плоская грань кристалла может представлять собой ступенчатую поверхность, образованную слоями кристаллических ячеек, но она кажется нам идеально гладкой, так как высота этих ступенек измеряется ангстремами. Исходя из внутреннего строения кристалла, можно дать другое определение кристаллического тела: кристалл - часть пространства, заполненная параллельной трансляцией геометрического элемента, называемого элементарной ячейкой.
Рассмотрим
элементарную ячейку простого куба и
определим ее основные
характеристики.
Важнейшей характеристикой
куба
является величина его ребра а.
Однако
не всегда расстояние между
его плоскостями d,
заполненными
материальными частицами и
вызывающими дифракцию и интерференцию
рентгеновских лучей,
равно величине ребра: d
= a.
В
кубе можно провести
несколько плоскостей (рис. 32).
Их
индикация определяется числом
пересечений с осями координат: это
плоскости 100, 110 и 111. Если
рентгеновские лучи падают перпендикулярно
плоскости 100 (рис. 33, а),
то
они встретят 2 плоскости и расстояние
между плоскостями
будет равно d100;
если
они перпендикулярны плоскости110, то
d110
=
![]() так как плоскостей будет уже 3 и расстояниемежду
плоскостями равно половине диагонали
грани куба (рис. 33, б),
а
если лучи будут падать перпендикулярно
плоскости 111, то они встретят
уже 4 плоскости и расстояние между этими
плоскостями равноd 111 =
так как плоскостей будет уже 3 и расстояниемежду
плоскостями равно половине диагонали
грани куба (рис. 33, б),
а
если лучи будут падать перпендикулярно
плоскости 111, то они встретят
уже 4 плоскости и расстояние между этими
плоскостями равноd 111 =
![]() (рис.
33,в).
(рис.
33,в).
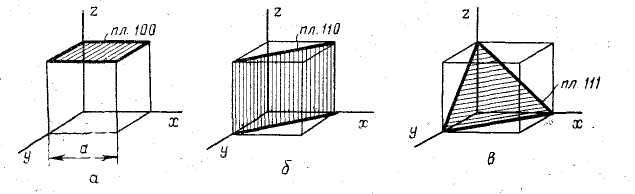
Рис. 32. Рентгенографические плоскости
в простой кубической решетке
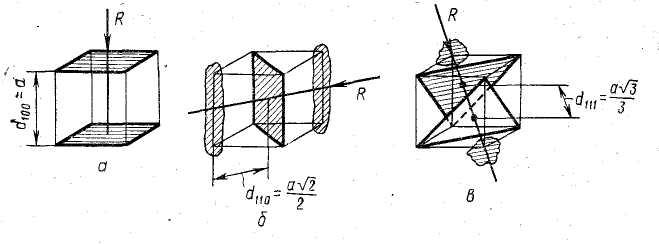
Рис. 33. Схема встречи рентгеновских лучей
с плоскостями в кристалле кубической системы
Отношение обратных величин d100, d110иd111является характеристикой для данного типа кристаллической решетки:
![]() :
:![]() :
:![]() =1:
=1:![]() :
:![]()
Это соотношение, постоянное для данной решетки, в конечном итоге определяет отношение расстояний на рентгенограмме кристалла (рис. 33).
Вторая важная характеристика любой элементарной ячейки - координационное число: координационным числомназывается число одинаковых частиц, расположенных на кратчайшем расстоянии от данной частицы (число ближайших соседей). Для простого куба на кратчайшем расстоянии от частицыАравнымарасположено 6 частиц, т.е. координационное числоK = 6.
Другой характеристикой элементарной ячейки является число частиц, необходимое для ее построения. каждая частица, находящаяся в вершине куба, принадлежит одновременно 8 кубам, сходящимся в одной точке(А), а, следовательно, на данный куб приходится только1/8ее часть. Вершин в кубе 8 и для построения данного куба требуется только одна частица:n = (1/8) 8 = 1.
Зная число частиц, необходимых для построения элемента кристаллической решетки, массу этих частиц и плотность кристалла, можно определить сторону куба, а, следовательно, и значения d, входящих в уравнение Брэггов, а это в свою очередь было необходимо для определения длины волныλрентгеновских лучей, получаемых от различных антикатодов. Если бы этого не было сделано, то Мозли не смог бы открыть свой закон.
В самом деле, зная систему кристаллической решетки и элементарной ячейки, число частиц, необходимое для построения, их массы и плотность кристалла, можно определить все геометрические размеры. Для кубических форм элементарных ячеек эта задача решается наиболее просто.
Если число частиц n, а масса ихA/N, гдеА- атомная масса, аN- число Авогадро, то масса элементарной ячейки будетm = nA/N. Объем элементарной ячейки выразим через плотность кристаллаρ, и он будет равен кубу стороны:
υ = (nA/ρN) = a3. Отсюда величина ребра куба
a=
![]()
Элементарный куб- типNaCl,n = l;K = 6, но так как в узлах элементарной ячейки находятся ионыNa+и ионыСl-, то это необходимо учесть:n = (l/8) 4Na++ (l/8) 4Cl- = (l/2) NaCl, т.е. требуется половина молекулы для построения ячейки
a
=
![]()
Плотность кристалла NaCl ρ = 2,164∙103 кг/см3;MNaCl = 58,5кг/кмоль; число АвогадроN = 6,02∙1026кмоль-1. Подставляем данные в уравнение и получаем
![]() =2,814
Ǻ
=2,814
Ǻ
Объемноцентрированный куб- типCsCl. В этом случаеК = 8; n = (1/8) 8+1 = 2. При построении ячейки также нужно учесть, что в узлах элементарной ячейки находятся ионыCs+иСl-. ТогдаCs+ + Cl- = CsClили уравнение для этого случая будет
а =
![]()
