
- •Введение
- •Раздел первый
- •1.2. Определение химии
- •1.3. Атомно-молекулярное учение
- •1.4. Основные стехиометрические законы химии
- •1.5. Значение химии в развитии техники
- •Глава 2. Строение атомов. Периодический закон и периодическая система химических элементов д.И. Менделеева
- •2.1. Первые модели строения атома
- •2.2. Квантово-механическая модель атома водорода
- •2.3. Квантовые числа
- •2.4. Атомные орбитали
- •2.5. Многоэлектронные атомы
- •2.6. Распределение электронов по энергетическим уровням и подуровням у элементов малых периодов
- •2.7. Распределение электронов по энергетическим уровням и подуровням у элементов больших периодов
- •2.8. Периодический закон д. И. Менделеева
- •2.9. Структура периодической системы химических элементов д. И. Менделеева
- •2.10. Свойства атомов элементов в периодической системе
- •2.11. Закономерности изменения свойств элементов и их соединений в периодической системе
- •Глава 3. Химическая связь и строение молекул
- •3.1. Развитие теории химической связи
- •3.2. Ковалентная связь. Кривая потенциальной энергии
- •3.3. Основные количественные характеристики ковалентной связи
- •3.4. Квантово – механическая теория валентности
- •3.5. Донорно – акцепторный механизм образования ковалентной связи
- •3.6. Свойства ковалентной связи
- •3.7. Метод молекулярных орбиталей
- •3.8. Ионная связь
- •3.9. Водородная связь
- •3.10. Межмолекулярное взаимодействие
- •Глава 4. Кристаллическое состояние вещества
- •4.1. Макроскопические свойства кристаллов
- •4.2. Внутреннее строение кристаллов
- •4.3. Виды элементарных ячеек
- •4.4. Металлическая связь
- •4.5. Реальные кристаллы и нарушения кристаллической структуры
- •Раздел второй
- •5.2. Первый закон термодинамики
- •5.3. Энтальпия образования химических соединений
- •5.4. Энтропия. Второй закон термодинамики
- •5.5. Третий закон термодинамики
- •5.6. Энергия Гиббса. Направленность химических реакций
- •164,9 КДж; 172,41 Дж/моль∙к;
- •Глава 6. Скорость химических реакций. Химическое равновесие
- •6.1. Влияние внешних факторов на скорость химических реакций
- •6.2. Химическое равновесие
- •6.3. Цепные реакции
- •6.4. Фазовые равновесия
- •6.5. Катализаторы и каталитические системы
- •Раздел третий растворы
- •Глава 7. Общие свойства растворов
- •7.1. Механизм процессов растворения
- •7.2. Способы выражения количественного состава растворов
- •100 ∙ 10,91 Моль % h2so4
- •7.3. Энергетика растворения
- •7.4. Свойства растворов неэлектролитов
- •7.5. Свойства растворов электролитов
- •7.6. Электролитическая диссоциация воды. Водородный показатель
- •7.7. Произведение растворимости. Гидролиз солей
- •Глава 8. Окислительно-восстановительные реакции
- •8.1.Общие понятия об окислительно- восстановительных реакциях
- •8.2. Классификация окислителей и восстановителей
- •8.3. Количественная характеристика окислительно-восстановительных реакций
- •8.4. Методы составления уравнения окислительно-восстановительных реакций
- •8.5. Влияние факторов на характер и направление реакций
- •8.6. Типы окислительно-восстановительных реакций
- •Глава 9. Электрохимические процессы
- •9.1. Строение двойного электрического слоя
- •9.2. Гальванические элементы
- •9.3. Стандартный водородный электрод
- •9.4. Поляризационные явления в гальванических элементах
- •9.5. Химические источники тока
- •9.6. Аккумуляторы
- •9.7. Топливные элементы
- •9.8. Теоретические основы электролиза
- •9.9. Последовательность электродных процессов
- •9.10. Техническое применение электролиза
- •Глава 10. Коррозия и защита металлов
- •10.1. Общие сведения о коррозии
- •10.2. Классификация коррозионных процессов
- •10.3. Количественная и качественная оценка коррозии и коррозионной стойкости
- •10.4. Химическая коррозия
- •10.5. Электрохимическая коррозия
- •10.6. Методы защиты от электрохимической коррозии
- •Раздел четвертый
- •11.2. Электропроводность металлов, полупроводников и диэлектриков
- •11.3. Химические свойства металлов высокой проводимости
- •11.4. Электропроводимость металлов подгруппы меди
- •11.5. Химические свойства магнитных материалов
- •11.6. Магнитные свойства металлов семейства железа
- •Глава 12. Химическая идентификация и анализ вещества
- •12.1. Химическая идентификация вещества
- •12.2. Количественный анализ
- •12.3. Инструментальные методы анализа
- •Заключение
- •Библиографический список
- •Глава 1. Основные понятия химии. Предмет и задачи
- •Глава 2. Строение атомов. Периодический закон и
- •Глава 3. Химическая связь и строение молекул………..54
- •Глава 4. Кристаллическое состояние вещества………..103
- •Глава 12. Химическая идентификация и анализ
Глава 9. Электрохимические процессы
Электрохимия изучает процессы, связанные с взаимным превращением химической и электрической энергии. Преобразование энергии химических реакций в электрическую осуществляются в устройствах, называемых химическими источниками тока или гальваническими элементами. Химические же превращения за счёт электрической энергии происходят в электролизёрах.
В устройствах обоих типов протекают окислительно-восстановительные процессы, называемые электрохимическими, особенностью которых является не хаотичность, а пространственная направленность электронных переходов.Процессы окисления и восстановления в этом случае пространственно разделены и проходят в двойном электрическом слое у электродов, соединенных металлическим проводником.
9.1. Строение двойного электрического слоя
Если в воду (или раствор электролита) погрузить пластинку какого-либо металла, то на его поверхности возникают процессы, приводящие к образованию так называемого двойного электрического слоя.
Ионы металла из его кристаллической решетки под влиянием полярных молекул воды отрываются и переходят в воду (или раствор). При этом поверхность металла заряжается отрицательно за счёт оставшихся в металле электронов, а слой воды заряжается положительно за счёт ионов, которые перешли в
раствор. В результате
на границе Ме- раствор устанавливается
равновесиеМе2+ (металл)
![]() Ме2+(раствор), т.к. по мере
увеличения заряда пластинки переход
катионов в одноимённо заряженный раствор
затрудняется. Если при установлении
контакта металл-раствор скорость
перехода катионов из металла в раствор
была меньше, чем скорость их перехода
в обратном
Ме2+(раствор), т.к. по мере
увеличения заряда пластинки переход
катионов в одноимённо заряженный раствор
затрудняется. Если при установлении
контакта металл-раствор скорость
перехода катионов из металла в раствор
была меньше, чем скорость их перехода
в обратном
направлении, то между электроном и раствором также устанавливается равновесие; но в этом случае электрод заряжается положительно, а раствор - отрицательно. Таким образом, происходит образование двойного электрического слоя, который может иметь различные заряды. Рассмотрим подробнее, от чего это зависит и как количественно можно охарактеризовать двойной электрический слой.
Электродные потенциалы.Заряд иона относительно велик, а электрическая ёмкость на границе между металлом и раствором мала, поэтому уже при переходе очень малого количества ионов между металлом и раствором возникает значительная разность потенциалов. Например, при переходе ионов серебра в количестве одной стомиллионной доли грамма(10-8 г)из раствора в металл его потенциал становится положительнее на0,5 В.
Таким образом, двойной электрический слой можно уподобить конденсатору, одна из обкладок которого представляет собой поверхность металла, а другая - слой ионов в растворе у поверхности металла. Между разноимённо заряженными обкладками и возникает разность, или скачок потенциала.
Различают три случаявозникновения скачка потенциала на границе металл - раствор электролита.
I. Ионы металла, находящиеся на поверхности обладают избыточной энергией по сравнению с энергией частиц, находящихся внутри металла. Взаимодействие полярных молекул воды с поверхностью металла приводит к отрыву катионов металла в виде гидратированных ионов
Ме + mН2О
![]() Меn+
(Н2О)m
+ n
Меn+
(Н2О)m
+ n![]()
В этом случае поверхность металла заряжается отрицательно (-), а слой электролита, примыкающий к ней - положительно(+). Образуется двойной слой с определённой разностью потенциалов.

 а
б
а
б
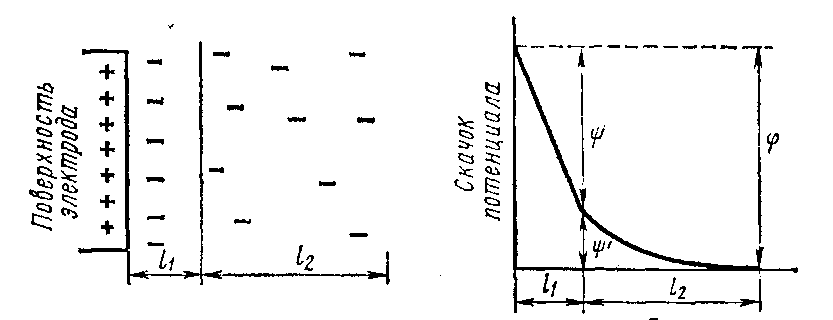
Рис. 59. Двойной электрический слой (а)и падение потенциал в нём(б);l1-адсорбционный слой;l2-диффузионный слой
Катионы распределяются
следующим образом: часть ионов плотно
прилегает к поверхности металла (ионы
находятся на расстояни радиуса иона),
образуя так называемый адсорбционный
слой (рис.59), а другая часть катионов под
влиянием сил молекулярного движения
распределяется на некотором расстоянии
от поверхности металла, образуя
диффузионный слой. Следовательно,
изменение потенциала
![]() в двойном электрическом слое слагается
из падения потенциала в адсорбционном
и диффузионном слое.
в двойном электрическом слое слагается
из падения потенциала в адсорбционном
и диффузионном слое.
![]() =
=
![]() +
+
![]() /
/
По мере увеличения концентрации катионов металла в растворе становится вероятным обратный процесс - восстановления ионов металла.
С течением времени скорость окисления металла становится равной скорости восстановления его ионов из раствора. На границе металл - раствор устанавливается равновесная разность потенциалов, которая называется равновесным электродным потенциалом(равновесный скачок потенциала).
Такая картина наблюдается для активных металлов. Это свидетельствует о том, что способность посылать ионы в раствор различных металлов выражена неодинаково. Она зависит от энергии ионизацииатомов металла, отэнергии гидратацииионов металла. Чем меньше энергия ионизации и больше энергия гидратации, тем выше способность металла окисляться и посылать свои ионы в раствор, при этом металл будет иметь и более отрицательный потенциал.
II.
Малоактивные металлы(Cu, Ag)окисляются с трудом, выход ионов в
раствор почти не происходит. Поэтому,
например, в случае медного электрода,
погруженного в раствор соли меди,
преобладает адсорбция ионов металла
на поверхности электрода. Схематично
процесс можно изобразить следующим
образом:[nCu] + x
Cu2+ ∙
(H2O)m
![]() [nCu]ּ
xּ
Cu2+
+ mH2O
[nCu]ּ
xּ
Cu2+
+ mH2O
В этом случае поверхность металла заряжается положительно, а прилегающий к ней раствор - отрицательно за счёт избытка в нём анионов (рис.60).
аб
Рис. 60. Двойной электрический слой (а)и падение потенциала
в нём (б): l1 - адсорбционный слой;l2 - диффузионный слой.
III. Иной механизм возникновения потенциала на инертном электроде, который опущен в раствор, содержащий окисленную или восстановленную форму какого - либо соединения. Например, если в растворFeCl3опустить платиновый (инертный) электрод, то катионFe3+отнимает от поверхности платины электрон и превращается в ионFe2+:
FeCl3 + ē → FeCl2 + Cl-
В результате
платина получает положительный заряд,
а раствор у поверхности её - отрицательный
заряд за счёт образовавшегося избытка
ионов Cl-. Равновесие в
двойном электрическом слое выразится
уравнениемFe3+ + e
![]() Fe2+. Таким образом, возникает
положительный потенциал на платине,
который будет тем выше, чем больше
окислительная способность катиона. И,
наоборот, чем сильнее восстановительная
активность иона, тем вероятней отдача
электрона им в кристаллическую решётку
платины и возникновение отрицательного
заряда на ней. Так появляется отрицательный
потенциал на платине в растворе,
содержащем ионыCr2+.
В двойном слое устанавливается равновесиеCr2+
Fe2+. Таким образом, возникает
положительный потенциал на платине,
который будет тем выше, чем больше
окислительная способность катиона. И,
наоборот, чем сильнее восстановительная
активность иона, тем вероятней отдача
электрона им в кристаллическую решётку
платины и возникновение отрицательного
заряда на ней. Так появляется отрицательный
потенциал на платине в растворе,
содержащем ионыCr2+.
В двойном слое устанавливается равновесиеCr2+![]() Cr3+
+ e.Потенциал платины в
разобранных двух примерах определяется
соотношением активных концентраций
окисленной и восстановленной формы
ионов и характеризует
окислительно-восстановительную
способность каждой из системFe2+, Fe3+ / PtиCr2+
,Cr3+ / Pt,
потому этот потенциал называетсяокислительно - восстановительным.
Cr3+
+ e.Потенциал платины в
разобранных двух примерах определяется
соотношением активных концентраций
окисленной и восстановленной формы
ионов и характеризует
окислительно-восстановительную
способность каждой из системFe2+, Fe3+ / PtиCr2+
,Cr3+ / Pt,
потому этот потенциал называетсяокислительно - восстановительным.
Во всех случаях возникающему электродному потенциалу присваивают тот знак, который имеет поверхность металла в двойном электрическом слое.
Разные металлы имеют различные потенциалы. Чем более активным является металл, тем отрицательнее его равновесный потенциал.
Потенциал электрода в растворе зависит не только от природы металла, но и от концентрации раствора и температуры. Зависимость равновесного потенциала электрода от концентрации выражается уравнением Нернста:
E![]() =E
=E![]() +
+![]() ln [Men+],
ln [Men+],
где [Men+]-концентрация ионов металла в растворе,г - моль/л;
R- универсальная газовая постоянная;8,314 Дж/град. моль
n - валентность металла;
F- число Фарадея;96 494 Кл/г-экв.
Т- температура раствора.
Подставив значение R иFприT = 2980, получим уравнение в приведенном виде:
EMe
= E
![]() +
+![]() lg [Men+],
lg [Men+],
где E
![]() - стандартное значение электродного
потенциала.
- стандартное значение электродного
потенциала.
Потенциал называется стандартным (нормальным) в том случае, когда активность каждого из участников обратимой электродной реакции равна единице. Если окислитель или восстановитель в системе находится в газообразном состоянии (O2,Cl2,H2и др.), тоа = 1при давлении газа1 атм.
Так как до сих пор не существует методов измерения абсолютных величин потенциалов, то в качестве потенциала сравнения, условно принятого за нуль, выбран потенциал нормального водородного электрода (концентрация ионов [H+] в раствореH2SO4равна1 г –ион/лиp = 1 атм). По отношению к этому стандартному электроду измеряют потенциалы различных электродов. Значения стандартных электродных потенциалов сведены в таблицу. Ряд стандартных электродных потенциалов называют также рядом напряжений металлов. Каждый металл, стоящий в ряду напряжений левее, более активен,
чем следующий за ним, может вытеснять из растворов солей все металлы, которые следуют за ним; могут вытеснять водород из кислот, если стоят левее водорода.
