
- •Биологическая химия Руководство к самостоятельной работе студентов
- •Введение
- •Правила работы с тестами
- •Модуль 1 «Белки. Ферменты»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Графологическая структура
- •3.1. Реагенты, позволяющие определить n-концевую аминокислоту -
- •3.2. Реагенты позволяющие определить с-концевую аминокислоту -
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Фотоэлектроколориметр
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Методы осаждения белка»
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Выделение и очистка белков»
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Общие свойства ферментов»
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Основы иммуноферментного анализа
- •Клинико-диагностическое значение ифа
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Контрольные вопросы к модулю «Белки. Ферменты»
- •Примеры заданий тестового контроля знаний
- •Эталоны ответов
- •Модуль 2. «Биохимия питания. Общие пути катаболизма. Биоэнергетика»
- •Рекомендуемые темы реферативных сообщений
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Основные характеристики пищеварительных соков
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •2.1. Анилиновая проба на витамин д.
- •2.2. Реакция с серной кислотой.
- •5.1. Реакция с гидросульфитом натрия.
- •5.2. Реакция с раствором уксусно-кислой меди.
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Количественное определение витаминов.
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний Вид 1. Выберите один наиболее правильный ответ.
- •Самостоятельная работа
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестовых заданий контроля исходного уровня знаний Вид 1. Выбор одного наиболее верного ответа
- •Вид 2. Установить соответствие.
- •Примеры ситуационных задач
- •Задача 2. В эксперименте с изолированными митохондриями в качестве субстрата дыхания используется изоцитрат. Определите:
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры заданий тестового контроля знаний
- •Ответы на тесты
- •Модуль 3 «Структура и обмен углеводов»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Модуль 4. «Структура и обмен липидов»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Занятие № 4. Обмен сложных белков – нуклеопротеинов и хромопротеинов.
- •Методические указания к самоподготовке
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы к коллоквиуму
- •Примеры тестовых заданий
- •Эталоны ответов на тесты:
- •Модуль 6. «Взаимосвязь и регуляция обмена веществ. Гормоны»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Ситуационные задачи
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Современные методы определения количества гормонов
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы к зачетному занятию
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Модуль 7. «Биохимия органов и тканей»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Занятие № 3. Биохимия мышечной и нервной тканей.
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •1. Качественное определение белка.
- •2. Качественное определение сахара в моче с помощью реактива Фелинга.
- •3. Качественное обнаружение сахара в моче при помощи индикаторной бумаги «Глюкотест».
- •4. Количественное определение белка в моче по методу Робертса-Стольникова.
- •5. Качественное определение кетоновых тел.
- •6. Качественная реакция на кровяные пигменты.
- •7. Качественное определение желчных пигментов.
- •8. Проба Петенкофера на желчные кислоты.
- •9. Проба Яффе на уробилин.
- •10. Качественное определение индикана в моче.
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тестовых заданий
- •Эталоны ответов к тестовым заданиям
- •Графологическая структура модуля «Белки. Ферменты»
- •Рекомендуемая литература
- •Журналы по биохимии
- •Некоторые референтные значения биохимических показателей жидких сред организма
- •Некоторые референтные значения биохимических показателей жидких сред организма у детей
- •Оглавление
Эталоны ответов к тестовым заданиям
Вид 1. 1.1.– в (продукт димеризации мочевины – биурет, также содержит фрагмент NH-CO, дающий хелатный комплекс с сульфатом меди);
1.2. – б;
1.3. –в (a-углеродный атом ®карбонильный углерод®амидный азот®a-углеродный атом);
Вид 2. 2.1. 1-е; 2-б; 3-г; 4-ж; 5-в; 6-а; 7-в; 8-д; 9-е;
2.2. – 1, 9, 10 – б; 2-д; 3-в; 4,6 – г; 5, 7, 8 – а;
2.3. - 1-а; 2-в; 3-б, в, г, д;
Вид 3. 3.1. –б, г; 3.2-а, в;
Вид 4. 4.1 – А (+, +, +); 4.2 - А (+, +, +).
Эталоны ответов на ситуационные задачи
Задача 1. С биуретовым реактивом реагируют пептидные группы белков – образуется хелатный комплекс фиолетового цвета. По сравнению с иммуноглобулинами, альбумин содержит меньше остатков аминокислот, так как имеет меньшую молекулярную массу, следовательно, интенсивность окраски раствора альбумина будет меньше.
Задача 2. Нингидрин является специфичным реагентом для a-аминокислот, тогда как пролин и оксипролин являются иминокислотами. С a-аминокислотами нингидрин реагирует по следующей схеме:
нингидрин α - аминокислота
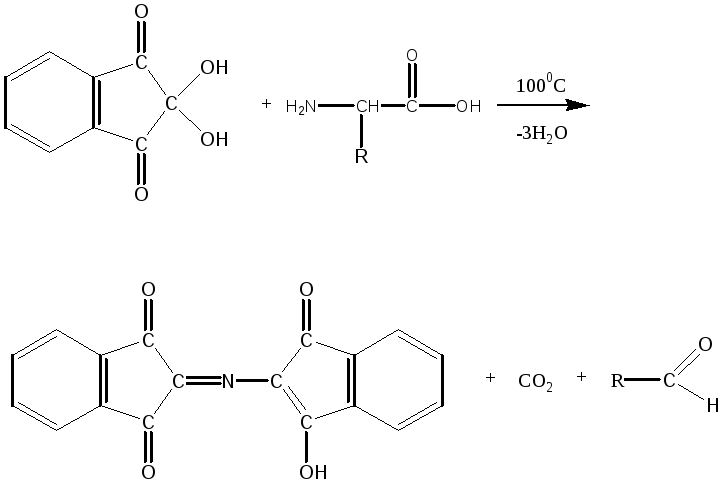
продукт реакции сине-фиолетового цвета альдегид
(светопоглощение в области 550-570 нм)
Занятие № 2. Физико-химические свойства белков.
Цель занятия. Изучить физико-химические свойства белков и овладеть некоторыми методами их анализа, используемыми в диагностических и препаративных целях.
|
Студент должен | |
|
знать: |
уметь: |
|
-строение белковой молекулы – уровни организации и связи их стабилизирующие; -электрические, амфотерные свойства белков; -факторы, определяющие растворимость белков; -методы осаждения белков из растворов. |
-разделять альбумины и глобулины крови методом высаливания; -определять количественное содержание белка в моче методом Брандберга-Роберта-Стольникова; -интерпретировать полученные данные.
|
Содержание занятия. После контроля выполнения самоподготовки студентам предстоит ответить на вопросы тест-контроля и вопросы преподавателя, провести фракционирование белков сыворотки крови методом высаливания, осаждение белков под действием температуры, органических и минеральных кислот, солей тяжелых металлов и количественное определение содержание белка в моче по методу Брандберга-Робертса-Стольникова, проанализировать полученные результаты и сделать соответствующие выводы.
УИРС. Решение ситуационных задач и обсуждение реферативных сообщений. Качественное и количественное исследование мочи на содержание белка. Сравнение различных методов количественного определения белка моче.
Методические указания к самоподготовке
При подготовке к занятию следует повторить структуры белка, вспомнить типы связей, стабилизирующие первичную, вторичную и третичную структуры белков. Необходимо изучить обратимые и необратимые методы осаждения белков, их амфотерные и электрические свойства. Для успешного усвоения материала при подготовке к занятию, пользуясь учебником и лекциями и по биохимии, дополнительной литературой, выполните следующие задания.
|
№№ |
Задание |
Указания к выполнению задания |
|
1 |
2 |
3 |
|
1. |
Изучите биологическую роль белка. |
1. Выпишите основные биологические функции, которые выполняют белки в организме человека и животных. |
|
2. |
Вспомните современные представления о структуре белка. |
1. Напишите схематически типы химических и физических связей, участвующих в образовании белковой молекулы. 2. Охарактеризуйте, какие связи участвуют в образовании первичной, вторичной, третичной и четвертичной структуры белка. 3. Что такое фолдинг белка? Роль шаперонов, белков теплового шока в формировании и поддержании нативной конформации белков, дайте понятие о прионовых болезнях. |
|
3. |
Изучите растворимость и осаждаемость белков. |
1. Перечислите факторы, определяющие растворимость белков. 2. Охарактеризуйте особенности белковых растворов. В чем суть нефелометрического определения содержания белка? 3. Приведите два основных фактора стабилизации белка в растворе. 4. В чем суть явления высаливания? 5. Приведите примеры практического использования высаливания. 6. Дайте определение явлению денатурации. Приведите классификацию видов денатурации. 7. Объясните механизм денатурирующего действия температуры, солей тяжелых металлов, спиртов, фенолов. 8. Приведите примеры практического использования денатурации белков. |
|
4. |
Изучите электрические свойства белков. |
1. Докажите амфотерные свойства белков. 2. Напишите схему диссоциации карбоксильной группы и аминогруппы в составе белка. 3. Выпишите два основных фактора, определяющих заряд белковой молекулы. 4. Напишите, что называется изоэлектрической точкой. Каковы свойства белков в изоэлектрическом состоянии? |
Выпишите кратко принцип метода и технику работ, выполняемых на лабораторном занятии. При этом не забывайте оставлять места для выводов и расчётов.
