
- •Биологическая химия Руководство к самостоятельной работе студентов
- •Введение
- •Правила работы с тестами
- •Модуль 1 «Белки. Ферменты»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Графологическая структура
- •3.1. Реагенты, позволяющие определить n-концевую аминокислоту -
- •3.2. Реагенты позволяющие определить с-концевую аминокислоту -
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Фотоэлектроколориметр
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Методы осаждения белка»
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Выделение и очистка белков»
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Общие свойства ферментов»
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Основы иммуноферментного анализа
- •Клинико-диагностическое значение ифа
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Контрольные вопросы к модулю «Белки. Ферменты»
- •Примеры заданий тестового контроля знаний
- •Эталоны ответов
- •Модуль 2. «Биохимия питания. Общие пути катаболизма. Биоэнергетика»
- •Рекомендуемые темы реферативных сообщений
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Основные характеристики пищеварительных соков
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •2.1. Анилиновая проба на витамин д.
- •2.2. Реакция с серной кислотой.
- •5.1. Реакция с гидросульфитом натрия.
- •5.2. Реакция с раствором уксусно-кислой меди.
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Количественное определение витаминов.
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний Вид 1. Выберите один наиболее правильный ответ.
- •Самостоятельная работа
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестовых заданий контроля исходного уровня знаний Вид 1. Выбор одного наиболее верного ответа
- •Вид 2. Установить соответствие.
- •Примеры ситуационных задач
- •Задача 2. В эксперименте с изолированными митохондриями в качестве субстрата дыхания используется изоцитрат. Определите:
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры заданий тестового контроля знаний
- •Ответы на тесты
- •Модуль 3 «Структура и обмен углеводов»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Модуль 4. «Структура и обмен липидов»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Занятие № 4. Обмен сложных белков – нуклеопротеинов и хромопротеинов.
- •Методические указания к самоподготовке
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы к коллоквиуму
- •Примеры тестовых заданий
- •Эталоны ответов на тесты:
- •Модуль 6. «Взаимосвязь и регуляция обмена веществ. Гормоны»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Ситуационные задачи
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Современные методы определения количества гормонов
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы к зачетному занятию
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Модуль 7. «Биохимия органов и тканей»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Занятие № 3. Биохимия мышечной и нервной тканей.
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •1. Качественное определение белка.
- •2. Качественное определение сахара в моче с помощью реактива Фелинга.
- •3. Качественное обнаружение сахара в моче при помощи индикаторной бумаги «Глюкотест».
- •4. Количественное определение белка в моче по методу Робертса-Стольникова.
- •5. Качественное определение кетоновых тел.
- •6. Качественная реакция на кровяные пигменты.
- •7. Качественное определение желчных пигментов.
- •8. Проба Петенкофера на желчные кислоты.
- •9. Проба Яффе на уробилин.
- •10. Качественное определение индикана в моче.
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тестовых заданий
- •Эталоны ответов к тестовым заданиям
- •Графологическая структура модуля «Белки. Ферменты»
- •Рекомендуемая литература
- •Журналы по биохимии
- •Некоторые референтные значения биохимических показателей жидких сред организма
- •Некоторые референтные значения биохимических показателей жидких сред организма у детей
- •Оглавление
Эталоны ответов к тестовым заданиям
Вид 1. 1.1.- а, 2- в, 3- г.
Вид 2. 2.1.: 1-в, 2-а, 3-б, 4-г, 5-в; 2.2.: 1-г, 2-в, 3-а, 4-б;
2.3: 1-а; 2-в; 3-д; 4-б; 5-г; 6-а.
Вид 3. 3.1.- 1, 2, 3; 3.2.- 1, 3; 3.3.- 4.
Вид 4. 4.1.- D (-, +, -); 4.2.- С (+, -, -).
Эталоны ответов на ситуационные задачи
Задача 1. Энергия гидролиза АТФ составляет – 7,3 ккал/моль, следовательно, гидролиз 12,5 молекул АТФ высвобождает 12,5 ´ 7,3 = 91,3 ккал/моль энергии, тогда как образование этого количества АТФ требует 273 ккал. Эффективность составляет 91,3´100/273=33,4%.
Задача 2. В результате альдольной конденсации щавелевоуксусной кислоты и меченого по указанным положениям ацетила образуется лимонная кислота со следующим распределением радиоактивной метки

Углеродные атомы, имеющие происхождение из меченого ацетила, в ходе первого оборота цикла окисляться не будут, поэтому радиоактивная метка будет обнаруживаться в центральных атомах регенерированного ЩУК (НООС-14СН214СО-СООН). В ходе второго оборота, после конденсации ацетила и меченого ЩУК, будет образовываться лимонная кислота:
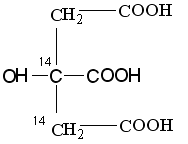 ,
,
поэтому в ходе второго оборота меченые углероды окислительному декарбоксилированию подвергаться не будут и выделится ЩУК со следующим распределением радиоактивной метки НООС-СН214СО-14СООН. Таким образом, 14СО2 будет выделяться в ходе третьего оборота цикла.
Задача 3. Активность ферментов определяется при концентрациях субстрата, обеспечивающих V max, поэтому состав инкубационной среды по прямой реакции должен содержать субстрат – яблочную кислоту. Достижение V max требует и поддержания оптимального значения рН, следовательно, должен использоваться соответствующий буфер. Вследствие того, что НАД-зависимые дегидрогеназы непрочно связывают кофермент, требуется добавление к среде определения и кофермента – окисленной формы НАД. Для определения активности фермента по обратной реакции (по убыванию светопоглощения) среда будет содержать оксалоацетат, восстанновленный НАД и соответствующий буфер.
Занятие № 5. Тканевое дыхание. Окислительное фосфорилирование (cеминар).
Цель занятия. Усвоить узловые вопросы сопряженного и свободного окисления, закрепив представления о связи энергетического обмена с анаболическими и катаболическими процессами обмена веществ в клетках, студент должен:
|
знать: |
уметь: |
|
1. Биологическое окисление в дыхательной цепи митохондрий, связь его с синтезом АТФ. 2. Окислительное фосфорилирование, его количественная характеристика, хемиосмотическая теория сопряжения дыхания и фосфорилирования. 3. Разобщение тканевого дыхания и фосфорилирования. Терморегуляторная функция тканевого дыхания. Особенности окисления в буром жире, значение процессов окисления в буром жире для младенцев.
|
1. Написать схему полной и укороченной дыхательной цепи митохондрий, включающую дыхательные комплексы I – IV, пункты сопряжения с фосфорилированием АДФ. 2. Написать схему перепада редокс-потенциалов компонентов цепи переноса электронов (ЦПЭ) от субстратов на кислород. 3. Объяснить механизм сопряжения дыхания и фосфорилирования, различия величин коэффициента P/O для субстратов пиридиновых (НАД-зависимых) и флавиновых (ФАД-зависимых) дегидрогеназ ЦПЭ. 4. Вычислить энергетическую эффективность (выход АТФ) процессов: цикла трикарбоновых кислот, полного окисления пирувата. 5. Объяснить механизмы разобщения дыхания и фосфорилирования; терморегуляторную функцию тканевого дыхания бурого жира, значение процессов окисления в буром жире для младенцев. |
