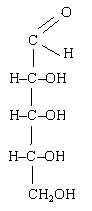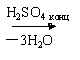- •Биологическая химия Руководство к самостоятельной работе студентов
- •Введение
- •Правила работы с тестами
- •Модуль 1 «Белки. Ферменты»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Графологическая структура
- •3.1. Реагенты, позволяющие определить n-концевую аминокислоту -
- •3.2. Реагенты позволяющие определить с-концевую аминокислоту -
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Фотоэлектроколориметр
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Методы осаждения белка»
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Выделение и очистка белков»
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Графологическая структура «Общие свойства ферментов»
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Основы иммуноферментного анализа
- •Клинико-диагностическое значение ифа
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Контрольные вопросы к модулю «Белки. Ферменты»
- •Примеры заданий тестового контроля знаний
- •Эталоны ответов
- •Модуль 2. «Биохимия питания. Общие пути катаболизма. Биоэнергетика»
- •Рекомендуемые темы реферативных сообщений
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Основные характеристики пищеварительных соков
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •2.1. Анилиновая проба на витамин д.
- •2.2. Реакция с серной кислотой.
- •5.1. Реакция с гидросульфитом натрия.
- •5.2. Реакция с раствором уксусно-кислой меди.
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •Количественное определение витаминов.
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний Вид 1. Выберите один наиболее правильный ответ.
- •Самостоятельная работа
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Примеры тестовых заданий контроля исходного уровня знаний Вид 1. Выбор одного наиболее верного ответа
- •Вид 2. Установить соответствие.
- •Примеры ситуационных задач
- •Задача 2. В эксперименте с изолированными митохондриями в качестве субстрата дыхания используется изоцитрат. Определите:
- •Эталоны ответов к тестовым заданиям
- •Эталоны ответов на ситуационные задачи
- •План занятия
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры заданий тестового контроля знаний
- •Ответы на тесты
- •Модуль 3 «Структура и обмен углеводов»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Модуль 4. «Структура и обмен липидов»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов для контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Занятие № 4. Обмен сложных белков – нуклеопротеинов и хромопротеинов.
- •Методические указания к самоподготовке
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы к коллоквиуму
- •Примеры тестовых заданий
- •Эталоны ответов на тесты:
- •Модуль 6. «Взаимосвязь и регуляция обмена веществ. Гормоны»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Ситуационные задачи
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Современные методы определения количества гормонов
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры тестов контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на тесты
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы к зачетному занятию
- •Примеры тест-контроля
- •Эталоны ответов на тесты
- •Модуль 7. «Биохимия органов и тканей»
- •Рекомендуемые темы реферативных сообщений
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Занятие № 3. Биохимия мышечной и нервной тканей.
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Примеры контроля исходного уровня знаний
- •Примеры ситуационных задач
- •Самостоятельная работа студентов
- •1. Качественное определение белка.
- •2. Качественное определение сахара в моче с помощью реактива Фелинга.
- •3. Качественное обнаружение сахара в моче при помощи индикаторной бумаги «Глюкотест».
- •4. Количественное определение белка в моче по методу Робертса-Стольникова.
- •5. Качественное определение кетоновых тел.
- •6. Качественная реакция на кровяные пигменты.
- •7. Качественное определение желчных пигментов.
- •8. Проба Петенкофера на желчные кислоты.
- •9. Проба Яффе на уробилин.
- •10. Качественное определение индикана в моче.
- •Эталоны ответов на ситуационные задачи
- •Методические указания к самоподготовке
- •Контрольные вопросы
- •Примеры тестовых заданий
- •Эталоны ответов к тестовым заданиям
- •Графологическая структура модуля «Белки. Ферменты»
- •Рекомендуемая литература
- •Журналы по биохимии
- •Некоторые референтные значения биохимических показателей жидких сред организма
- •Некоторые референтные значения биохимических показателей жидких сред организма у детей
- •Оглавление
Примеры ситуационных задач
Задача 1. В приемное отделение больницы поступил 67-летний мужчина с жалобами на сжимающие боли в груди и сильную одышку. Цвет лица и конечностей синюшный, кровь, взятая на анализ, шоколадного цвета. Больной сообщил, что долгое время страдает от стенокардии и принимает препараты изосорбита тринитрата и нитроглицерин. Что послужило причиной резкого ухудшения состояния больного?
Задача 2. Больная 42 лет. Жалуется на боли в области почек и при мочеиспускании. При анализе крови изменений не обнаружено. В моче обнаружена кровь, белок – 0,33%, значительное количество осадка. Содержание урогликопротеинов в суточной моче 95 мг. Какое заключение можно сделать на основе анализа мочи? Какие дополнительные биохимические исследования необходимо провести для уточнения диагноза?
Самостоятельная работа студентов
Работа № 1. Проба Тейхмана.
Проба позволяет обнаружить наличие очень небольших количеств крови в исследуемом материале. Широко используется в судебно-медицинской практике.
Проба основана на том, что при действии на гемоглобин концентрированных кислот происходит отщепление свободного гема, который в присутствии солей соляной кислоты переходит в гемин, выпадающий в форме характерных кристаллов ромбовидной формы.
Ход работы.Приготовить мазок крови и осторожно подсушить его, держа стекло высоко над пламенем спиртовки. Прибавить 2-3 кристалликаNaClи 1-2 капли концентрированной уксусной кислоты, тщательно перемешать стеклянной палочкой и нагреть до кипения на небольшом пламени.
П осле
охлаждения стекла исследовать мазок
под микро- скопом. Кристаллы гемина
зарисовать в протоколе.
осле
охлаждения стекла исследовать мазок
под микро- скопом. Кристаллы гемина
зарисовать в протоколе.
Рисунок 4. Кристаллы гемина под микроскопом.
Работа № 2. Выделение муцина слюны и определение в нем углеводного компонента.
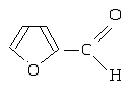
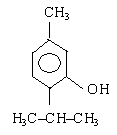
Углевод в муцине можно обнаружить с помощью реакции Молиша. Реакция основана на дегидратации гексоз и пентоз с образованием оксиметилфурфурола и фурфурола при действии концентрированной серной кислоты, которые дают с тимолом продукт конденсации красного цвета.
|
|
|
|
+ |
|
|
продукт конденсации красного цвета
|
|
рибоза |
|
фурфурол |
|
тимол |
|
|
Порядок выполнения работы.В пробирку собирают около 2 мл слюны и по каплям (4-5 капель) приливают концентрированную уксусную кислоту. Выпадает осадок муцина, трудно растворимый в избытке уксусной кислоты. Жидкость из пробирки осторожно сливают. Со сгустком муцина проделывают реакцию Молиша, доказывающую присутствие в белке углеводов. Для этого к сгустку муцина добавить 0,5-1,0 мл 1% спиртового раствора тимола. Содержание пробирки перемешать, по стенке пробирки наслоить равный объем концентрированной серной кислоты. Появляется красное окрашивание.
Работа № 3. Выделение казеиногена из молока.
В молоке казеиноген содержится в виде растворимой кальциевой соли. При подкислении достигается изоэлектрическая точка, и казеиноген выпадает в осадок в свободном виде. Избыток кислоты мешает осаждению, т.к. при pHниже изоэлектрической точки (pH=4,7) молекулы белка перезаряжаются, и казеиноген вновь переходит в раствор.
Ход работы.Молоко (2 мл) разбавляют равным объемом дистиллированной воды и осаждают казеиноген добавлением 2 капель 10% раствора уксусной кислоты. Казеин выделяется в виде хлопьевидного осадка, который отфильтровывают и промывают на фильтре дистиллированной водой (2-3 раза). Небольшие порции осадка снимают с фильтра стеклянной палочкой и употребляют для цветных реакций на белки (провести биуретовую пробу).
Работа № 4. Гидролиз казеина и открытие в гидролизате фосфорной кислоты.
Ход работы.100 мг порошка казеина растворяют в пробирке в 3 мл 10% раствора едкого натра или кали. Пробирку закрывают пробкой со стеклянной трубкой в качестве холодильника, закрепляют ее на асбестовой сетке металлической лапкой и нагревают. Через час после начала кипения жидкости гидролиз прекращают, жидкости дают остыть и нейтрализуют ее концентрированной азотной кислотой (12-15 капель) до слабокислой реакции на лакмус. При нейтрализации выпадает осадок высокомолекулярных продуктов неполного гидролиза белков (пептоны). После отстаивания жидкость фильтруют, с фильтром проделывают молибденовую пробу на фосфорную кислоту (к 20 каплям молибденового реактива добавляют 2-3 капли гидролизата и кипятят несколько минут на голом огне). Выпадает небольшой кристаллический осадок фосфорномолибденовокислого аммония (лимонно-желтого цвета).
12(NH4)2·Mo O4 + H3PO4 + 21HNO3 → (NH4)3PO4·12Mo O3 + 21 NH4NO3 + 12 H2O
желтый кристаллический осадок
По результатам проведенных качественных проб на простетические группы сложных белков заполните следующую таблицу:
|
Сложный белок |
Простетическая группа |
Реакция, характерная для простетической группы |
Результат |
Чем обусловлена реакция |
|
|
|
|
|
|
Работа № 5. Определение липопротеинов низкой плотности (ЛПНП) в сыворотке крови турбидиметрическим методом.
Клинико-диагностическое значение. Содержание ЛПНП (b-липопротеинов) в крови колеблется в зависимости от возраста, пола и составляет в норме 3-4,5 г/л. Увеличение концентрации ЛПНП наблюдается при атеросклерозе, механической желтухе, острых гепатитах, хронических заболеваниях печени, сахарном диабете, гликогенозах, ксантоматозе и ожирении.
Принцип метода. Метод основан на способности ЛПНП образовывать с гепарином комплекс, который под действием хлорида кальция выпадает в осадок. По степени помутнения раствора судят о концентрации ЛПНП в сыворотке крови.
Ход работы. 1. В пробирку вносят 2 мл раствора хлорида кальция и 0,2 мл сыворотки крови. Содержимое пробирки перемешивают.
2. Определяют оптическую плотность раствора (Е1) против раствора хлорида кальция при красном светофильтре (630нм) в кювете на 0,5 см.
3. Раствор из кюветы переливают в пробирку, добавляют микропипеткой 0,04 мл 1% раствора гепарина и точно через 4 мин снова определяют оптическую плотность раствора (Е2) в тех же условиях.
4. Рассчитывают концентрацию ЛПНП (с, г/л) по стандартной формуле:
С = (Е2- Е1) х 10, где 10 – эмпирический коэффициент