
5 курс / Госпитальная педиатрия / Кардиология_и_ревматология_детского_возраста_Самсыгина
.pdfБолезни миокарда |
1 8 1 |
рацией мононуклеарными клетками, в дальнейшем (после 15 дня) возникает картина, характерная для ДКМП.
Клинические данные также подтверждают значение вирусов в этиологии ДКМП. Так у больных ДКМП значительно чаще, чем у здоровых определяются нейтрализующие антитела к серовариантам ВЗ, В4, В6 вирусов Коксаки в высо ких титрах 1:128. Эти данные служат основанием для предположения, что ДКМП является либо исходом вирусного кардита, либо возникает первично на фоне нарушенных механизмов иммунологической защиты.
Вирусоиммунологическая теория. Обсуждается возможность прямого кардиоцитотоксического действия вируса, в сочетании с иммунологическими на рушениями. Высказывается предположение, что вирус управляет иммунным ответом, но не вызывает прямо "иммунной фазы" повреждения.
Вирусы, персистирующие в миокарде содержат белки, частично гомологич ные аутоантителам, в результате чего продолжается иммуностимуляция. Ауто иммунное влияние на развитие идиопатической ДКМП изучено больше на гу моральном иммунитете. Имеются сообщения о наличии кардиальных органоспецифических аутоантител, таких как антимиозин, антиактин, антимиолемма, анти-альфа-миозин и анти-бета-миозин тяжелых цепей, последние две харак теризуются высокой специфичностью для кардиомиоцитов и вставочных дис ков. Выявлен также анти-аденозин-дифосфат-аденозин-трифосфат, представ ляющий антитела к митохондриальной мембране кардиомиоцита и оказываю щий неблагоприятное влияние на функционирование мембранных кальциевых каналов, что в свою очередь приводит к нарушению метаболизма миокарда. Однако подобные открытия являются лишь следствием причинного фактора, который еще необходимо установить. Следует отметить, что кардиоспецифические антитела в большинстве случаев выявлены при семейных ДКМП, следо вательно, генетические факторы могут иметь большое значение в развитии иди опатической ДКМП, что стало очевидно в результате многих работ. Антимиокардиальные антитела выявляются в 5 4 - 6 3 % случаев у больных с ДКМП при иммуноморфологическом изучении биоптата и в 1 1 - 3 0 % в сыворотке крови. У 50% больных с ДКМП обнаруживаются антитела к миелину, что возможно при водит к демиелинизации волокон афферентной системы. Эти антитела способ ны повреждать нервные окончания за счет комплимент-зависимого иммунного цитолиза или индукции антитело-зависимой цитотоксичности.
Иммунологические нарушения при ДКМП. Материалы, касающиеся иссле дования субпопуляции лимфоцитов при ДКМП противоречивы. Возможно сни жение числа Т-супрессоров и увеличение соотношения хелперов к супрессорам. Увеличение соотношения хелперы/супрессоры может сопровождаться увеличе нием содержания В-лимфоцитов, гиперинтерферонемией, повышением содер жания бета-2 микроглобулина, что возможно является признаком активации им-
182 КАРДИОЛОГИЯ И РЕВМАТОЛОГИЯ ДЕТСКОГО ВОЗРАСТА
мунной системы в ответ на вирусную инфекцию. Наряду с дисбалансом иммунорегуляторных клеток отмечено и изменение клеточных цитотоксических реак ций: снижение естественной цитотоксичности и антителозависимой клеточной цитотоксичности. Последнее обусловлено сниженным содержанием в крови ко личества эффекторных клеток, нарушением функциональной активности есте ственных киллеров, действием интерферона и интерлейкина 2.
Существуют данные, указывающие на возможность генетической детерми нированности иммунного ответа при ДКМП. Обнаружение с помощью моноклональных антител антигенов второго класса системы HLA В12, В27, DR4, DR5 на клетках эндокарда или эндотелия рассматривается как маркер ДКМП.
Таким образом, одним из основных механизмов возникновения ДКМ следует считать аутоиммунный, запускаемый кардиотропными вирусами в условиях из мененной иммунологической реактивности.
Роль генетических факторов в возникновении ДКМП.
Важнейшим открытием для медицины стала возможность молекулярной ге нетики идентифицировать гены, отвечающие за развитие тех или иных заболе ваний. С этой точки зрения большие успехи достигнуты при изучении генети ческого базиса идиопатических ДКМП. Среди идиопатических ДКМП семейная агрегация заболевания варьирует от 25 до 50% случаев. Преимущественно превалирует аутосомно-доминантное наследование (аутосомно-доминантные ДКМП). Наряду с аутосомно-доминантными описываются аутосомно-рецессив- ные,Х-сцепленные, митохондриальные ДКМП. Аутосомно-доминантные формы характеризуются клинической вариабельностью и генетической гетерогеннос тью. Эти формы ассоциируются с шестью различными локусами: так называе мая простая ДКМП - с локусами 1q32,2p31,9ql3,10q21-q23, тогда как ДКМП с нарушениями проводимости - с локусами 1q1-1q1, Зр22-3р25, причем неиз вестно, за синтез каких кардиальных белков отвечают эти локусы. Установлено, что мутации кардиального актина локализуются в локусах 9 q l 3 - 22 и lq32, а также в локусе15q14.Показано, что если ДКМП выявляется у одного из род ственников 1 степени пробанда, эмпирический риск наличия подобных забо леваний у других членов семьи не менее 6%, если поражен более, чем один родственник 1 степени родства, риск заболевания возрастает до 50%.
Митохондриальные ДКМП являются следствием аномалии митохондриальной структуры и дисфункции процесса окислительного фосфорилирования. Как известно, митохондрии имеют собственную ДНК, содержащую всего лишь 37 генов, и свои механизмы транскрипции и трансляции. Митохондриальные ДНК отличаются от геномных ДНК тем, что первые не имеют интронов, защитных гистонов, эффективных ДНК-восстановительных систем, следовательно часто та мутаций митохондриальных ДНК в 10 раз выше, чем в ядерных геномных ДНК. В каждой митохондрии имеется одиночная хромосома, кодирующая ряд
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Болезни миокарда |
183 |
ферментов (13 из 69), участвующих в механизме окислительного фосфорилирования. Следовательно, вследствие мутации нарушается энергетический об мен кардиомиоцитов, что ведет к развитию ДКМП.
Описаны точечные мутации и множественные делеции в митохондриальных ДНК как при спорадических случаях ДКМП, так и при семейных. Многие мито хондриальные миопатии ассоциируются с неврологическими нарушениями и поражением сердца. Митохондриальные ДКМП встречаются при таких мито хондриальных синдромах, как синдром MELAS (митохондриальная миопатия,
энцефалопатия, |
лактацидоз, |
эпизоды нарушения |
мозгового |
кровообращения), |
||||
MERRF |
(сопровождается |
миоклонус-эпилепсией), |
Kearus-Sayre-синдром |
(KSS), |
||||
при синдроме |
дефицита |
НАДН - коэнзим |
Q редуктазы. При синдромах MELAS и |
|||||
MERRF |
выявлены точечные |
мутации, |
делеции |
найдены |
при |
синдроме |
||
KSS (Синдром |
Кернса-Сейра). |
|
|
|
|
|
||
Существенный прогресс достигнут в изучении молекулярных основ Х-сцеплен- ных ДКМП. Описаны мутации различных участков гена, отвечающего за синтез белка дистрофина (21 хромосома). Дистрофии - миокардиальный белок, входя щий в состав мультипротеинного комплекса, который связывает мышечный цитоскелет кардиомиоцита с внеклеточным матриксом, благодаря этому происходит скрепление кардиомиоцитов в экстрацеллюлярном матриксе. В клетке дистрофии связан непосредственно с сократительным белком актином. Таким образом, дист рофии выполняет ряд важнейших функций: 1) мембраностабилизирующую; 2) пе редает сократительную энергию кардиомиоцита во внеклеточную среду; 3) обес печивает мембранную дифференциацию, т.е. специфичность мембраны кардио миоцита. Выявлены мутации, при которых происходит замена нуклеотидов, в ре зультате чего синтезируются аминокислоты, которые нарушают полярность и дру гие свойства дистрофина как белка, поэтому теряется мембраностабилизирующее свойство последнего. Итогом является дисфункция кардиомиоцита.
Мутации гена дистрофина описаны также при ДКМП, ассоциированных с мышечными дистрофиями Дюшена, Беккера, чаще всего в этих случаях выяв лялись делеции. Однако популяционных исследований по выявлению мутации гена дистрофина у неродственных больных идиопатической ДКМП не проводи лось. По данным С.Н.Терещенко исследование по выявлению мутации генов кардиального актина и дистрофина у 20 больных идиопатическойДКМП выяв лено не было. Не менее значимым было бы исследование генов других струк турных компонентов сердечной мышцы, в частности, коллагена и эластина, му тация которых, возможно, тоже имеет значение в развитии ДКМП . При мышеч ной дистрофии Эмери-Дрейфуса (Х-сцепленной), одной из проявлений кото рой является ДКМП, выявлена мутация гена, отвечающего за синтез белка эмерина (28-я хромосома). Эмерин является компонентом оболочки ядра кардио миоцита и скелетной мускулатуры, поэтому наряду с ДКМП заболевание харак-
184 КАРДИОЛОГИЯ И РЕВМАТОЛОГИЯ ДЕТСКОГО ВОЗРАСТА
теризуется также наличием суставных контрактур. Дебютирует заболевание чаще в возрасте от 2 до 10 лет, когда появляется слабость в мышцах плечевого пояса и верхних конечностей.
Что касается несемейных случаев идиопатической ДКМП, описано нарушение в экспрессии гена белка метавинкулина. Последний является белком цитоскелета кардиомиоцита и связывает актин со вставочными дисками. Исследованы 23 боль ных с идиопатической ДКМП, с помощью полимеразной цепной реакции выявлено нарушение транскрипции метавинкулина и отсутствие этого белка в тканях сер дечной мышцы. В ряде работ выявлена усиленная экспрессия генов внеклеточных белков металлопротеиназ, одним из представителей которых является интерстициальная коллагеназа; у больных с идиопатической ДКМП отмечено 3-4-х кратное повышение уровня последнего в сердечной ткани. Проводился поиск взаимосвязи между полиморфизмом гена АПФ и идиопатической ДКМП. В трех работах отмече на корреляция DD-генотипа с ДКМП. В настоящее время во Франции в этом плане проводится исследование 433 больных с идиопатической ДКМП.
Изучение системы HLA у больных КМП не позволило выделить специфичес кий генный дефект, ответственный за возникновение заболевания. Вместе с тем выделены HLA гены, локализующиеся в районе 6 хромосомы, контролиру ющие механизм иммунного ответа на вирусный агент.
Таким образом, бесспорна роль генетических факторов в этиопатогенезе ДКМП.
Патоморфологические изменения
ДКМП характеризуется фокальным повреждением кардиомиоцитов, следстви ем чего является их некроз. Погибшие клетки замещаются соединительной тка нью с развитием фиброза. Причина фокального, а не диффузного поражения кардиомиоцитов недостаточно ясна, возможно, это связано с особенностями регионарного кровообращения (рис. 39).
Фиброз необходим не только для замещения погибшей миокардиальной тка ни, но и важен как компенсаторный механизм, предотвращающий дальнейшую дилатацию камер сердца. Дилатация сердца хотя и способна длительно ком пенсировать сниженную сократительную способность миокарда, но невыгодна с энергетической точки зрения. Чрезмерное развитие соединительной ткани сердца способствует сдавлению капилляров и/или соседних жизнеспособных клеток, что усиливает ишемический компонент. При этом происходит наруше ние энергетического метаболизма в виде недостаточного ресинтеза аденозинтрифосфата из-за нарушения гликолиза в кардиомиоцитах. Также имеет место снижение уровня фосфокреатинина, отражающее степень фиброза
Стенки дилатированного левого желудочка вынуждены развивать гораздо большее напряжение для создания нормального давления в полости левого желудочка, следствием чего является повышенная потребность миокарда в кис-
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

Болезни миокарда |
185 |
Рис. 39. Макропрепарат сердца при Д К М П . Имеет место дилатация всех
полостей сердца с одновременной гипертрофией миокарда (масса сердца увеличена в 3 раза). Обращает на себя внимание хорошее состояние коронар
ных артерий. В области верхушки левого желудочка имеются небольшие пристеночные тромбы (которые при Д К М П становятся источником тромбоэмболических осложнений). Цитируется по данным Терещенко
лороде, что способствует развитию ишемических явлений, и в конечном счете усугубляет повреждение кардиомиоцитов.
Оставшиеся жизнеспособные клетки подвергаются изменениям как деструк тивного, так и компенсаторного характера. Отмечается атрофия и альтерна ция кардиомиоцитов с заместительным склерозом, полиморфизм и альтерна ция ядер клеток, кальцификация матрикса митохондрий, характерна дилата ция коронарных артерий, преимущественно в левом венечном бассейне. Наря ду с этим наблюдаются признаки гипертрофии отдельных клеточных органелл - миофибрилл, митохондрий, а также клеток в целом.
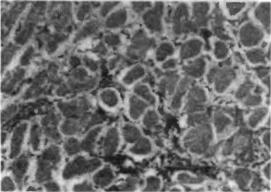
Возможно мутное набухание гипертрофированных мышечных волокон с круп ными уродливыми ядрами и светлыми ободками вокруг них. При этом отмеча ется изменение митохондрий. Волокна актина и миозина разъединены, смеще ны к сарколемме, местами обнаруживаются очаги пересокращения (рис. 40) .
Помимо функции кардиомиоцитов морфологические изменения при ДКМП затрагивают рецепторный аппарат. Так, выявлено уменьшение количества бета 1- и бета 2-адренорецепторов, что может иметь значение в генезе снижения инотропной функции сердца.
186 |
КАРДИОЛОГИЯ И РЕВМАТОЛОГИЯ ДЕТСКОГО ВОЗРАСТА |
Рис. 40. Дилатационная кардиомиопатия. Гистологический препарат миокарда при Д К М П . Отмечается гипертрофия отдельных кардиомиоцитов и интерсти циальный фиброз (коллаген окрашен в синий цвет по Мassort).
Патоморфологические проявления легочной гипертензии при ДКМП.
характеризуются тромботической и плексогенной артериопатией, веноокклюзивная артериопатия встречается значительно реже. Тромботическая артериопатия гистологически характеризуется следующими изменениями сосудис того ложа легких (мелких артерий и артериол): преимущественно эксцентри ческим фиброзом интимы, разной стадии организации микротромбов, гиперт рофией медии и фиброэластическими сетевидными изменениями в просвете сосуда, исходящими из интимы. Тромботическая легочная артериопатия носит прогрессирующий характер. Генерализация данного процесса в артериальном сосудистом ложе легких приводит к диффузной интимальной пролиферации и тромбозу, развитию легочной гипертензии пропорционально тяжести окклю зии сосудов. Плексогенная легочная артериопатия возникает вследствие хро нической высокой легочной гипертензии различной этиологии. Развитие плек согенной артериопатии характеризуется следующей последовательностью: ги пертрофия медии, утолщение интимы и ее пролиферация (по типу "лукович ных" слоев), приводящие к окклюзии просвета сосуда; развитие плексиформных образований. Плексиформные образования проявляются как сплетения канальцев, исходящих из артериолярной стенки. Точная причина образования плексусов не установлена. Поскольку плексиформные изменения гистологи чески возникают вслед за прогрессирующей интимальной пролиферацией и гипертрофией медии, можно полагать, что пусковым механизмом образования плексусов является артериальная вазоконстрикция. Некоторые авторы счита ют, что плексусы отражают стадию пролиферативного замещения области фибриноидного некроза или возникают в результате локального реактивного по-
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Болезни миокарда |
187 |
вреждения сосудов. Другие авторы полагают, что плексусы являются "анасто мозами" между легочными артериями и венами или "аневризмами", возникши ми вследствие недоразвития медии сосуда или ее слабости (Carrington С В . , Liebow А.А., 1970). Во всех случаях плексиформные изменения наблюдаются только при прекапиллярной легочной гипертензии. Ультраструктурные иссле дования показывают, что плексусы состоят из миофибробластов и примитив ных сосудоформирующих резервных клеток. В настоящее время подтвержде но, что клетки, находящиеся в просвете сосуда имеют мышечное происхожде ние и мигрируют из медии артериол (Fujinami М с соавт., 1987). Причина такой пролиферации и миграции этих клеток не установлена.
Результаты биопсии сердечной мышцы. Для верификации диагноза ДКМП наиболее часто используется биопсия правого желудочка. При этом отмечается атрофия и альтерация кардиомиоцитов с заместительным склерозом, полимор физмом и аморфностью ядер клеток сократительного миокарда, а также кальцификация матрикса митохондрий. Волокна актина и миозина разъединены, сме щены к сарколемме, местами образуют узлы пересокращения. У некоторых боль ных обнаруживается уплотнение эндокарда - так называемый фиброэластоз эн докарда. По современным представлениям фиброэластоз эндокарда является реактивным неспецифическим процессом, развивающимся в антенатальном или раннем возрасте в ответ на гипоксическое повреждение миокарда.
Однако существуют большие трудности, не позволяющие в ряде случаев точ но провести грань между миокардитами и ДКМП, особенно при биопсии право го желудочка, чему также способствует очаговость поражения миокарда.
Патогенез
Роль нарушения симпатоадреналового дисбаланса в развитии ДКМП
В последние годы большое внимание исследователи уделяют проблеме симпа тоадреналового дисбаланса при идиопатическихкардиомиопатиях. У больных ДКМП различной этиологии обнаруживается увеличение уровня циркулирующих в кро ви катехоламинов и снижение бетта-адренергического контрактильного резерва. Антитела против beta 1-адренорецепторов при ДКМП обнаруживаются у 73% боль ных (Wallukat G. с соавт.,1992). Развивается, так называемый синдром "потери ре гуляции" ("down-regulation") миокарда бета-рецепторами (Dubrava J. с соавт., 1992). Хроническое увеличение эндогенных катехоламинов в крови и поврежде ние бета-адренергических рецепторов миокарда приводит к адреналовому пора жению миокарда и развитию ДКМП (Stewart M.J., Goldsmith S.R., 1992).
Патогенез легочной гипертензии
Механизм развития легочной гипертензии при ДКМП является сложным и мало изученным. В возникновении венозной легочной гипертензии при ДКМП ведущую роль играют левожелудочковая недостаточность и митральная регургитация. Затруднение оттока крови из легочных вен вследствие левожелудоч-
188 |
КАРДИОЛОГИЯ И РЕВМАТОЛОГИЯ ДЕТСКОГО ВОЗРАСТ/ |
ковой дисфункции и митральной регургитации приводит к легочной артери альной гипертензии по двум причинам: 1) путем механической передачи дав ления с вен через капилляры на артериальную систему; 2) путем рефлекторно го повышения тонуса легочных сосудов. В экспериментальных и клинических исследованиях доказано, что первично возникающее повышение давления в венозном отделе малого круга непосредственно передается на капиллярную сеть и артериальную систему. Этому способствуют меньшая растяжимость леточных вен среднего и крупного калибра по сравнению с соответствующими венозными сосудами большого круга, отсутствие клапанов в легочных венах широкие капилляры легких и значительно меньшее активное сокращение леточных артериол, поскольку последние в противоположность артериолам большого круга имеют слабо развитый мышечный слой. Рефлекторное повышение тонуса легочных артериальных сосудов обусловлено в основном р е ф л е к с ом Китаева. При этом рефлексе раздражение рецепторов левого предсердия и венозно-капиллярного отдела легочных сосудов обуславливает рефлекторное сокращение легочных артериол. Большинство авторов рассматривают рефлекс Китаева как защитный, так как в результате сужения артериол уменьшается приток крови к капиллярам и тем самым предотвращается более значительное повышение в них давления и развитие отека легких.
Понижение напряжения кислорода и повышение напряжения углекислоты в
крови играет определенное значение в возникновении легочной гипертензии у больных с ДКМП. Гипоксия вызывает констрикцию легочных сосудов и повышение легочного сосудистого сопротивления.
Нарушения регуляции тонуса сосудов легочной артерии с их констрикцией обусловленное центральными нервнорефлекторными влияниями или расстройством взаимодействия систем биологически активных веществ, определяющих уровень легочно-артериолярного сопротивления могут являться еще одной причиной легочной гипертензия у больных ДКМП.
Дисфункция клеток эндотелия может быть одним из патогенетических факторов легочной гипертензии при ДКМП. Установлено, что при повреждении эндотелия, возникает резкий вазоспазм и увеличение чувствительности сосудов и вазоконстрикторным стимулам. При гипоксии происходит ингибирование синтеза окиси азота в клетках эндотелия и синтез цГМФ в подлежащих гладкомышечных клетках. Вследствие этого у больных с ДКМП может возникать стойкая вазоконстрикция в легочных сосудах. Возникновение легочной гипертензии при ДКМП может быть связано как с увеличением продукции эндотелиального сокращающего фактора, так и с уменьшением продукции эндотелиального релаксирующего фактора.
Гиперкоагуляционные изменения и микротромбоз мелких сосудов являются еще одной из причин развития легочной гипертензии.
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Болезни миокарда
Роль нарушения клеточной энергетики в развитии ДКМП
Для ДКМП характерны изменения кардиомиоцитов как деструктивного, так и компенсаторного характера. Отмечается атрофия и альтернация кардиомиоци тов с заместительным склерозом, полиморфизм и альтернация ядер клеток, кальцификация матрикса митохондрий. Возможно мутное набухание гипертрофи рованных мышечных волокон с крупными уродливыми ядрами и светлыми обод ками вокруг них. При этом отмечается изменение структуры и функции мито хондрий. Отмечаются деструктивные изменения в митохондриях, уменьшение количества крист что сопровождаются нарушениями энергетического мета болизма. Снижается синтез АТФ и концентрации креатинфосфата, имеет место потеря калия кардиомиоцитами из-за повреждения K-Na-АТФ-азы продуктами перекисного окисления липидов.
Митохондриальные повреждения способствуют нарушению бета-окисления жирных кислот, что сопряжено со снижением уровня карнитина. Обнаружено уг нетение кислород-зависимых звеньев внутриклеточного метаболизма, сопровож дающееся снижением эндогенного цитохрома С. В результате потери К+ кардиоми оцитами и выхода его во внеклеточную среду снижается мембранный потенциал покоя, амплитуда и длительность потенциала действия, максимальная скорость деполяризации, что создает предпосылки для снижения сократительной способ ности миокарда. Кроме того проявляется патогенное действие ферментов лизо сом, снижающее активность АТФ-азы, способствующее выходу К+ из деэнергезированных митохондрий и развитию ацидоза. Одной из причин недостаточного ресинтеза АТФ может быть функциональная неполноценность гликолиза из-за разви тия ацидоза в кардиомиоцитах. Деструктивные изменения проявляются также в вакуолизации структур саркоплазматического ретикулума, истончении миофибрилл, появлении пересокращенных или перерастянутых сакромеров. Последнее обус ловлено, кальциевой перегрузкой кардиомиоцитов и предшествует развитию нео братимых повреждений клеток. Следовательно, причиной сердечной недостаточ ности при ДКМП является необратимая миокардиодистрофия, сопровождающаяся перерастянутостью миофибрилл, массивными фиброзными изменениями в мио карде и электролитными расстройствами, способствующая гемодинамическим из менениям, характеризующимся снижением контрактильной способности миокар да, следствием чего является снижение минутного объема кровообращения.
Клиническая симптоматика
Жалобы
Следует подчеркнуть, что заболевание в течение длительного времени мо жет протекать субклинически, дети не предъявляют жалоб, в связи с чем не редко позднее выявление патологии при развитии выраженных симптомов сер дечной декомпенсации. Кардиомегалия или различного варианта аритмии мо гут длительно предшествовать развитию застойной сердечной недостаточное-
190 КАРДИОЛОГИЯ И РЕВМАТОЛОГИЯ ДЕТСКОГО ВОЗРАС
ти. Увеличение сердца или изменения на ЭКГ часто выявляются случайно на профилактических осмотрах.
У детей наиболее часто первыми клиническими проявлениями заболевания является одышка и/или снижение физической активности.
Одышка является одной частых жалоб у детей ДКМП В основе механизма развития одышки лежит компенсаторная гипервентиляция в ответ на артериальную гипоксемию. Причинами возникновения гипоксемии являются снижение сердечного выброса и минутного объема кровообращения, нарушение вен- тиляционно-перфузионного соотношения в легких. Вначале одышка выявляется только при физической нагрузке, затем при прогрессировании заболевания появляется в покое, иногда сопровождается приступами удушья. Это связано с тем, что при прогрессировании легочной гипертензии значительно снижается адаптивный резерв малого круга кровообращения. Чем выше давление в легочной артерии, тем более выражена одышка.
Синкопе. Возникновение обморочных состояний свидетельствует о наступлении тяжелой стадии заболевания. Обмороки появляются при физической нагрузке, во время игр, эмоционального перенапряжения, однако в ряде случаев могут возникать в покое. Предположительные механизмы обмороков могут быть следующие: вазовагальный рефлекс с легочной артерии,тяжелая правожелудочковая недостаточность, снижение минутного объема, приступ фибриляции желудочков из-за снижения коронарного кровотока при нагрузке.
Стенокардитические боли. Характер болей в сердце у пациентов с ДКМП сжимающий, давящий. Болевой синдром возникает при физической нагрузке или психоэмоциональном напряжении, сопровождается усилением одышки, общим беспокойством, страхом. Боли купируются назначением кислорода, могут наблюдаться и при небольшом повышении давления в легочной артери!
Приступы болей в грудной клетке наиболее часто обусловлены ишемией миокарда, возникающей под действием общей гипоксии. Имеет место недостаточность коронарного кровотока при гипертрофии миокарда и снижении сердечного выброса. Возможен рефлекторный спазм коронарных артерий из-за расширения ствола легочной артерии при легочной гипертензии.
Кашель у детей с ДКМП характеризует наличие венозного застоя в малом круге кровообращения и всегда отражает повышение легочного капиллярного давления
Снижение толерантности к физической нагрузке, быстрая утомляемость, яв ляются характерными жалобами для детей с ДКМП, что является одним из первых клинических проявлений сердечной недостаточности, что обусловлено низкой адап тационной способностью легочной и системной периферической циркуляции.
Физикальные изменения
Основными клиническими симптомами этого заболевания являются кардиомегалия, систолический шум недостаточности митрального и/или трикуспидаль
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
