
6 курс / Кардиология / ХИРУРГИЧЕСКОЕ_ЛЕЧЕНИЕ_ИНФЕКЦИОННОГО_ЭНДОКАРДИТА_И_ОСНОВЫ_ГНОЙНО
.pdfЛетальность у животных без лечения составила 100%, а средняя продолжитель ность жизни – 5,6 ± 2,7 суток. Клинически наблюдались отчетливые признаки гене рализованной гнойной инфекции. Отмечались выраженная адинамия, быстрая по теря массы тела до 25% от исходной, лихорадка неправильного типа с подъемами температуры тела до 40,5–41°С (норма – 38,5–39,5°С), увеличение частоты дыхания до 70–80 в минуту (норма – 50–60 в минуту), частоты сердечных сокращений до 170–175 в минуту, септические поносы. У некоторых животных появлялись при знаки очагового поражения центральной нервной системы (вестибулярные рас стройства, парезы и параличи верхних и нижних конечностей).
Учитывая, что стафилококковый токсин избирательно поражает соматическую нервную систему, вызывая мышечную слабость, парезы, параличи, для оценки обще го состояния животных нами использовался простой тест: время, за которое кролик после быстрого укладывания на бок возвращается в вертикальное положение. Мгновенное возвращение в вертикальное положение характерно для нормальных, здоровых животных. При развернутой клинической картине сепсиса кролики при нимали вертикальное положение спустя 15–20 с. Более длительное время возвраще ния в нормальное положение свидетельствовало о тяжелой интоксикации.
Результаты бактериологических исследований артериальной крови и клапанов сердца у экспериментальных животных (собак) в зависимости от наличия микроор ганизмов в тканях сердца при гистологическом исследовании позволили установить, что если в 1–2-е сутки после введения микроорганизмов в артериальное русло по ложительные гемокультуры были получены у 15 из 21 собаки, то на 6–7-е сутки – лишь у 6 из 17. Это происходит либо вследствие элиминации микробов из организма, либо вследствие отграничения очагов внутрисердечной инфекции от кровеносного русла. Таким образом, при экспериментальном ангиогенном сепсисе частота поло жительных посевов крови снижается в зависимости от продолжительности заболе вания. По всей вероятности, бактериемия, сопровождающая появление очага инфек ции в сердце, по мере его отграничения тромботическими массами начинает носить периодический характер, обусловленный прорывом инфекции через формирующий ся барьер в кровеносное русло.
Из 9 собак, у которых микроорганизмы были выявлены при посмертном гистоло гическом исследовании пораженных клапанов сердца, положительные гемокульту ры оказались лишь у четырех. Это может быть объяснено неудачным выбором участ ка ткани клапана, использованного для посева, и дефектами культуральной техники. С другой стороны, в ряде случаев, когда при гистологическом исследовании микро организмы не обнаруживаются, посевы тканей клапанов, тем не менее, дают рост микрофлоры. Так, был получен рост микрофлоры у четырех животных, хотя при гистологическом исследовании тканей сердца микроорганизмы выявлены не были. Возможно, это связано с тем, что далеко не всегда микробы попадают в гистологи ческий срез, а делать бесконечное множество срезов не имеет смысла. С другой сто роны, возможны артефакты при посевах с клапанов сердца, особенно однократных.
При исследовании иммунологических показателей на третьи и пятые сутки после введения микробной культуры обнаружено статистически достоверное (Р < 0,05) повышение уровня ЦИК с 34 ед. до 61 ед., лейкоцитарного индекса интоксикации с 0,3 до 4,5, титров антистрептолизина-О до 3000 AEStO (при норме 125 AEStO) и титров гетерофильных антител к шигеллам Флекснера и Зонне до 1:16–1:2048 (при
61
норме 1:2–1:16). На 5-е сутки наблюдалось снижение фагоцитарного индекса и фаго цитарного показателя. Различия по другим показателям в эти сроки были статисти чески недостоверны. После 5-х суток описанные иммунологические сдвиги сохраня лись. При бактериальных посевах крови положительная гемокультура зафиксирова на в 70% случаев (14 из 20).
При патологоанатомическом исследовании у большинства погибших животных наблюдалась двусторонняя септическая пневмония, часто с очагами деструкции легочной ткани и большим количеством серозно-геморрагического экссудата в плевральных полостях. Во всех случаях имелась картина септического эндокардита с вегетациями обычно на трикуспидальном клапане, пристеночными эрозиями, абс цессами миокарда, гнойными метастатическими очагами в почках, печени, селезен ке. У некоторых животных наблюдались значительной величины (до 10 см) абсцес сы, локализованные в брюшной полости. Селезенка имела характерный септиче ский вид: увеличенная, дряблая, с поверхности обильно соскабливается пульпа, на разрезе атрофия белой и красной пульпы с почти полным исчезновением лимфо идных фолликулов.
Гистологически у всех животных наблюдались более или менее выраженные явле ния паренхиматозной и жировой дистрофии миокарда, печени и почек. Гнойные очаги в почках представляли собой микроабсцессы, местами сливающиеся между собой, об наруживаемые в основном в корковом веществе. В лимфатических фолликулах селе зенки и лимфоузлов наблюдалось отсутствие центров размножения, слабо выражен ные явления фагоцитоза микробов лейкоцитами в очагах воспаления. У большинства животных резко атрофирован тимус. Повсеместно имелись признаки гемодинами ческих расстройств: полнокровие мелких сосудов, отек стромальной ткани, мелкие периваскулярные кровоизлияния с гемолизированными эритроцитами.
Таким образом, экспериментальные данные также свидетельствуют о том, что внутрисердечный очаг инфекции возникает как следствие срыва компенсации им мунной системы. При этом следует отметить, что резервные возможности организма по борьбе с инфекцией весьма значительны. Поэтому однократное введение стафи лококка не вызывает развитие сепсиса и эндокардита. Это же подтверждают и про веденные нами ранее бактериологические исследования инфузионных жидкостей, приготавливаемых ex tempore и используемых в хирургической клинике для внут ривенного введения. Оказалось, что их микробная загрязненность достигала иногда 22%, однако введение этих растворов также не приводило к развитию сепсиса, т.к. срабатывали механизмы противоинфекционной защиты, обеспечивающие быст рую и эффективную санацию организма.
Монослой эндотелиальных клеток выстилает соединительнотканную мембрану и составляет первый защитный барьер против различных процессов, включая гемостаз и тромбоз. Эндотелиоциты поставляют в субэндотелий ряд веществ: компоненты базальной мембраны, коллаген, эластин, ламилин, протеазы и их ингибиторы, тром боспондин, мукополисахариды, витронектин, фибронектин и фактор Виллебранда. Эти белки имеют большое значение для межклеточного взаимодействия и образова ния диффузного барьера, который предотвращает попадание крови из внутрисосу дистого пространства во внесосудистое. Кроме того, эндотелиальные клетки выпол няют разные физиологические функции, включая регулирование реактивности тромбоцитов, контроль за направленной миграцией лейкоцитов, регулирование
62
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
активности фактора роста и текучести крови. Эндотелиоциты также продуцируют вещества, которые секретируются в просвет сосуда и способствуют текучести крови. К этим веществам относятся: гликозаминогликаны, системы гепарин (гепаран- сульфат)-антитромбин III, тромбин-тромбомодулин-белок С и плазминоген-акти ватор плазмина. Кроме того, эндотелиальные клетки продуцируют простациклин и эндотелиальный фактор релаксации, два возможных ингибитора адгезии и агрега ции тромбоцитов. Эти вещества также являются вазодилататорами и действуют си нергично. Нормальный эндотелий действует как мощная антикоагулянтная поверх ность, которая не активирует белки свертывания крови и не привлекает к себе кле точные компоненты крови. Но после стимуляции или травмы эндотелий трансфор мируется в мощную прокоагулянтную поверхность. Это происходят за счет синтеза, выделения или приобретения многих прокоагулянтных веществ, включая тканевой фактор, фактор Виллебранда, фактор V, ингибиторы активатора плазминогена (ИАП-1 и ИАП-2), интерлейкин-1 (ИЛ-1), фактор некроза ткани (ФНТ), эндоте лин-1 (вазоконстриктор).
Втех же случаях, когда в результате механической травмы эндокарда и последую щего инфицирования этого участка возникал инфекционный очаг в сердце, картина менялась. Теперь уже вегетация микроорганизмов происходила под «прикрытием» слоев фибрина, откладывающегося в зоне травматизации, а выброс микробных аген тов и их токсинов осуществлялся достаточно регулярно. Учитывая же, что характер ной особенностью первичного очага при ангиогенном сепсисе и септическом эндо кардите является поступление возбудителей непосредственно в кровоток, минуя покровный, лимфатический, гистогематический барьеры, то, в конце концов, это обе спечивало истощение (декомпенсацию) тех или иных звеньев иммунной системы
споследующей генерализацией септического процесса и появлением вторичных очагов во внутренних органах и тканях (апостематозный нефрит, септическая пнев мония и т.д.).
Следует заметить, что, по-видимому, срыв компенсации возможен и даже наибо лее вероятен не по всему «фронту противоинфекционной защиты», а лишь на опре деленном его участке. Другими словами, характерную для септического процесса возможность беспрепятственного размножения в организме получают не все сущест вующие виды возбудителей, а лишь один-два, которые не удается нейтрализовать либо ввиду их слабой иммуногенности, либо вследствие быстрых темпов размноже ния, опережающих темпы выработки специфических антител.
Всвязи с тем, что при внутрисердечной инфекции поступление возбудителя про исходит непосредственно в кровоток, доза микробных агентов, необходимая для практически полного блока рецепторов иммунокомпетентных клеток, ответствен ных за распознавание и элиминацию генетически чужеродного материала, а также рецепторов имеющихся антител, оказывается вполне достаточной даже при неболь ших размерах очага. Оставшиеся необезвреженными микробные агенты получают определенную свободу для дальнейшего размножения и диссеминации. При этом развивающийся в последующие дни иммунный ответ как бы постоянно отстает, за паздывает и не может адекватно обеспечить санацию организма от инфекции. К тому же процесс формирования иммунного ответа идет уже в неблагоприятных условиях токсического поражения печени и других органов, когда возможности организма ограничены. В результате декомпенсация иммунной системы с фатальным для боль
63

А |
|
|
Б |
В |
|
|
|
|
1-й сигнал |
Т |
В |
М |
Т |
В |
|
||||
М |
|
|
2-й сигнал |
|
|
|
|
||
Рис. 2.2. Схема патогенеза ангиогенного сепсиса, вызванного патогенной микрофлорой. |
||||
А – поступление микробных агентов из интраваскулярного очага инфекции в кровоток; Б – бло |
||||
када имеющихся в крови антител и начало иммунного ответа; В – размножение избытка микро |
||||
организмов в условиях полной блокады антимикробных антител. Т – Т-лимфоцит, М – макро |
||||
фаг, В – В-лимфоцит. |
|
|
|
|
|
А |
|
Б |
В |
Т |
|
|
|
|
|
В |
М |
Т |
В |
М |
|
|||
|
|
|
|
|
Рис. 2.3. Схема патогенеза ангиогенного сепсиса, вызванного условно-патогенной микро- |
||||
флорой. А – поступление условно-патогенных микробных агентов из интраваскулярного оча |
||||
га инфекции в кровоток; Б – слабая стимуляция иммунного ответа вследствие преобладания |
||||
толерогенных свойств микроорганизмов над их иммуногенными свойствами; В – размножение |
||||
избытка микроорганизмов вследствие недостаточной выработки антимикробных антител. Т – |
||||
Т-лимфоцит, М – макрофаг, В – В-лимфоцит. |
|
|||
64
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

ного исходом может наступить довольно быстро. Такой вариант патогенеза свойстве нен в первую очередь ангиогенному сепсису, вызванному патогенной микрофлорой (рис. 2.2). По своей сути он напоминает вариант с истощением факторов противо микробной защиты при массивном инфицировании у больных с обширными гнойнодеструктивными процессами.
Важно заметить, что для возникновения очага внутрисердечной инфекции необхо димо, чтобы поступление возбудителей было относительно растянуто по времени и не приводило бы к шокоподобному состоянию. В этом плане особое внимание должно уделяться санации очагов дремлющей инфекции как возможных источников бактерие мии. А.Б.Шилов и соавт. (1982) показали, что в очаге дремлющей инфекции пато генный стафилококк может сохраняться не менее 100 дней без изменения биологиче ских свойств и антибиотикочувствительности. Следует помнить о том, что в присут ствии инородных тел вирулентность микрофлоры возрастает: например, в присутствии шелковых лигатур патогенность кокковой флоры увеличивается в 1000 раз.
Постоянное или периодическое, но продолжительное и достаточно частое посту пление значительного количества микроорганизмов и продуктов их жизнедеятель ности в кровеносное русло в течение нескольких дней приводит, как правило, снача ла к резкому перенапряжению иммунной системы, а затем и к ее декомпенсации. Развитие сепсиса в данном случае, как уже говорилось, фактически означает истоще ние, срыв компенсации иммунной системы или отдельных ее звеньев.
С другой стороны, возможен еще один механизм развития ангиогенного сепсиса, когда возбудителями его являются представители так называемой условно-патогенной микрофлоры. Чаще всего эти микроорганизмы обитают на кожных покровах и слизи стых оболочках человека. К ним относятся сапрофитные штаммы стафилококка, раз личные виды стрептококка, кишечная флора и др. У подобного рода микроорганизмов ввиду длительного сосуществования в процессе филогенеза с человеком толерогенные свойства преобладают над иммуногенными. В результате организм не способен отве чать на их инвазию мощной выработкой антител и т.п. факторов. И когда такие микро организмы чаще всего в результате различных инвазивных лечебно-диагностических
|
3000 |
|
8 |
|
|
|
|
2500 |
|
7 |
|
|
|
|
|
6 |
|
|
|
|
|
2000 |
|
|
|
|
|
|
титрыIg |
5 |
|
|
|
|
AEStО |
|
|
|
|
||
1500 |
4 |
|
|
|
||
|
|
|
|
|
||
|
1000 |
|
3 |
|
|
|
|
|
2 |
|
|
|
|
|
500 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
А |
0 |
Б |
0 |
Флекснера |
Провачека |
К Vi-антигену |
|
|
|
Зонне |
|||
|
|
Эпидермальный стафилококк |
Золотистый стафилококк |
|
||
Рис. 2.4. Показатели иммунореактивности экспериментальных животных при ангиогенном сепсисе, вызванном патогенным и условно-патогенным штаммами стафилококков. А – анти стрептолизин-О; Б – гетерофильные антитела к микроорганизмам (шигеллам).
65
А
процедур, выполненных без должного соблюдения асептики, получают возможность проникнуть во внутреннюю среду организма больного, минуя барьеры покровных тканей, то они, вследствие своей слабой иммуногенности, также получают определен ную свободу размножения и диссеминации в макроорганизме (рис. 2.3).
Всвязи с тем, что число патогенных факторов у сапрофитной флоры значительно меньше, то это накладывает отпечаток и на клиническое течение заболевания: в этом варианте внутрисердечная инфекция протекает менее бурно.
Положение о меньшей иммуногенности сапрофитных штаммов микроорганизмов подтверждается различиями в показателях иммунореактивности эксперименталь ных животных при ангиогенном сепсисе, вызванном патогенным золотистым (штамм
№209) и «условно-патогенным» белым (эпидермальным) стафилококком (рис. 2.4).
Вразвитии внутрисердечной инфекции, естественно, имеют значение и все факто ры, способствующие ослаблению макроорганизма: тяжелая операционная травма, характер основного заболевания (ревматизм, злокачественные опухоли, лейкозы и т.д.), кахексия, алкоголизм, наркомания, преклонный возраст больных, сопутствую щая патология эндокринной системы (сахарный диабет), а также наличие инород ных тел (клапанные и сосудистые протезы, другие пластические материалы), имму носупрессивная терапия (длительный прием кортикостероидов, цитостатиков, луче вая терапия) и т.д. Однако их влияние, по-видимому, опосредовано через механизмы антиинфекционной защиты организма.
Таким образом, подводя итог, можно сказать, что формулой, определяющей раз витие внутрисердечной инфекции, является:
травма эндокарда + бактериемия + ослабление резистентности организма.
В каждом конкретном случае значимость этих компонентов различна, но общий смысл формулы остается постоянным.
66
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

Энрике Симоне. И у нее было сердце! 1890. Музей изобразительных искусств, Малага, Испания.
Энрико Симоне (Enrique Simonet Lombardo, 1866–1927) – испанский художник, работал в Валенсии, Риме, Марокко, Барселоне, Мадриде. Картина «И у нее было сердце!» (другие названия – «Анатомия сердца», «Вскрытие») является его наиболее известной работой.

|
|
Глава III
Внутрисердечный септический очаг, его особенности и возможности
оперативной санации
P
На клиническом материале практически невозможно проследить истинное раз витие инфекционного процесса в сердце при бактериальном эндокардите, так как операционные находки и материал вскрытий, с одной стороны, отражают длительное консервативное лечение, а с другой, в большинстве случаев являются результатом далеко зашедшего заболевания, когда имеются тяжелые разрушения с обширным и глубоким поражением эндокарда камер сердца, и кроме сложной комплексной их санации для нормализации внутрисердечной гемодинамики необходимо восстанов ление внутрисердечных структур с применением различных искусственных пласти ческих материалов (клапанов, всевозможных заплат и т.д.).
Вместе с тем опыт свидетельствует о целесообразности ранних вмешательств, когда инфекционный процесс еще не вышел за пределы отдельных структур и нет их тяжелых разрушений, когда возможны санирующие вмешательства на сердце с со хранением клапанного аппарата.
Нами в эксперименте изучены закономерности инфекционного поражения эндокар да, распространения его в сердце и характер разрушения внутрисердечных структур. При этом особое внимание было обращено на течение процесса в ранней стадии заболе вания. На основе полученных экспериментальных данных, анализа клинических и сек ционных морфологических исследований изучены возможности санации камер сердца на разной стадии инфекционного процесса с использованием механических приемов и обработки инфицированных тканей различными антисептиками. Также оценены воз можности клапаносохраняющих операций при активном инфекционном эндокардите.
Экспериментальный эндокардит вызывали у беспородных собак разного пола, воз раста и массы тела. Предварительно проводили сенсибилизацию животных подкож ным введением в течение 3 суток взвеси золотистого стафилококка. Взвесь приготав ливали из суточной агаровой культуры золотистого стафилококка на изотоническом растворе хлорида натрия. Мутность взвеси в пробирке доводили до стандарта, после чего приготавливали нужное разведение. Животным вводили по 10 млн/кг культуры.
Через 5 суток после первой подкожной инъекции микробной взвеси животным под наркозом через выделенную на шее левую сонную артерию проводили фторо пластовый катетер в сердце и устанавливали его конец в выходном отделе левого
68
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

желудочка ниже аортального клапана |
|
|
(рис. 3.1). Паруса аортального клапана и |
|
|
эндокард выходного отдела левого желу |
|
|
дочка при этом положении кончика ка |
|
|
тетера подвергаются постоянной меха |
|
|
нической травме. Через 1 сутки с интер |
|
|
валом в 6 часов дважды через катетер |
|
|
в левый желудочек медленно вводили |
|
|
суспензию вирулентного золотистого |
|
|
стафилококка из расчета 30 млн культу |
|
|
ры на 1 кг массы животного. |
|
|
Эксперименты выполнены на 40 жи |
|
|
вотных. У 5 животных через 15–30 ми |
|
|
нут развивался тяжелый септический |
|
|
шок, и они погибли в течение 1–2 часов. |
|
|
У 35 собак развился типичный острый |
|
|
стафилококковый эндокардит, протекав |
|
|
ший по септическому типу. 8 собак по |
Рис. 3.1. Принципиальная схема опыта по |
|
гибли в разные сроки в результате есте |
||
созданию экспериментального инфекцион- |
||
ственного течения и прогрессирования |
||
ного эндокардита. |
септического эндокардита с развитием различных осложнений. Остальных животных выводили из эксперимента в разные
сроки введением миорелаксантов. Анализу подвергнуты результаты 26 опытов, кото рые по продолжительности жизни подопытных животных разделены на три группы: I – 15 суток, II – 30 суток, III – 45 суток.
В стерильных условиях вскрывали грудную клетку и удаляли сердечный органо комплекс, включавший начальный отдел аорты, легочной артерии, полых и легочных вен. Сердце вскрывали на отдельном стерильно оборудованном столике. Тотчас из различных участков левых камер брали материал для бактериологического и гисто логического исследований. В последующем макроскопически оценивали состояние внутрисердечных структур, характер поражения эндокарда и степень распространен ности инфекционного деструктивного процесса. Механически удаляли все поражен ные ткани, тромбы, иссекали клапаны, выскабливали абсцессы. После этого в разных сериях опытов в течение 2 минут обрабатывали камеры сердца одним из следующих антисептиков: спирт 96%-ный, настойка йода 5%-ная, первомур. По завершении са нации вновь производили посев материала для бактериологического контроля. С этой целью в 50 мл глюкозопептонного бульона засевали 5–6 кусочков ткани, взя тых из разных отделов санированной полости сердца.
Кроме изучения эффективности перечисленных антисептиков применительно к санации инфицированных камер сердца необходимо было выяснить и их отрица тельное воздействие на ткани: степень повреждения здорового эндокарда и миокар да. С этой целью проводилось гистологическое исследование тканей сердца, подверг нутых химической санации. Для гистологического исследования препараты фикси ровали в первой жидкости Кайзерлинга с последующим восстановлением цвета. После обычной проводки подготовленный материал заливали в целлоидин. Окраску срезов производили гематоксилин-эозином по ван Гизону.
69
3.1. Морфологические изменения в сердце при экспериментальном инфекционном эндокардите
На препаратах, полученных через 15 суток после заражения животных, макроско пически отмечено тотальное поражение аортального клапана у всех 8 животных. У одной собаки оказался пораженным и митральный клапан. Еще у одной собаки найдено тяжелое поражение стенки восходящей аорты с обширным изъязвлением по ходу катетера и множественными вегетациями на тромботических массах. В этот срок в функциональном отношении клапаны были состоятельны. Однако аорталь ные паруса были резко утолщены вследствие отека и изъязвлены. На аортальной стороне створок имелись наложения массивных, рыхлых инфицированных тромбов и свободные вегетации разной величины. В двух препаратах тромботические массы, фиксированные к створкам клапана, явно сужали устье аорты. Местами на створках
митрального клапана и на пристеночном эндокарде выходного отдела левого же лудочка определялись обширные эро зии, покрытые ровной пленкой фибрина. У одной собаки этой группы при широ кой секции сердца найден большой аб сцесс межжелудочковой перегородки (рис. 3.2).
А |
Тромботические массы, фибринозные |
|
наложения и вегетации относительно |
||
|
||
|
легко снимались при помощи пинцета, |
|
|
влажным тупфером, а также смывались |
|
|
струей раствора из шприца, причем |
|
|
после удаления инфицированных тром |
|
|
бов находившаяся под ними поверхность |
|
|
эндокарда была блестящей, изъязвлен |
|
|
ной, но без признаков поражения и де |
|
Б |
струкции более глубоких слоев. |
|
|
Микроскопически в препаратах этого |
|
|
срока отмечались типичные признаки |
|
|
острого воспаления. В тромботических |
|
|
массах с аортального клапана имелась |
|
|
выраженная клеточная инфильтрация с |
|
|
большим количеством сегментоядерных |
|
|
лейкоцитов, а на поверхности тромбов и |
|
В |
в их средней части обнаруживались ско |
|
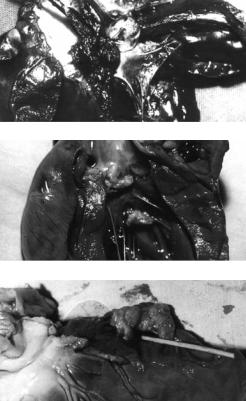
Рис. 3.2. Макропрепарат сердца при 15-су- |
пления микроорганизмов. В структуре |
|
точном сроке экспериментального инфекци- |
самих клапанов был некроз поверхност |
|
онного эндокардита. А – тромбоэндокардит |
ного слоя с выраженной клеточной сег |
|
с поражением митрального, аортального кла |
ментоядерной лейкоцитарной инфиль |
|
панов и стенки восходящей аорты; Б – веге |
||
трацией более глубоких слоев. Бактерий |
||
тации на митральном и аортальном клапанах; |
||
в глубине клапанов ни в одном из пре |
||
В – абсцесс и перфорация межжелудочковой |
||
перегородки. |
паратов этого срока найдено не было. |
|
70 |
|
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
