
- •Введение
- •Обработка результатов физико-химических измерений Погрешность измерений
- •Выражение результатов измерений и расчетов
- •Термохимия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение интегральной теплоты растворения соли и теплоты гидратообразования
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Определение энтальпии диссоциации слабого электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3 Определение изменения энтальпии реакции нейтрализации
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Коллигативные свойства растворов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 4. Криометрия
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в однокомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №5. Давление насыщенного пара
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в двухкомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №6. Получение кривой разгонки
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 7. Получение диаграммы состояния двухкомпонентной неконденсированной системы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Распределение вещества в двухфазной системе. Экстракция Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 9. Экстракция цветных металлов нафтеновой кислотой
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Электропроводность растворов электролитов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 10. Определение степени диссоциации слабого электролита кондуктометрическим способом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №11. Определение чисел переноса ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Термодинамика электрохимических систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 12. Определение стандартных электродных потенциалов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 13. Определение коэффициента активности электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Ионометрия и рН-метрия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 14. Определение константы диссоциации слабого электролита потенциометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Строение вещества. Молекулярные спектры Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 15. Определение константы нестойкости тиоцианата (роданида) железа фотометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Химическая кинетика Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 16. Определение константы скорости реакции окисления иодида калия персульфатом аммония
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 17. Исследование кинетики омыления сложного эфира
- •Молекулярная адсорбция
- •Адсорбция на поверхности раздела жидкость – газ
- •Адсорбция на поверхности твердого тела
- •Ионообменная адсорбция
- •Контрольные вопросы
- •Лабораторная работа № 18. Исследование поверхности раздела фаз: раствор пав - воздух
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Лабораторная работа № 19. Исследование молекулярной адсорбции растворенного вещества из растворов на активированном угле
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 20. Исследование обменной адсорбции ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 21. Исследование кинетики ионообменной адсорбции
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №22. Разделение меди и цинка на катионите
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Устойчивость дисперсных систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 23. Получение лиофобных золей
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 24. Определение порога коагуляции визуальным методом
- •Выполнение работы
- •I. Приблизительное определение порога коагуляции
- •Содержание протокола лабораторной работы
- •II. Уточнение значения порога коагуляции
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 25. Изучение коагуляции гидрозоля железа
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 26. Определение размеров частиц дисперсных систем турбидиметрическим методом Краткие теоретические сведения
- •Контрольные вопросы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Содержание
Содержание протокола лабораторной работы
Наименование электролита и его химическая формула
Концентрация раствора электролита
Зависимость кажущейся оптической плотности золя гидроксида железа от объема добавленного электролита
№ колбы |
Объем электролита VЭ, мл |
Объем воды V(H2O), мл |
Оптическая плотность золя, D |
1 |
0 |
10 |
|
2 |
1,0 |
9,0 |
|
3 |
1,5 |
8,5 |
|
4 |
2,0 |
8,0 |
|
5 |
2,5 |
7,5 |
|
6 |
3,0 |
7,0 |
|
7 |
3,5 |
6,5 |
|
8 |
4,0 |
6,0 |
|
9 |
4,5 |
5,5 |
|
10 |
5,0 |
5,0 |
|
Обработка результатов эксперимента
1. Посторить график зависимости D = f(Vэл) для Na2SO4 или CH3COONa.
2. По графику найти пороговые объемы электролита Vэл, вызывающие быструю коагуляцию золя.
3. Рассчитать значение Скр, называемую порогом коагуляции
,
где СЭЛ – концентрация раствора электролита, применяемого для коагуляции, VЭЛ – наименьший объем раствора электролита, V – суммарный объем коллоидного раствора с электролитом.
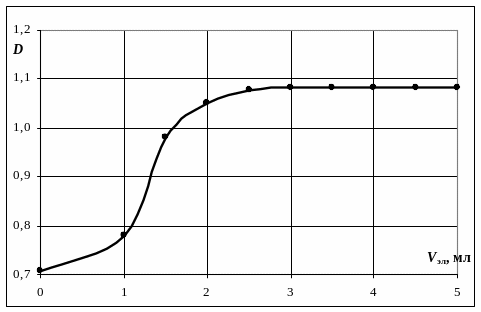
Рис. ___. Обработка графической зависимости D = f(Vэл)
4. Сравнить найденные значения Скр для Na2SO4 и CH3COONa и проверить их соответствие правилу Шульце – Гарди.
![]() .
.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Экспериментальные данные (см. протокол к лабораторной работе).
5. Обработка экспериментальных данных.
6. Вывод.
Лабораторная работа № 26. Определение размеров частиц дисперсных систем турбидиметрическим методом Краткие теоретические сведения
Уравнение Рэлея может быть использовано для определения размеров частиц формы, близкой к сферической, если их радиус R не превышает 0,1 длины волны падающего света. Уравнение Рэлея определяет интенсивность рассеянного света от размера частиц, угла рассеяния и длины волны падающего света:
![]() ,
,
где I0 – интенсивность падающего света, I – интенсивность рассеянного света, С – концентрация частиц в единице объема, V – объем частицы, - длина волны падающего света, r – расстояние частицы от источника света (оптический путь), β – угол рассеяния. F – функция показателей преломления дисперсной и дисперсионной среды:
 ,
,
где n1, n0 – показатели преломления дисперсной и дисперсионных фаз соответственно.
Из уравнения Рэлея радиус частицы равен:
![]() ,
,
где С – концентрация взвешенных частиц, – мутность системы,
![]() .
.
Необходимым условием использования уравнения Релея для дисперсных систем является отсутствие поглощения света, а также минимум вторичного светорассеяния. Поэтому уравнение Рэлея применимо только для «белых» золей, т.е., не поглощающих свет дисперсных систем при очень низких концентрациях дисперсной фазы.
Для дисперсных сред, неудовлетворяющих уравнению Рэлея используют турбидиметрические измерения. Турбидиметрические методы основаны на измерении интенсивности проходящего через дисперсную среду света. Рассеянный свет можно считать фиктивно поглощенным, поэтому для дисперсных сред закон Бугера –Ламберта – Бера связывает мутность среды с кажущейся оптической плотностью:
![]() ,
,
где d
– средний диаметр поглощающих свет
частиц;
![]() и
α – константы, зависящие от метода
измерения и природы суспензии; λ – длина
волны; l – толщина
поглощающего слоя; С – концентрация
определяемого вещества; I0
и I – интенсивность
потока света – падающего и прошедшего
через исследуемый раствор.
и
α – константы, зависящие от метода
измерения и природы суспензии; λ – длина
волны; l – толщина
поглощающего слоя; С – концентрация
определяемого вещества; I0
и I – интенсивность
потока света – падающего и прошедшего
через исследуемый раствор.
При постоянных значениях среднего диаметра частиц d, характера суспензии и α, длине волны λ
![]() или
или
![]() ,
,
где K – молярный коэффициент мутности.
Мутность = I/I0 и оптическая плотность D пропорциональна концентрации и квадрату объема частиц. Это позволяет определять размеры частиц и их концентрацию по кажущейся оптической плотности системы с помощью турбидиметрических измерений.
При увеличении размеров частиц закон Рэлея не выполняется, и интенсивность рассеянного света становится обратно пропорциональной длине волны в степени меньше чем четвертая. В общем случае для поглощающих золей степень при длине волны становится дробной, что делает невозможным использование уравнения Рэлея. Если размер (диаметр) взвешенных частиц составляет от 1/10 до 1/3 длины световой волны и показатели преломления частиц и среды не сильно различаются, то в случае турбидиметрических измерений можно пользоваться эмпирическим уравнением Геллера:
D = k−n и = k’−n,
где k и k’ – константы, не зависящие от длины волны.
Зависимость lgD или lg от lg представляет собой прямую, тангенс угла наклона которой равен –n. Показатель степени связан с длиной волны и размером частиц эмпирическим соотношением:
![]() ,
,
которое табулировано для n < 4 (табл. 1). С увеличением z значение n уменьшается в пределе к 2 для частиц, радиус которых больше длины волны. При малых значениях z показатель степени n стремится к 4 и выполняется уравнение Рэлея.
