
- •Введение
- •Обработка результатов физико-химических измерений Погрешность измерений
- •Выражение результатов измерений и расчетов
- •Термохимия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение интегральной теплоты растворения соли и теплоты гидратообразования
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Определение энтальпии диссоциации слабого электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3 Определение изменения энтальпии реакции нейтрализации
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Коллигативные свойства растворов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 4. Криометрия
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в однокомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №5. Давление насыщенного пара
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в двухкомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №6. Получение кривой разгонки
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 7. Получение диаграммы состояния двухкомпонентной неконденсированной системы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Распределение вещества в двухфазной системе. Экстракция Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 9. Экстракция цветных металлов нафтеновой кислотой
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Электропроводность растворов электролитов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 10. Определение степени диссоциации слабого электролита кондуктометрическим способом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №11. Определение чисел переноса ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Термодинамика электрохимических систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 12. Определение стандартных электродных потенциалов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 13. Определение коэффициента активности электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Ионометрия и рН-метрия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 14. Определение константы диссоциации слабого электролита потенциометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Строение вещества. Молекулярные спектры Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 15. Определение константы нестойкости тиоцианата (роданида) железа фотометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Химическая кинетика Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 16. Определение константы скорости реакции окисления иодида калия персульфатом аммония
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 17. Исследование кинетики омыления сложного эфира
- •Молекулярная адсорбция
- •Адсорбция на поверхности раздела жидкость – газ
- •Адсорбция на поверхности твердого тела
- •Ионообменная адсорбция
- •Контрольные вопросы
- •Лабораторная работа № 18. Исследование поверхности раздела фаз: раствор пав - воздух
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Лабораторная работа № 19. Исследование молекулярной адсорбции растворенного вещества из растворов на активированном угле
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 20. Исследование обменной адсорбции ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 21. Исследование кинетики ионообменной адсорбции
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №22. Разделение меди и цинка на катионите
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Устойчивость дисперсных систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 23. Получение лиофобных золей
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 24. Определение порога коагуляции визуальным методом
- •Выполнение работы
- •I. Приблизительное определение порога коагуляции
- •Содержание протокола лабораторной работы
- •II. Уточнение значения порога коагуляции
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 25. Изучение коагуляции гидрозоля железа
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 26. Определение размеров частиц дисперсных систем турбидиметрическим методом Краткие теоретические сведения
- •Контрольные вопросы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Содержание
Содержание протокола лабораторной работы
Электролит _______________.
Исходная концентрация электролита C0 = ______ н.
Температура Т = ________°С.
Атмосферное давление Ратм = _________ мм рт. ст.
Объем 1 н. раствора серной кислоты в бюретках до начала электролиза
V1 = ________ мл; V2 = ________ мл;
Сила тока __________ А
Продолжительность электролиза _____ мин.
Уровень 1 н. раствора серной кислоты в бюретках по окончании электролиза
V*1 = ________ мл; V*2 = ________ мл;
h1 = ________ мм; h2 = ________ мм
Концентрация титранта (гидроксида натрия)
CT = ________ н.
Объем раствора в катодном пространстве
VK = __________ мл
Объем пробы, взятой для анализа Va,K = ______ мл
Объем титранта
![]() = ________ мл
= ________ мл
![]() = ________ мл.
= ________ мл.
Средний объем титранта
![]() = ______ мл
= ______ мл
Объем раствора в анодном пространстве VА = __________ мл
Объем пробы, взятой для анализа Va,A = ______ мл
Объем титранта
![]() = ________ мл
= ________ мл
![]() = ________ мл.
= ________ мл.
Средний объем титранта
![]() = ______ мл
= ______ мл
Обработка результатов эксперимента
Вычислить равновесную концентрацию электролита в катодном пространстве:
![]() .
.
Вычислить равновесную концентрацию электролита в анодном пространстве:
![]() .
.
Вычислить убыль вещества в катодном пространстве:
![]() ,
моль.
,
моль.
Вычислить прибыль вещества в анодном пространстве:
![]() ,
моль.
,
моль.
Вычислить объем выделившегося
кислорода:
![]() .
.
Рассчитать давление газа в бюретке:
![]() ,
,
где
![]() – давление насыщенного пара воды при
данной температуре, мм рт. ст.; h2/13,6
– гидростатическое давление столба
жидкости в бюретке, мм рт. ст.
– давление насыщенного пара воды при
данной температуре, мм рт. ст.; h2/13,6
– гидростатическое давление столба
жидкости в бюретке, мм рт. ст.
Вычислить количество эквивалентов газа, которое соответствует количеству электричества, прошедшего через раствор, т.к. 1 фарадей электричества переносит 1 эквивалент вещества:
![]() ,
,
где n – согласно закону эквивалентов – количество вещества, разложившееся под действием заданного количества электричества
Давление газа следует перевести в Па (760 мм рт.ст. = 1,013·105Па), объем газа – в м3 (1 мл = 10−6 м3).
Рассчитать число переноса
сульфат-иона:
![]() и катиона водорода:
и катиона водорода:
![]() .
.
Проверить правильность
определения чисел переноса:
![]() .
.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Экспериментальные данные (см. протокол к лабораторной работе).
5. Обработка экспериментальных данных.
6. Вывод.
Термодинамика электрохимических систем Краткие теоретические сведения
К электрохимическим будем относить процессы, сопровождающиеся переносом заряда, образованием двойного электрического слоя (ДЭС) и идущие на поверхности раздела фаз. Такой комплекс процессов, как правило, сопровождается взаимным превращением электрической энергии в химическую в результате протекания окислительно-восстановительных реакций.
Электрохимический потенциал возникает на поверхности раздела фаз электрод – раствор. Причиной образования электродного потенциала является появление на поверхности электрода двойного электрического слоя, который можно сравнить с плоским конденсатором, одной обкладкой которого служит заряженная поверхность металла, а другой – внешняя граница ДЭС. В простейшем случае двойной электрический слой состоит из слоя потенциалопределяющих ионов, расположенных непосредственно на поверхности электрода и слоя противоионов, которые соединены с потенциалопределяющими ионами за счет сил электростатического взаимодействия.
Непосредственно измерить потенциал какой-либо системы пока не представляется возможным. Мы можем измерить только разность потенциалов или электродвижущую силу (ЭДС) гальванической системы, состоящей из пары электродов – электрохимической цепи. С другой стороны, потенциал электрода зависит от температуры и концентрации раствора. В связи с этим было введено понятие стандартного водородного электрода и шкалы стандартных электродных потенциалов. Потенциал стандартного водородного электрода условно принят равным нулю и относительно него считаются потенциалы всех возможных электродных систем, приведенные к единым условиям, получивших название стандартных: температура 298 K и концентрация раствора 1 моль/кг (если речь идет о газовых электродных системах, то давление газа – 1 атм).
Зависимость потенциала электрода
от температуры и состава раствора
относительно значения стандартного
электродного потенциала была выведена
Нернстом для окислительно-восстановительного
процесса, протекающего на поверхности
электрода
![]() :
:
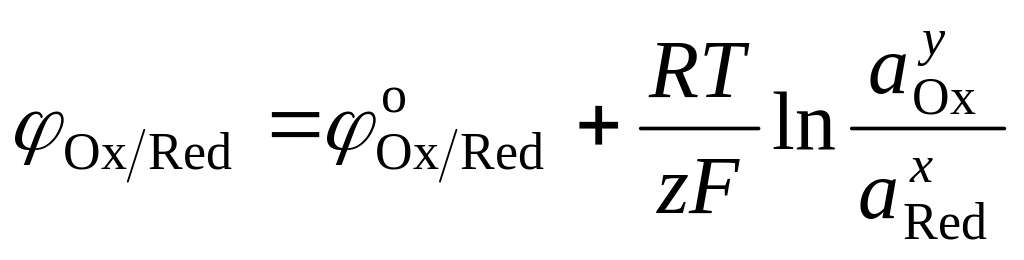 ,
,
где
![]() – электродный потенциал, В;
– электродный потенциал, В;
![]() – стандартный электродный потенциал,
В; R – универсальная газовая
постоянная; Т – температура, K; z
– число электронов, принимающих участие
в электродном процессе; F – постоянная
Фарадея;
– стандартный электродный потенциал,
В; R – универсальная газовая
постоянная; Т – температура, K; z
– число электронов, принимающих участие
в электродном процессе; F – постоянная
Фарадея;
![]() – активность окисленной формы элемента
в растворе;
– активность окисленной формы элемента
в растворе;
![]() – активность восстановленной формы.
– активность восстановленной формы.
При схематической записи
электрохимических систем, а также
уравнений протекающих в них реакций
необходимо соблюдать следующие основные
правила. Для электродов (полуэлементов)
вещества, находящиеся в растворе,
указываются слева от вертикальной
черты, справа указываются вещества,
образующие другую фазу, или электродный
материал. Если одна фаза содержит
несколько веществ, то их символы
разделяются запятыми:
![]() .
.
Уравнение электродной реакции записывается так, чтобы слева располагались вещества в окисленной форме и электроны, а справа вещества в восстановленной форме, например: Cu2+ + 2e = Cu0; 2H+ + 2e = H2; Fe3+ + e = Fe2+.
Принять различать 4 типа электродных систем.
Электроды 1 рода образованы простым веществом (металлом или неметаллом), погруженным в раствор своей соли. Металлическому электроду Меz+|Ме соответствует реакция Меz+ + ze = Me и потенциал электрода описывается уравнением:
![]() .
.
Примерами электрода первого рода могут быть медный электрод Cu2+|Cu (CuSO4|Cu), цинковый электрод Zn2+|Zn (ZnSO4|Zn) и др.
Неметаллическому электроду Az|A соответствует электродная реакция A + ze = Az и потенциал электрода описывается уравнением:
![]() .
.
Потенциал электрода первого рода зависит от активности лишь одного сорта ионов.
Электроды 2 рода состоят из металла, покрытого слоем своей малорастворимой соли и погруженного в раствор, содержащий одноименные с этой солью анионы An−|MeAn, Me. Уравнение Нернста для электрода 2 рода записывается следующим образом:
![]() .
.
Примером электрода второго рода может служить хлорсеребряный электрод, Ag, AgCl|KCl, потенциал которого зависит от содержания ионов Cl в растворе. Хлорсеребряный электрод нередко используют в качестве электрода сравнения при потенциометрических измерениях. В этом случае приэлектродное пространство заполняют насыщенным раствором хлорида калия, что обеспечивает стабильность значения электродного потенциала.
Газовые электроды состоят из инертного металла (Pt), контактирующего с газом и с раствором, содержащим одноименные с газом ионы. Самый известный пример газового электрода – водородный электрод: H+|H2, Pt. Для этого электрода реализуется реакция: H+ + e 1/2H2, для которой уравнение Нернста:
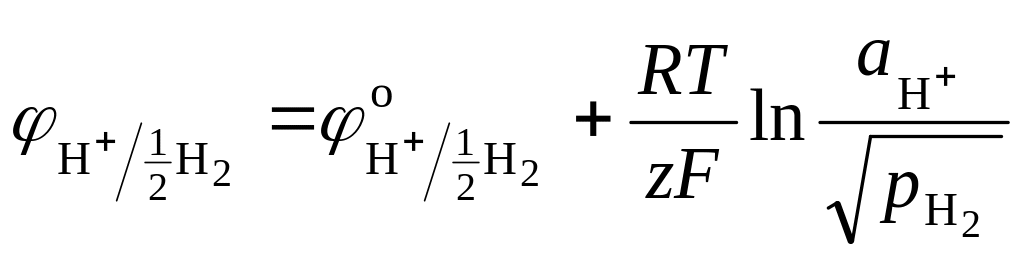 или
или
![]() .
.
Окислительно-восстановительные электроды. Такая система состоит из компонентов, находящихся в растворе. В этом случае индикаторным электродом служит инертный металл (обычно платина или золото), который не принимает участия в реакции, а служит лишь передатчиком электронов между компонентами окислительно-восстановительной системы, поэтому только последние определяют величину потенциала электрода. Примером может служить платина, погруженная в раствор, содержащий Fe2+ и Fe3+. В этом случае на электроде протекает реакция Fe3+ + е = Fe2+, потенциал которой будет определяться уравнением:
![]() .
.
Два электрода, соединенных
друг с другом посредством электролитического
ключа или каким-либо другим проводником,
представляют собой электрохимическую
цепь. Для записи формул цепей существуют
определенные правила. Сева располагается
электрод, имеющий более отрицательный
потенциал (анод), а справа – менее
отрицательный (катод). На катоде идет
процесс восстановления:
![]() ,
на аноде идет процесс окисления:
,
на аноде идет процесс окисления:
![]() .
.
Растворы обоих электродов
отделяются вертикальной пунктирной
линией, если они контактируют друг с
другом:
![]() и двумя сплошными линиями, если между
растворами находятся солевой мостик
и двумя сплошными линиями, если между
растворами находятся солевой мостик
![]() .
.
Электрической характеристикой электрохимической цепи является электродвижущая сила. ЭДС гальванического элемента определяется по формуле:
Е = К – А или Е = ox red,
где К и А – потенциалы катода и анода; ox – электрохимический потенциал «окислителя», более положительного электрода, red – электрохимический потенциал «восстановителя», более отрицательного электрода.
Электрохимическая цепь может быть составлена из разных электродов или из одинаковых электродов. В последнем случае, так как потенциал электрода зависит от концентрации, ЭДС гальванического элемента, составленных из однотипных электродов (один и тот же металл в растворе одной и той же соли) с разными концентрациями растворов, будет отличен от нуля. Такой гальванический элемент называется концентрационным. Анодом в нем является электрод с меньшей концентрацией потенциалопределяющих ионов.
Разность электрохимических потенциалов определяет направление протекания процесса:
G = −zFE,
где G – энергия Гиббса электрохимической реакции, z – число электронов, принимающих участие в окислительно-восстановительном процессе, F – число Фарадея, Е – разность потенциалов.
Приближенно направление электрохимического процесса вообще, можно оценить по значению стандартных электрохимических потенциалов.
Группа методов анализа, основанная на измерении ЭДС электрохимических систем получила название потенциометрический анализ или потенциометрия. Существуют два основных варианта проведения потенциометрического анализа растворов: метод прямой потенциометрии и потенциометрическое титрование.
Метод прямой потенциометрии, помимо установления концентрации определяемого вещества в растворе, позволяет определить такие важные физико-химические величины, как значение стандартного электродного потенциала, средний ионный коэффициент активности электролита, константу диссоциации слабого электролита, растворимость малорастворимого соединения и т.д. Особенно важно, что потенциометрические методы можно применять для изучения процессов в неводных средах. В настоящее время все большее применение получают мембранные электроды, которые представляют собой тонкую мембрану, способную обмениваться с раствором ионами. Вследствие такого обмена на границе «мембрана – раствор» устанавливается потенциал, зависящий от концентрации обмениваемых ионов в растворе.
В качестве электродов сравнения при потенциометрических определениях наиболее часто используют хлорсеребряный или каломельный электроды. Электроды сравнения, если это допустимо, погружают непосредственно в исследуемый раствор или соединяют с ним посредством электролитического мостика – стеклянной U-образной трубки, наполненной электролитом (чаще всего хлоридом или нитратом калия).
