
- •Введение
- •Обработка результатов физико-химических измерений Погрешность измерений
- •Выражение результатов измерений и расчетов
- •Термохимия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение интегральной теплоты растворения соли и теплоты гидратообразования
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Определение энтальпии диссоциации слабого электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3 Определение изменения энтальпии реакции нейтрализации
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Коллигативные свойства растворов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 4. Криометрия
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в однокомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №5. Давление насыщенного пара
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в двухкомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №6. Получение кривой разгонки
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 7. Получение диаграммы состояния двухкомпонентной неконденсированной системы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Распределение вещества в двухфазной системе. Экстракция Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 9. Экстракция цветных металлов нафтеновой кислотой
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Электропроводность растворов электролитов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 10. Определение степени диссоциации слабого электролита кондуктометрическим способом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №11. Определение чисел переноса ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Термодинамика электрохимических систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 12. Определение стандартных электродных потенциалов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 13. Определение коэффициента активности электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Ионометрия и рН-метрия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 14. Определение константы диссоциации слабого электролита потенциометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Строение вещества. Молекулярные спектры Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 15. Определение константы нестойкости тиоцианата (роданида) железа фотометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Химическая кинетика Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 16. Определение константы скорости реакции окисления иодида калия персульфатом аммония
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 17. Исследование кинетики омыления сложного эфира
- •Молекулярная адсорбция
- •Адсорбция на поверхности раздела жидкость – газ
- •Адсорбция на поверхности твердого тела
- •Ионообменная адсорбция
- •Контрольные вопросы
- •Лабораторная работа № 18. Исследование поверхности раздела фаз: раствор пав - воздух
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Лабораторная работа № 19. Исследование молекулярной адсорбции растворенного вещества из растворов на активированном угле
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 20. Исследование обменной адсорбции ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 21. Исследование кинетики ионообменной адсорбции
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №22. Разделение меди и цинка на катионите
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Устойчивость дисперсных систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 23. Получение лиофобных золей
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 24. Определение порога коагуляции визуальным методом
- •Выполнение работы
- •I. Приблизительное определение порога коагуляции
- •Содержание протокола лабораторной работы
- •II. Уточнение значения порога коагуляции
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 25. Изучение коагуляции гидрозоля железа
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 26. Определение размеров частиц дисперсных систем турбидиметрическим методом Краткие теоретические сведения
- •Контрольные вопросы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Содержание
Контрольные вопросы
1. Какими независимыми переменными определяются свойства двухкомпонентных систем?
2. Какие системы называют неконденсированными?
3. Какое основное уравнение описывает гетерогенные фазовые равновесия?
4. Какие показатели двухкомпонентной системы можно определить на основании изучения диаграмм состояния?
5. Что показывают линии ликвидуса и солидуса?
6. Возможно ли разделение компонентов азеотропной смеси методом простой перегонки?
7. Как при помощи диаграммы состояния определить состав равновесных фаз?
8. Для чего применяется правило рычага при расшифровке диаграмм состояния?
9. Какие особенные свойства имеет точка эвтектики?
10. Какие самые распространенные способы построения диаграмм состояния?
11. В чем суть аналитического метода?
12. Каковы основные принципы метода построения диаграммы состояния конденсированной системы на основании изучения кривых охлаждения?
13. Каким законом определяются парциальные давления компонентов при перегонке бинарной смеси?
14. Каким уравнением связано парциальное давление компонента в паровой фазе с общим давлением пара?
15. Каким уравнением определяется отношение парциальных давлений компонентов в паровой фазе?
16. Каким компонентом обогащена паровая фаза при перегонке?
Лабораторная работа №6. Получение кривой разгонки
Цель работы: изучить особенности перегонки двухкомпонентной системы; составить материальный баланс процесса перегонки.
Сущность метода: Дробная (или фракционная) перегонка применяется для выделения в чистом виде компонентов смеси жидкостей, отличающихся по температурам кипения и не образующих друг с другом азеотропных смесей. В зависимости от природы компонентов прибор нагревают на водяных банях, электроплитках или горелкой на асбестовой сетке.
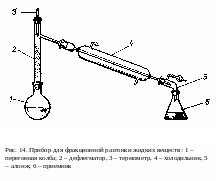
Смесь разгоняют в приборе (рис. 14). После того как прибор собран и установлен, вынимают пробку с термометром из дефлегматора. Вставляют воронку (конец ее трубки должен находиться ниже отвода у дефлегматора) и наливают смесь. На дно колбы помещают «кипелки». Дистиллят должен поступать в приемник со скоростью 30-40 капель в минуту.
В ходе разгонки собирают три фракции: первая фракция – от начала перегонки до момента, когда температура кипения начнет быстро повышаться. Быстрое повышение температуры означает ее подъем на 5 – 7°С в течение 10 – 20 с. Собранную фракцию после измерения ее объема переливают в плоскодонную колбочку. Вторая фракция (промежуточная) собирается во время быстрого повышения температуры отходящих паров. Третья фракция (окончательная) собирается с момента прекращения быстрого роста температуры до конца перегонки.
Перегонку прекращают, когда в перегонной колбе остается 2-3 мл жидкости. Для лучшего разделения смеси веществ проводят вторичную разгонку. В перегонную колбу помещают первую (головную) фракцию и перегоняют ее в прежних температурных пределах. При этом получающаяся фракция обогащается низкокипящим компонентом.
Когда температура отходящих паров достигнет верхней границы первого температурного интервала, перегонку прекращают. Прибор охлаждают. В перегонную колбу добавляют среднюю фракцию от первой перегонки и вновь начинают разгонку, как описано выше. По окончании перегонки средней фракции к остатку приливают третью фракцию и продолжают разгонку, собирая фракции во второй и третий приемники. При многократном повторении разгонки средняя фракция значительно уменьшается, разделяясь на первую и третью фракции. При этом происходит сужение температурных интервалов крайних фракций. Таким способом удается достаточно хорошо разделить смесь компонентов. При прерывании перегонки необходимо каждый раз добавлять новые «кипелки».
Для работы используются системы, в которых оба компонента значительно отличаются по температуре кипения (при наличии азеотропных смесей это не столь существенно) и по показателю преломления. Например: бензол – ацетон; бензол – хлороформ; дихлорэтан – толуол; четыреххлористый углерод – ацетон; ацетон – хлороформ; пропиловый спирт – четыреххлористый углерод; этиловый спирт – вода; четыреххлористый углерод – этиловый спирт; этиловый спирт – бензол. Ниже приведены характеристики перечисленных веществ.
Вещество |
Химическая формула |
Ткипения, °С |
Показатель преломления
|
Плотность, d20 г/см3 |
Бензол |
С6Н6 |
80 |
1,5011 |
0,8790 |
Ацетон |
СН3СОСН3 |
56 |
1,3588 |
0,7905 |
Хлороформ |
СНСl3 |
61 |
1,4449 |
1,489 |
1,2-Дихлорэтан |
CH2ClCH2Cl |
83 |
1,4448 |
1,2570 |
Толуол |
C6H5CH3 |
111 |
1,4969 |
0,8670 |
Четыреххлористый углерод |
CCl4 |
77 |
1,4603 |
1,5940 |
Пропиловый спирт |
CH3CH2CH2OH |
97 |
1,3853 |
0,8040 |
Этиловый спирт |
CH3CH2OH |
78 |
1,3611 |
0,7893 |
Вода |
H2O |
100 |
1,3330 |
0,9982 |
|
|
|
|
|
Оборудование и реактивы. Круглодонная колба объемом 100 мл; дефлегматор длиной 100 мм; насадка Вюрца; холодильник Либиха, длиной 300 мм; алонж; мерный цилиндр объемом 15 – 25 мл – 3 шт.; мерный цилиндр объемом 50 – 100 мл; пробирка – 1 шт.
