
- •Работа 1 растворы. Кислотно-основное титрование
- •Основные теоретические положения
- •Индикаторы кислотно-основного титрования
- •Порядок выполнения работы
- •Часть 1. Определение состава анализируемого раствора методом прямого титрования
- •Экспериментальные и расчетные данные, полученные по методу прямого титрования
- •Часть 2. Определение состава анализируемого раствора методом потенциометрического титрования
- •Экспериментальные и расчетные данные, полученные методом потенциометрического титрования
- •Изменение рН анализируемого раствора от объема титранта
- •Часть 1. Определение состава анализируемого раствора методом прямого титрования
- •Часть 2. Определение состава анализируемого раствора методом потенциометрического титрования.
- •Контрольные задания Вариант 1
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 2 произведение растворимости
- •Основные теоретические положения
- •Порядок выполнения работы
- •Контрольные задания
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 3 гидролиз солей
- •Основные теоретические положения
- •Порядок выполнения работы
- •Часть 1. Определение среды растворов различных солей
- •Часть 2. Смещение гидролитических равновесий
- •Экспериментальные и расчетные данные
- •Экспериментальные и расчетные данные
- •Часть 1. Определение среды растворов различных солей
- •Часть 2. Смещение гидролитических равновесий
- •Контрольные задания
- •Комплексные соединения
- •Основные теоретические положения
- •Порядок выполнения работы
- •Контрольные задания Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Определение жесткости воды
- •Основные теоретические положения
- •Порядок выполнения работы
- •Часть 1. Определение временной жесткости воды
- •Определение временной жесткости воды
- •Часть 2. Определение общей жесткости воды
- •Определение общей жесткости воды
- •Часть 1. Определение временной жесткости воды
- •Часть 2. Определение общей жесткости воды
- •Часть 3. Определение постоянной жесткости воды
- •Определение жесткости воды
- •Контрольные задания
- •Третьяков ю.Д. Практикум по неорганической химии: Учеб. Пособие. – м.: Академия, 2004.
- •Приложение 1 Метрологическая карта средств измерения
- •Приложение 2 Значения произведения растворимости труднорастворимых в воде веществ при температуре 25 °с
- •Приложение 3 Константы диссоциации воды
- •Приложение 4 Константы диссоциации некоторых электролитов в водных растворах (при температуре 25 °с)
- •Часть 2
- •162600, Г. Череповец, пр. Луначарского, 5
Часть 1. Определение временной жесткости воды
1.
Найти средний объем титранта
![]() ,
см3,
израсходованный на титрование, по
формуле
,
см3,
израсходованный на титрование, по
формуле
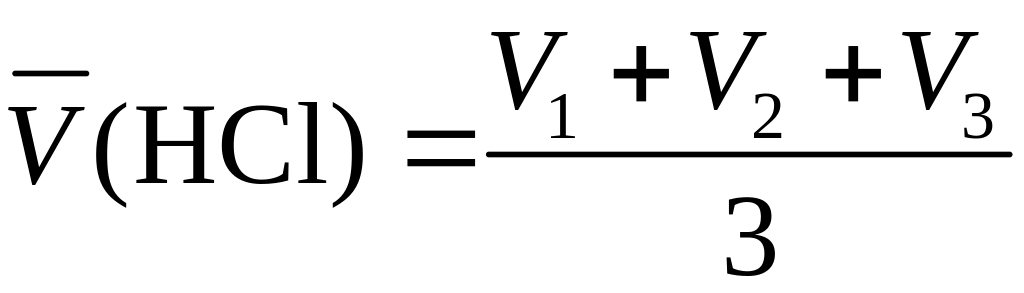 .
.
2. Временную жесткость Ж, ммоль/дм3, рассчитать по формуле
Жвр
=
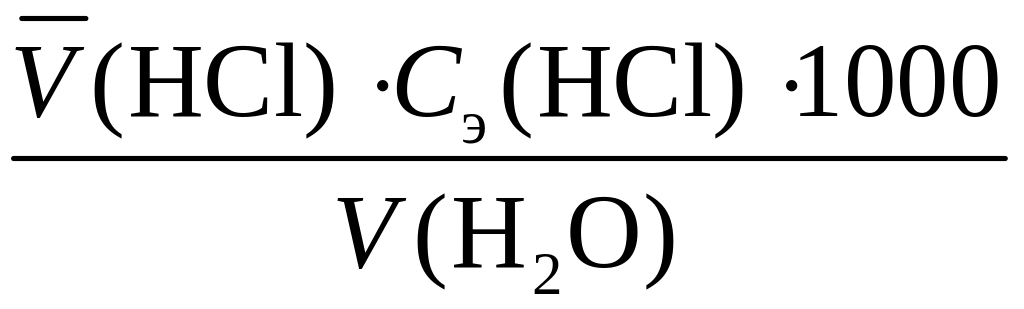 ,
,
где
![]() – объем
воды, взятый для анализа, см3.
– объем
воды, взятый для анализа, см3.
3. Результаты расчетов занести в табл. 6.
Часть 2. Определение общей жесткости воды
1.
Найти средний объем титранта
![]() ,
см3,
израсходованный на титрование, по
формуле
,
см3,
израсходованный на титрование, по
формуле
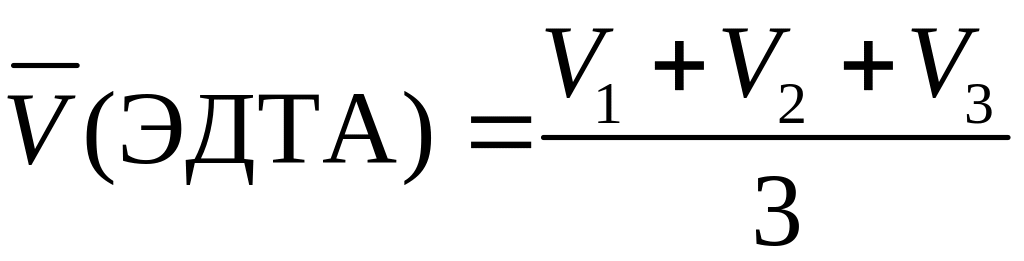 .
.
2. Рассчитать общую жесткость Жвр, ммоль/дм3, по формуле
Жвр
=
 .
.
3. Результаты расчетов занести в табл. 8.
Часть 3. Определение постоянной жесткости воды
1. Постоянную жесткость Жпост, ммоль/дм3, рассчитать по формуле
Жпост = Жобщ – Жвр.
2. Результаты расчетов занести в табл. 9.
3. Анализируемую воду классифицировать по величине жесткости.
4. Оформить метрологическую карту средств измерения и сформулировать выводы.
Таблица 9
Определение жесткости воды
Анализируемая вода |
Жвр, ммоль/дм3 |
Жобщ, ммоль/дм3 |
Жпост, ммоль/дм3 |
Классификация воды |
|
|
|
|
|
Контрольные задания
Вариант 1
1. Какие реагенты устраняют жесткость воды: а) гидроксид натрия; б) карбонат натрия; в) фосфат калия; г) хлорид натрия? Написать соответствующие уравнения реакций.
2. Сколько граммов гидроксида кальция надо добавить к 1000 л воды, чтобы удалить временную жесткость, равную 2,86 мэкв/л?
Вариант 2
1. Какая вода содержит минимальное количество растворенных солей жесткости: а) кипяченая; б) водопроводная; в) дождевая; г) морская; д) дистиллированная?
2. Вычислить временную жесткость воды, если на реакцию с гидрокарбонатом кальция, содержащимся в 100 мл этой воды, потребовалось 5 мл 0,1 н раствора соляной кислоты?
Вариант 3
1. Какие соли, присутствующие в воде, увеличивают расход мыла: а) сульфат натрия; б) сульфат магния; в) сульфат железа (II); г) сульфат кальция; д) гидрокарбонат калия?
2. Рассчитать общую жесткость воды, которая содержит гидрокарбонат кальция (16,2 мг), гидрокарбонат магния (2,92 мг) и хлорид кальция (11,1 мг) в 150 мл воды?
Вариант 4
1. Присутствие каких солей в воде придает ей некарбонатную жесткость: а) хлорида магния; б) гидрокарбоната кальция; в) хлорида кальция; г) гидрокарбоната калия; д) хлорида железа (III); е) сульфата магния; ж) сульфата кальция?
2. Сколько граммов карбоната кальция надо добавить к 5 л воды, чтобы устранить общую жесткость, равную 4,6 мэкв/л?
Вариант 5
1. Добавление каких
ионов к воде обеспечивает ее умягчение:
а) CO![]() ;
б) NO
;
б) NO![]() ;
в) Cl–;
г) PO
;
в) Cl–;
г) PO![]() ?
Написать соответствующие уравнения
реакций.
?
Написать соответствующие уравнения
реакций.
2. При кипячении 250 мл воды, содержащей гидрокарбонат кальция, выпал осадок массой 3,5 мг. Чему равна жесткость воды?
Вариант 6
1. Присутствие каких солей в воде придает ей карбонатную жесткость: а) гидрокарбоната кальция; б) гидрокарбоната магния; в) карбоната кальция; г) гидрокарбоната бария?
2. Рассчитать общую жесткость воды, которая содержит гидрокарбонат кальция (48,6 мг) и сульфат магния (29,6 мг) в 1 л воды?
Вариант 7
1. Присутствие каких ионов в воде обуславливает ее жесткость: а) Са2+; б) Mg2+; в) Fe2+; г) Na+; д) К+; е) Fe3+; ж) Аl3+?
2. Чему равна временная жесткость воды, в 0,5 л которой содержится 0,073 г гидрокарбоната магния?
Вариант 8
1. Какие химические реакции происходят при добавлении к жесткой воде карбоната натрия? Рассмотреть случаи постоянной и временной жесткости.
2. Рассчитать общую жесткость воды, содержащей гидрокарбонат магния (65,7 г) и сульфат кальция (61,2 г) в 600 л воды?
Вариант 9
1. Какие химические реакции происходят при добавлении к жесткой воде гидроксида кальция? Рассмотреть случаи постоянной и временной жесткостей.
2. Жесткость воды, содержащей только гидрокарбонат кальция, равна 1,785 мэкв/л. Определить массу соли в 5 л воды.
Вариант 10
1. Какие химические реакции происходят при добавлении к жесткой воде гидроксида натрия? Рассмотреть случаи постоянной и временной жесткостей.
2. Рассчитать общую жесткость воды, содержащей гидрокарбонат кальция (1,62 г), хлорид магния (9,8 г) и сульфат кальция (6,12 г) в 25 л воды?
Вариант 11
1. Почему опасно для здоровья человека употребление жесткой воды?
2. Рассчитать общую жесткость воды, содержащей сульфат магния (38,0 мг), гидрокарбонат магния (29,2 мг) и хлорид кальция (22,2 мг) в 10 л воды?
Вариант 12
1. Какие химические реакции происходят при добавлении к жесткой воде фосфата натрия? Рассмотреть случаи постоянной и временной жесткостей.
2. Рассчитать общую жесткость воды, содержащей гидрокарбонат железа (II) (4,58 мг), хлорид магния (16,40 мг) и хлорид кальция (2,36 мг) в 5 л воды?
Вариант 13
1. Написать уравнения реакций, объясняющих появление накипи в нагревательных сосудах при кипячении воды. Какие вещества входят в состав накипи?
2. Рассчитать общую жесткость воды, содержащей сульфат кальция (2,44 г), сульфат магния (8,76 г) и хлорид кальция (2,86 г) в 10 л воды?
Вариант 14
1. Присутствие каких солей в воде обуславливает ее жесткость? Указать виды жесткости воды.
2. Рассчитать общую жесткость воды, содержащей гидрокарбонат кальция (2,12 г), гидрокарбонат магния (1,06 г) и сульфат магния (0,086 г) в 3 л воды?
Вариант 15
1. Почему после кипячения водопроводной воды ее жесткость понижается? Написать соответствующие уравнения реакций.
2. Рассчитать общую жесткость воды, содержащей гидрокарбонат кальция (46,0 г), сульфат кальция (86,0 г) и хлорид кальция (120,00 г) в 1 м3 воды?
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
