
- •Работа 1 растворы. Кислотно-основное титрование
- •Основные теоретические положения
- •Индикаторы кислотно-основного титрования
- •Порядок выполнения работы
- •Часть 1. Определение состава анализируемого раствора методом прямого титрования
- •Экспериментальные и расчетные данные, полученные по методу прямого титрования
- •Часть 2. Определение состава анализируемого раствора методом потенциометрического титрования
- •Экспериментальные и расчетные данные, полученные методом потенциометрического титрования
- •Изменение рН анализируемого раствора от объема титранта
- •Часть 1. Определение состава анализируемого раствора методом прямого титрования
- •Часть 2. Определение состава анализируемого раствора методом потенциометрического титрования.
- •Контрольные задания Вариант 1
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 2 произведение растворимости
- •Основные теоретические положения
- •Порядок выполнения работы
- •Контрольные задания
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 3 гидролиз солей
- •Основные теоретические положения
- •Порядок выполнения работы
- •Часть 1. Определение среды растворов различных солей
- •Часть 2. Смещение гидролитических равновесий
- •Экспериментальные и расчетные данные
- •Экспериментальные и расчетные данные
- •Часть 1. Определение среды растворов различных солей
- •Часть 2. Смещение гидролитических равновесий
- •Контрольные задания
- •Комплексные соединения
- •Основные теоретические положения
- •Порядок выполнения работы
- •Контрольные задания Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Определение жесткости воды
- •Основные теоретические положения
- •Порядок выполнения работы
- •Часть 1. Определение временной жесткости воды
- •Определение временной жесткости воды
- •Часть 2. Определение общей жесткости воды
- •Определение общей жесткости воды
- •Часть 1. Определение временной жесткости воды
- •Часть 2. Определение общей жесткости воды
- •Часть 3. Определение постоянной жесткости воды
- •Определение жесткости воды
- •Контрольные задания
- •Третьяков ю.Д. Практикум по неорганической химии: Учеб. Пособие. – м.: Академия, 2004.
- •Приложение 1 Метрологическая карта средств измерения
- •Приложение 2 Значения произведения растворимости труднорастворимых в воде веществ при температуре 25 °с
- •Приложение 3 Константы диссоциации воды
- •Приложение 4 Константы диссоциации некоторых электролитов в водных растворах (при температуре 25 °с)
- •Часть 2
- •162600, Г. Череповец, пр. Луначарского, 5
Комплексные соединения
Цель работы: формирование теоретических представлений и практических навыков о свойствах и методах получения комплексных соединений.
Основные теоретические положения
Комплексные соединения (иначе соединения высшего порядка) образуются при взаимодействии друг с другом простых соединений, то есть соединений первого порядка. Например:
CuCl2 + 4NH3 = [Cu(NH3)4]Cl2.
Основу комплексного соединения составляют центральный атом (или ион), называемый комплексообразователем, и частицы (ионы или молекулы), располагающиеся вокруг комплексообразователя, которые называются лигандами. Комплексообразователь и лиганды образуют внутреннюю сферу комплексного соединения. Ионы, нейтрализующие суммарный заряд частиц внутренней сферы и располагающиеся более отдаленно от комплексообразователя, называются внешней сферой. При написании формулы комплексного соединения внутреннюю сферу отделяют от внешней квадратными скобками. Например:
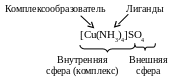
Общее число связей, возникающих между комплексообразователем и его лигандами, называется координационным числом (КЧ) или координационной дентатностью комплексообразователя. Наиболее характерное значение координационного числа можно оценить по формуле
КЧ ≈ 2 · Zк ,
где Zк – степень окисления комплексообразователя (иначе заряд иона).
Координационное число не является постоянной величиной данного комплексообразователя, а обусловлено также природой лиганда. Нейтральные лиганды обычно присоединяются в большем количестве, чем заряженные. Например, для комплексов кобальта (II) известно существование ионов [Co(H2O)6]2+ и [CoCl4]2–.
По числу связей, образованных с центральным атомом, различают:
1) монодентатные лиганды – образуют одну связь и занимают одно место в координационной сфере комплексообразователя. В этом случае координационное число совпадает с числом лигандов во внутренней сфере. К таким лигандам относятся Н2О, NH3, CO, Cl–, CN– и др.
Например, в ионах [Fe(CN)6]3– и [Cu(NH3)4]2+ координационные числа равны 6 и 4 соответственно;
2)
бидентатные
лиганды. Они связаны с комплексообразователем
двумя связями. В этом случае координационное
число в два раза больше числа лигандов.
К таким лигандам относятся молекулы
гидразина, аминоуксусной кислоты,
этилендиамина, а также ионы С2О![]() ,
SO
,
CO
,
SO
,
CO![]() .
.
Например, оксалат-ион – бидентатный, образует с ионом Cu2+ соединение K2[Cu(C2O4)2], в котором координационное число комплексообразователя равно 4. Следует помнить, что в зависимости от условий лиганды SO и CO могут быть как монодентатными, так и бидентатными;
3) полидентатные лиганды. Они занимают в координационной сфере более двух мест, т.е. соединены с комплексообразователем тремя или более связями. Например, этилендиаминтетраацетат (ЭДТА) – шестидентатный лиганд.
При определении заряда комплекса необходимо учитывать следующее:
1) если лигандами являются только нейтральные молекулы, то заряд комплекса равен заряду центрального иона;
2) если во внутреннюю сферу входят как ионы, так и молекулы, то заряд комплексного иона равен алгебраической сумме зарядов комплексообразователя и лигандов с учетом их количества.
Например,
для определения заряда иона [Cr3+(H2O)![]() Cl–]x
следует решить уравнение
Cl–]x
следует решить уравнение
x = 1 (+3) + 5 0 + 1 (–1) = +2.
Номенклатура комплексных соединений
Образование названий комплексных соединений осуществляется по следующим правилам:
1. Порядок перечисления частиц. Если соединение является комплексной солью, то его название будет состоять из двух слов: сначала называется анион в именительном падеже, а затем катион в родительном падеже.
Если внутренняя сфера – катион, то для названия комплексообразователя используют русский корень элемента, а если внутренняя сфера – анион, то в названии применяют латинский корень. Степень окисления комплексообразователя указывается в скобках римской или арабской цифрой.
У нейтральных комплексов (без внешней сферы) название состоит из одного слова в именительном падеже с использованием русского корня комплексообразователя, при этом его степень окисления не указывается.
При названии комплексного иона сначала указываются лиганды, затем комплексообразователь. Перечисление лигандов ведут в следующем порядке: сначала анионы – ОН–, одноатомные, полиатомные; затем нейтральные лиганды (сначала неорганические, затем органические); далее катионы в любом порядке.
Записанная формула читается справа налево. При составлении формулы по ее названию в квадратных скобках сначала записывают комплексообразователь, а затем лиганды в обратном порядке их перечисления. Например:
K3[Fe(CN)6] – гексацианоферрат (III) калия;
[Pt(NH3)6]Cl4 – хлорид гексаамминплатины (IV);
[Pt(NH3)2Cl4] – тетрахлородиамминплатина;
2. Названия лигандов. Для нейтральных лигандов используют однословные названия веществ без изменений. Например: N2 – диазот, N2H4 – гидразин, C2H4 – этилен. Для молекул Н2О, NH3, СО, NO применяют особые термины: аква, аммин, карбонил, нитрозил соответственно.
К
названиям анионных лигандов прибавляют
соединительную гласную «о». Например:
Cl–
– хлоро, SO
– сульфато, О2–
– оксо, S2–
– тио, ОН–
– гидроксо, CN–
– циано, NСS–
– тиоцианато, Н–
– гидридо, NO![]() – нитро, NO
– нитро, NO![]() –
нитрато и т.д. Исключение составляют
анионы углеводородов, например, С5Н
–
нитрато и т.д. Исключение составляют
анионы углеводородов, например, С5Н![]() – циклопентадиенил.
– циклопентадиенил.
Громоздкие по написанию формулы органических лигандов заменяют буквенными обозначениями: NH2CH2CH2NH2 (этилендиамин) – Еn; C5H5N (пиридин) – py; (NH2)2CO (карбамид) – ur; NH2CH2COO– (глицинат-ион) – gly.
3. Приставки и окончания. Число простых лигандов указывают с помощью приставок греческих числительных: ди – 2, три – 3, тетра – 4, пента – 5, гекса – 6, гепта – 7, окта – 8, нона – 9, дека – 10, ундека – 11, додека – 12.
Для лигандов со сложными названиями, в которых уже имеются приставки (моно-, ди- и т.д.), используют приставки бис – 2, трис – 3, тетракис – 4, а названия таких лигандов заключаются в круглые скобки.
Для названия анионных комплексов применяют окончания: –ат, если комплексное соединение относится к классу солей; –овая или –ная, если комплексное соединение является кислотой. Для катионных и нейтральных комплексов типичных окончаний нет.
Например:
[Fe(Еn)3]Cl3 – хлорид трис(этилендиамин)железа (+3);
[Pt(Еn)(NH3)2(NO2)Cl]SO4 – сульфат хлоронитродиамминэтилендиаминплатины (IV);
H2[SiF6] – гексафторокремниевая кислота.
Классификация комплексных соединений
Комплексные соединения очень разнообразны по строению и свойствам, поэтому применяющиеся системы классификации основываются на различных принципах:
1. По принадлежности к определенному классу химических соединений различают: комплексные кислоты (например, Н[AuCl4]); комплексные основания ([Cu(NH3)4](OH)2); комплексные соли (K4[Fe(CN)6]).
2. По природе лигандов: аквакомплексы (лиганды – молекулы воды, например [Co(Н2О)4](NO3)2); аммиакаты (лиганды – молекулы аммиака, [Ag(NH3)2]Cl); ацидокомплексы (лиганды – анионы кислот, Na3[AlF6]); гидроксокомплексы (лиганды – гидроксогруппы, K3[Al(OH)6]); смешанного типа (содержатся лиганды нескольких видов, [Co(NH3)4Cl2]).
3. По знаку заряда комплекса: катионные – [Zn(NH3)4]2+Cl ; анионные – Li+[AlH4]– ; нейтральные (без внешней сферы) – [Pt(NH3)2Cl2]0; бикомплексы – [Co(NH3)6][Fe(CN)6].
Равновесия в растворах комплексных соединений
При растворении в воде комплексные соединения, имеющие внешнюю сферу, диссоциируют как сильные электролиты с образованием комплексного иона, состоящего из частиц внутренней сферы, и ионов внешней сферы. Этот процесс называется первичной диссоциацией.
Например:
К4[Fe(CN)6] 4К+ + [Fe(CN)6]4–.
Наряду с этим процессом, как правило, протекает обратимая ступенчатая диссоциация внутренней сферы, которую называют вторичной диссоциацией. Так, для иона [Fe(CN)6]4– этот процесс идет по следующим ступеням:
первая ступень [Fe(CN)6]4– ↔ CN– + [Fe(CN)5]3–;
вторая ступень [Fe(CN)5]3– ↔ CN– + [Fe(CN)4]2– и т.д.
Количественной характеристикой прочности комплексного иона в растворе является константа равновесия процесса вторичной диссоциации, которую называют константой нестойкости Kнест. Например, для иона [Fe(CN)6]4– константы нестойкости первой и второй ступеней выражаются уравнениями:
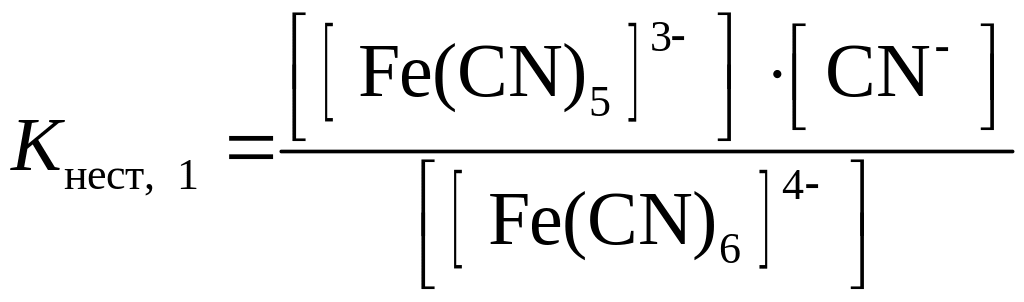 ;
;
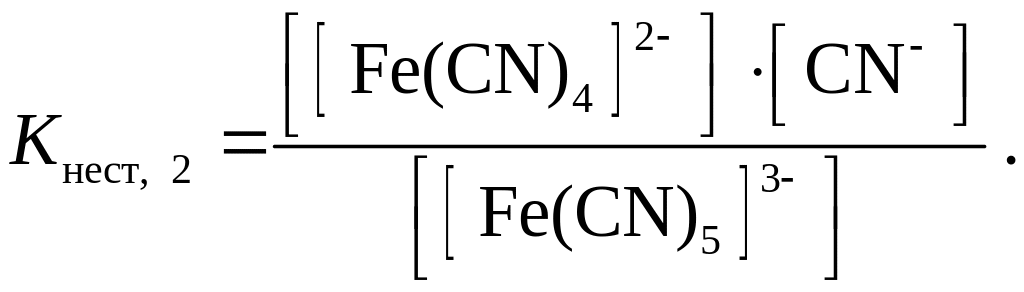
На практике чаще пользуются величиной общей константы нестойкости Kнест, которая характеризует суммарное равновесие вторичной диссоциации. Например, для иона [Fe(CN)6]4–
[Fe(CN)6]4–
↔ 6CN–
+ Fe2+,
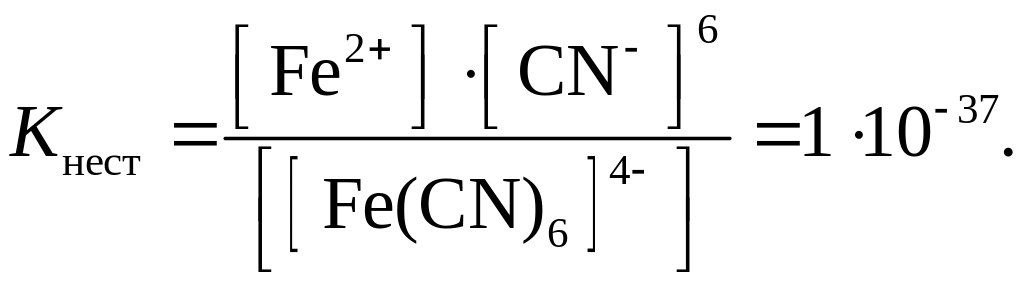
Общая Kнест равна произведению констант нестойкости всех ступеней:
Kнест = Kнест, 1 · Kнест, 2 · Kнест, 3 ·... · Kнест, n.
Иногда вместо Kнест пользуются обратной величиной – константой устойчивости Kуст:
Kнест = 1/Kуст.
Если комплексы имеют одинаковое число лигандов, то их устойчивость можно определить по общей константе нестойкости: чем меньше Kнест, тем более устойчив комплексный ион.
Сопоставление Kнест комплексов для реагента и для продукта (при постоянном значении координационного числа) позволяет установить направление смещения равновесия реакции обмена лигандами в растворе. Например, для процесса
K2[PtCl4] + 4KI ↔ K2[PtI4] + 4KCl,
сравнив Kнест ионов [PtCl4]2– и [PtI4]2–, которые равны 1 10-16 и 1 10-31 соответственно, видно, что комплексный ион-продукт намного устойчивее комплекса-реагента. Следовательно, равновесие такого процесса сильно сдвинуто вправо, то есть данная реакция протекает в прямом направлении.
