- •Содержание
- •1. Введение.
- •1.1 Общие закономерности химических процессов. Классификация процессов общей химико-технологических процессов
- •Требования к химическим производствам
- •Компоненты химического производства
- •Разделение на две твердые фазы:
- •Разделение жидкости и твердого вещества:
- •1.2 Промышленный катализ
- •Основные положения теории катализа.
- •1.3. Сырьевая база химической промышленности.
- •Классификация сырья
- •Характеристика минерального сырья
- •Химическое сырье
- •Растительное и животное сырье
- •Характеристика разработок минерального сырья
- •Качество сырья и методы его обработки
- •Способы сортировки:
- •Способы обогащения:
- •Сырьевая база химических производств
- •1.4 Энергетическая база химических производств
- •1.5 Критерии оценки эффективности производства
- •1.5.1. Интегральные уравнения баланса материальных потоков в технологических процессах. Понятие о расходных коэффициентах. Относительный выход продукта
- •1.5.2. Балансы производства
- •1. Материальный баланс
- •2. Энергетический (тепловой) баланс
- •3. Экономический баланс
- •1.5.3. Технологические параметры химико-технологических процессов.
- •1.6.Принципы создания ресурсосберегающих технологий
- •2. Теоретические основы химической технологии
- •2.1. Энергия в химическом производстве. Тепловой эффект реакции в технологических расчетах. Направленность реакции в технологических расчетах
- •2.2 Массообменные процессы. Основные принципы массообменных процессов. Моделирование процессов теплообмена.
- •Молекулярная диффузия. Первый закон Фика
- •Турбулентная диффузия
- •Уравнение массоотдачи
- •Уравнение массопередачи
- •Связь коэффициента массопередачи и коэффициентов массоотдачи (или уравнение аддитивности фазовых сопротивлений)
- •Подобие массобменных процессов
- •3. Химическое производство как сложная система. Иерархическая организация процессов в химическом производстве
- •3.1. Химико-технологические системы (хтс). Элементы хтс. Структура и описание хтс. Методология исследования хтс, синтез и анализ хтс.
- •Методология исследование химико-технологических систем.
- •3.2. Сырьевая и энергетическая подсистема хтс
- •1. Классификация химических реакторов по гидродинамической обстановке.
- •2. Классификация химических реакторов по условиям теплообмена.
- •3. Классификация химических реакторов по фазовому составу реакционной массы.
- •4. Классификация по способу организации процесса.
- •5. Классификация по характеру изменения параметров процесса во времени.
- •6. Классификация по конструктивным характеристикам.
- •3.4. Промышленные химические реакторы. Реакторы для гомогенных процессов, гетерогенных процессов с твердой фазой, гетерогенно-каталитических процессов, гетерофазных процессов.
- •Реакторы для гетерогенных процессов с твердой фазой.
- •Реакторы для гетерогенно-каталитических процессов.
- •4. Основные математические модели процессов в химических реакторах
- •4.1. Идеальные химические реакторы. Непрерывный реактор идеального вытеснения. Непрерывный реактор идеального смешения
- •4.2. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения. Обоснование использования каскада реакторов.
- •Каскад реакторов смешения.
- •Влияние степени конверсии.
- •Влияние температуры.
- •5. Применение кинетических моделей для выбора и оптимизации условий проведения процессов
- •5.1. Экономические критерии оптимизации и их применение для оптимизации реакционных узлов.
- •Оптимальные концентрации инициатора и температуры в радикально-цепных реакциях
- •Оптимизация степени конверсии.
- •7. Важнейшие промышленные химические производства
- •7.1 Проблема фиксации атмосферного азота. Синтез аммиака, Физико-химические основы производства и обоснование выбора параметров и типа реакционного узла. Технологическая схема процесса.
- •Синтез аммиака
- •Сырье для синтеза аммиака.
- •Технология процесса.
- •Основные направления в развитии производства аммиака.
- •7.2. Получение азотной кислоты. Физико-химические основы химических стадий процесса, обоснование выбора параметров и типа реакторов. Технологическая схема процесса.
- •Физико-химические основы процесса.
- •Контактное окисление аммиака.
- •Обоснование роли параметров и их выбор.
- •Окисление оксида азота (II) до диоксида.
- •Абсорбция диоксида азота.
- •Технология процесса.
- •7.3. Производство минеральных удобрений. Классификация минеральных удобрений
- •Классификация минеральных удобрений.
- •7.3.1. Азотные удобрения. Физико-химические основы производства нитрата аммония. Устройство реакционного узла. Теоретические основы процесса и его технологическое оформление
- •Производство нитрата аммония.
- •7.3.2. Производство фосфорной кислоты. Физико-химические основы процесса. Технологическая схема
- •Функциональная схема производства эфк.
- •Сернокислотное разложение апатита.
- •7.3.3. Фосфорные удобрения. Физико-химические основы процессов их производства. Типы реакционных узлов.
- •Производство простого суперфосфата.
- •Производство двойного суперфосфата
- •Азотнокислое разложение фосфатов. Получение сложных удобрений
- •Обжиг серосодержащего сырья.
- •Обоснование роли параметров и их выбор.
- •Сжигание серы.
- •Окисление диоксида серы.
- •Обоснование роли параметров и их выбор.
- •Технология контактного окисления so2.
- •Абсорбция триоксида серы.
- •Перспективы развития сернокислотных производств.
- •7.5. Электрохимические производства. Теоретические основы электролиза водных растворов и расплавленных сред. Технология электролиза раствора хлорида натрия.
- •Основные направления применения электрохимических производств
- •Электролиз раствора хлорида натрия
- •Электролиз раствора NaCl с твердым катодом и фильтрующей диафрагмой
- •Электролиз раствора хлорида натрия с ртутным катодом
- •7.6. Промышленный органический синтез
- •Первичная переработка нефти.
- •Каталитический риформинг углеводородов.
- •7.6.2. Производство этилбензола и диэтилбензола. Теоретические основы процесса и обоснование выбора условий процесса. Технология процесса
- •7.6.3. Синтезы на основе оксида углерода. Производство метанола. Теоретические основы процесса.
- •Окисление изопропилбензола (кумола)
- •Технологическая схема получения фенола и ацетона кумольным способом.
- •7.6.5. Биохимические производства. Особенности процессов биотехнологии.
- •7.6.5.1. Производство уксусной кислоты микробиологическим синтезом
- •7.6.5.2. Производство пищевых белков
- •8. Химико-технологические методы защиты окружающей среды
- •8.1. Утилизация и обезвреживание твердых отходов
- •8.2. Утилизация и обезвреживание жидких отходов
- •8.3. Обезвреживание газообразных отходов
Окисление изопропилбензола (кумола)
Окисление изопропилбензола представляет собой типичный свободно-радикальный процесс с вырожденным разветвлением цепей. В отсутствие каких-либо посторонних инициирующих агентов зарождение цепей осуществляется посредством бимолекулярного взаимодействия молекул кислорода и изопропилбензола

Эта реакция характеризуется высоким энергетическим барьером и протекает крайне медленно. Низкая скорость инициирования не может обеспечить концентрацию свободных радикалов на уровне, вызывающем заметное протекание цепного процесса.
Поскольку гидропероксид изопропилбензола легко распадается по слабой кислород-кислородной связи
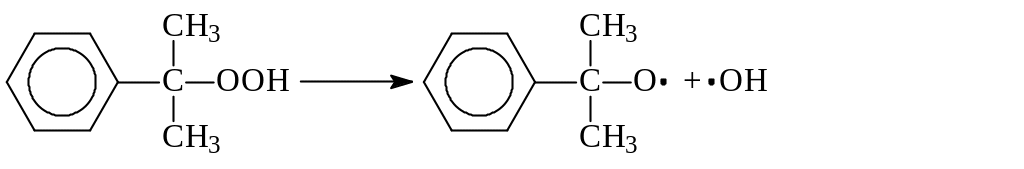
его накопление в ходе процесса приводит к лавинообразному увеличению скорости генерирования свободных радикалов, а значит, и скорости окисления изопропилбензола. Такой характер процесса обусловливает наличие некоторого индукционного периода реакции, который можно определить как время, в течение которого в системе накапливается количество гидропероксида, обеспечивающее заметное протекание цепного процесса. В связи с этим естественным способом сокращения индукционного периода является добавление в исходный изопропилбензол некоторое количество гидропероксида или окисленной реакционной массы.
Индукционный период процесса может быть значительно больше по причине присутствия в реакционной массе ингибиторов свободно-радикального окисления таких как серосодержащие органические соединения, фенолы и др. В этом случае индукционный период определяется как время, в течение которого в системе разрушается ингибитор J-H за счёт его взаимодействия с радикалами цепи
R + J-H RH + J
Образующиеся при этом радикалы J малоактивны и не способны дальше продолжать цепь. В связи с отмеченной причиной увеличения индукционного периода важной технологической задачей является очистка исходного сырья от веществ, являющихся ингибиторами или способных при окислении давать ингибиторы.
Обычные катализаторы жидкофазного окисления (соли марганца, кобальта и др.) в данном случае нельзя использовать в качестве инициирующих агентов, так как они вызываеют заметное разложение гидропероксида в побочный продукт – диметилфенилкарбинол.
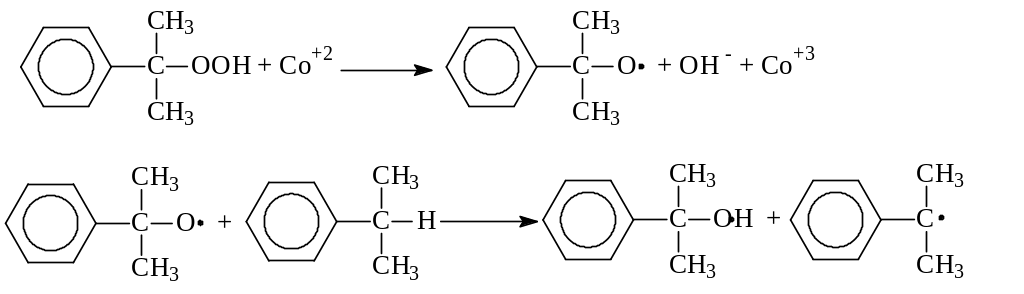
Процесс окисления изопропилбензола в гидропероксид осложняется образованием побочных продуктов: ацетофенона и диметилфенилкарбинола. Механизм основной и побочных реакций может быть представлен следующей схемой
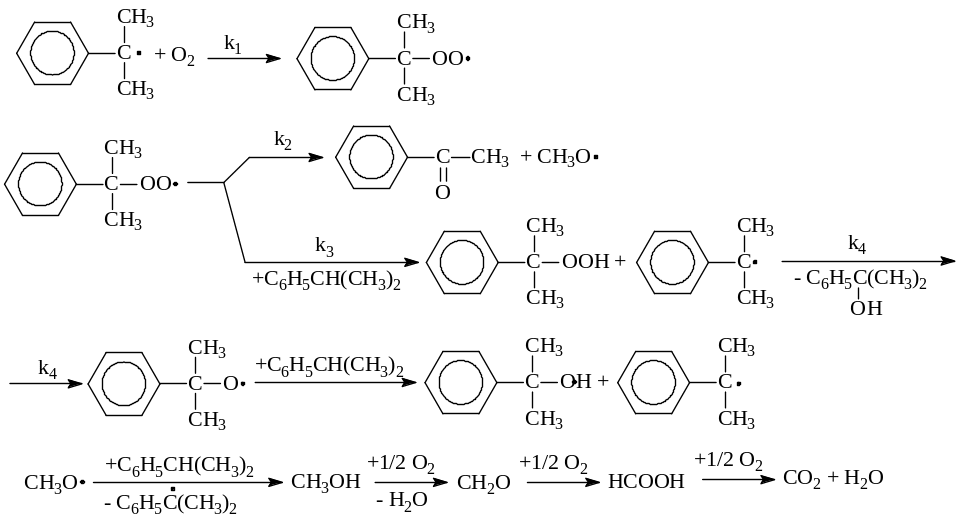
В соответствии с представленной схемой дифференциальная селективность процесса по гидропероксиду выразится уравнением
|
(4) |
В условиях стационарности
![]()
однако поскольку удельный вес ацетофенона в этом процессе невелик, членом r2 в последнем равенстве можно пренебречь
![]()
Тогда соотношение концентраций
![]() выразится
уравнением
выразится
уравнением
![]()
Подставляя последнее выражение в уравнение (4), имеем окончательно
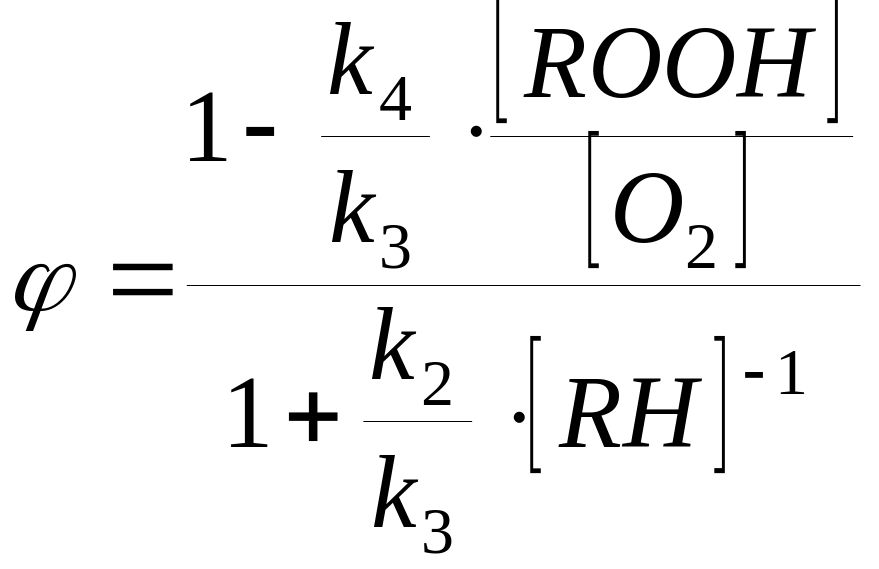
Анализ этого уравнения показывает, что селективность реакции падает с понижением парциального давления кислорода и ростом глубины превращения (что соответствует накоплению гидропероксида и уменьшению концентрации углеводорода). В соответствии с более низкими энергиями активации реакции развития цепей основного процесса по сравнения с побочными Е4>E1 и E2>E3 селективность процесса растёт с понижением температуры, однако при этом понижается его скорость. Это обусловливает необходимость выбора оптимальной температуры. На практике процесс проводят при температурах 105-120С. Если процесс осуществляется в каскаде реакторов, то температуру процесса ступенчато понижают при переходе от одного реактора к другому. Такое решение позволяет при сохранении скорости процесса (за счёт увеличения концентрации гидропероксида) увеличить селективность процесса.
Увеличение давления приводит к росту скорости и селективности процесса. В то же время давление ограничивается сверху в связи с более жёсткими условиями работы оборудования, увеличением расходов на компримирование, расширением пределов взрываемости паро-газовой смеси над реакционной массой. На практике работают с давлением 0,3-0,5 МПа.
Время реакции определяется значением оптимальной конверсии. Увеличение конверсии (соответствующие накоплению ROOH и исчерпыванию RH) приводит в соответствии с уравнением (5) к снижению селективности.
Снижение конверсии, выгодное с точки зрения селективности, приводит к возрастанию доли непрореагировавшего изопропилбензола, что требует дополнительных затрат на его рециркуляцию. Оптимальная конверсия, представляющая компромисс между требованиями высокой селективности и экономичного рецикла, составляет обычно 25-30%. Таким значениям конверсии соответствует продолжительность реакции порядка нескольких часов.
В силу высокой реакционной способности изопропилбензола процесс при определенных условиях может протекать в диффузионной области. В этом случае низкие концентрации кислорода в реакционной массе, в соответствии с уравнением (5) обусловливают понижение селективности процесса. Поэтому важной технологической задачей при реализации процесса является создание эффективного гидродинамического режима.
Эта задача решается созданием режима циркуляции реакционной массы, проведением процесса в высокоэффективных массообменных аппаратах.
Присутствие кислых примесей в реакционной массе вызывает нежелательный процесс разложения гидропероксида с образованием фенола, который является ингибитором процесса свободно-радикального окисления:
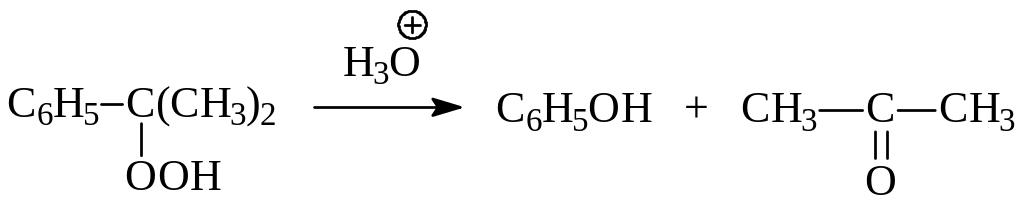
С целью нейтрализации образующихся в ходе процесса кислых примесей, например, по реакции:
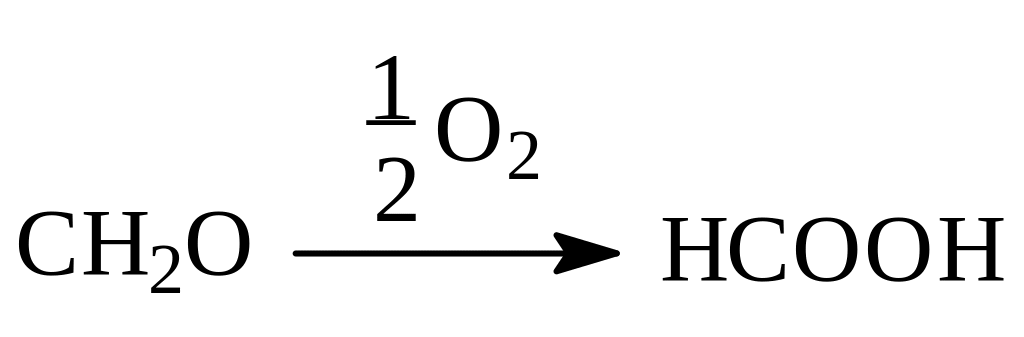
процесс окисления изопрпилбензола часто ведут в присутствии щелочных агентов. В качестве последних используют BaCO3, CaCO3, Na2CO3, NaHCO2 и др.
Разложение гидропероксида на фенол и ацетон.
Разложение гидропероксида изопропилбензола катализируется протонными кислотами. Реакция протекает по ионному механизму:
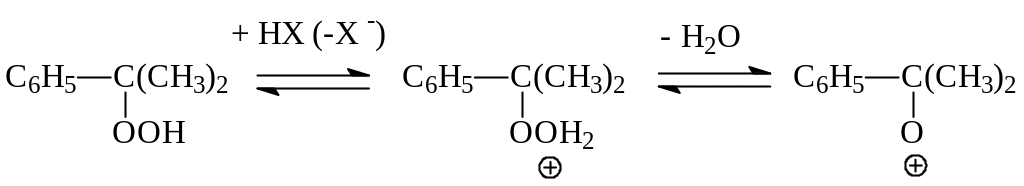
Образующийся катион перегруппировывается с миграцией енольной группы к кислородному атому и последующими превращениями, в результате которых получается фенол и ацетон:
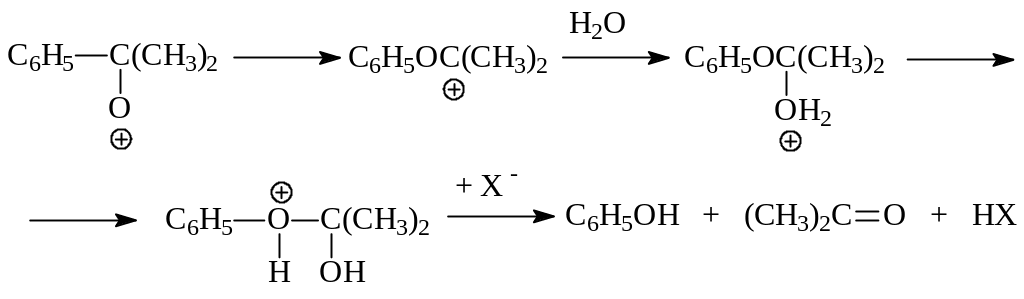
Побочные продукты окисления, содержащиеся в качестве примесей в гидропероксиде, также способны вступать в различные реакции под действием кислотных катализаторов. Так, диметилфенилкарбинол дегидратируется с образованием -метилстирола, а также выступает в качестве алкилирующего агента по отношению к фенолу. Кроме того, -метилстирол димеризуется:
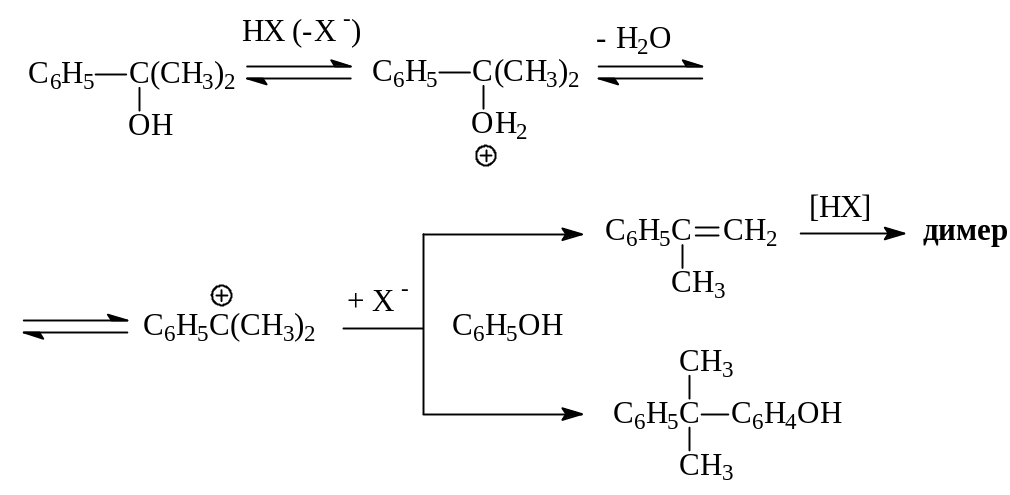
Получаются также небольшое количество смол более сложного строения. При повышении концентрации кислоты и температуры становятся возможными кислотно-каталитические превращения ацетофенона и ацетона, например, по типу альдолной конденсации с последующим отщеплением воды:
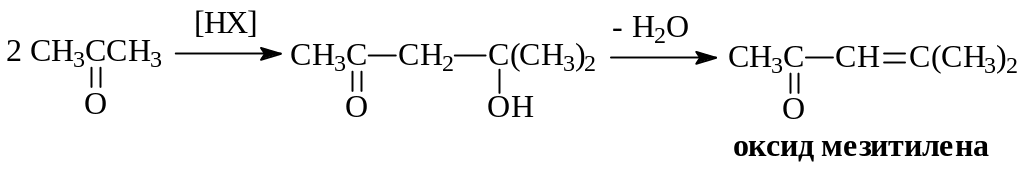
Скорость основной реакции описывается уравнением:
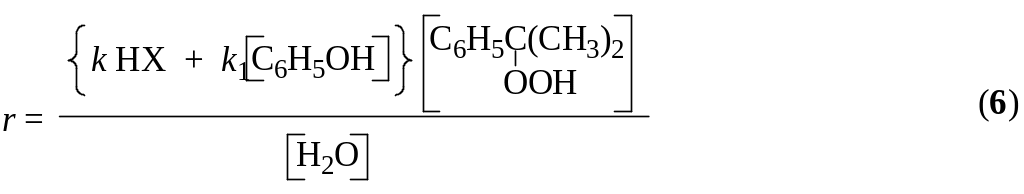
Реакция протекает очень быстро. В присутствии 0,05-0,1 % (масс.) H2SO4 при 50-600С достигается практически полное превращение за 2-3 мин.
Ввиду высокой скорости процесса при его промышленной реализации необходимо, чтобы ее значение не достигало предела, при котором невозможно снять тепловыделения, чтобы сделать процессы съема тепла контролируемыми, реакцию ведут в разбавителях, в качестве которых выступают продукты реакции и ацетон.
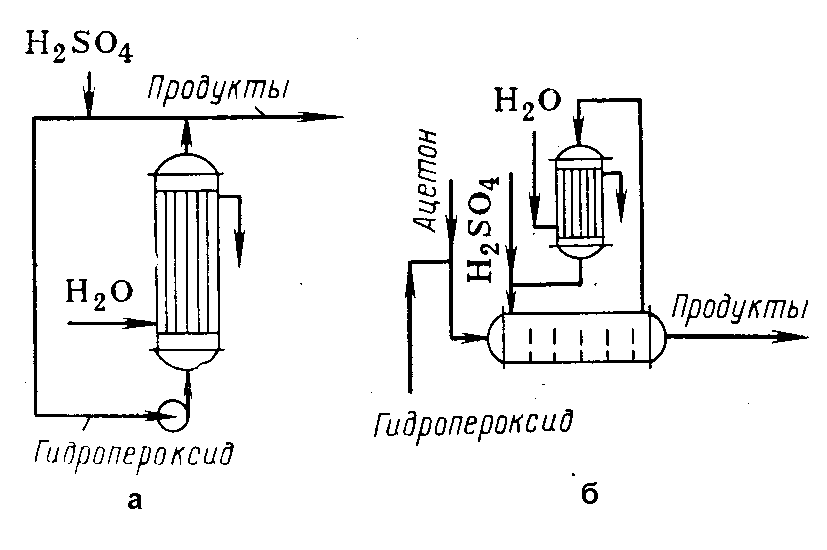
Рис. 1. Реакционные узлы для кислотного разложения гидропероксидов:
а – проточно-циркуляционная установка;
б – установка с отводом тепла за счет испарения ацетона.
Один из методов проведения реакции состарив применении проточно-циркуляционной установки (pис. 1а), когда выделяющееся тепло снимают в трубчатом реакторе за счет охлаждения его водой. Реакционную смесь по выходе из реактора частично отводят на дальнейшую переработку, но основное количество направляют на рециркуляцию: добавляют кислоту-катализатор и в насосе смешивают с исходным гидроперокси-дом. При такой системе время контакта лимитируется теплоотводом и является завышенным. Кроме того, рециркуляция смеси ведет к повышенному выходу побочных веществ. Так, на 1 т фенола получается 100—150 кг отходов, в том числе 15-20 кг -метилстирола, 40—50 кг димера и смол, 5—10 кг ацетофенона, 30 кг кумилфенола и т. д. Хотя окиси мезитила образуется немного, но она существенно затрудняет очистку фенола.
Другой способ кислотного разложения гидропероксидов (рис. 1б) состоит в проведении реакции в растворе ацетона и отводе тепла за счет его испарения. Ацетон конденсируют в обратном холодильнике и возвращают в реактор, который можно секционировать поперечными перегородками. Это наряду с уменьшением концентрации фенола в растворе и времени контакта снижает выход побочных веществ.