
- •Содержание
- •1. Введение.
- •1.1 Общие закономерности химических процессов. Классификация процессов общей химико-технологических процессов
- •Требования к химическим производствам
- •Компоненты химического производства
- •Разделение на две твердые фазы:
- •Разделение жидкости и твердого вещества:
- •1.2 Промышленный катализ
- •Основные положения теории катализа.
- •1.3. Сырьевая база химической промышленности.
- •Классификация сырья
- •Характеристика минерального сырья
- •Химическое сырье
- •Растительное и животное сырье
- •Характеристика разработок минерального сырья
- •Качество сырья и методы его обработки
- •Способы сортировки:
- •Способы обогащения:
- •Сырьевая база химических производств
- •1.4 Энергетическая база химических производств
- •1.5 Критерии оценки эффективности производства
- •1.5.1. Интегральные уравнения баланса материальных потоков в технологических процессах. Понятие о расходных коэффициентах. Относительный выход продукта
- •1.5.2. Балансы производства
- •1. Материальный баланс
- •2. Энергетический (тепловой) баланс
- •3. Экономический баланс
- •1.5.3. Технологические параметры химико-технологических процессов.
- •1.6.Принципы создания ресурсосберегающих технологий
- •2. Теоретические основы химической технологии
- •2.1. Энергия в химическом производстве. Тепловой эффект реакции в технологических расчетах. Направленность реакции в технологических расчетах
- •2.2 Массообменные процессы. Основные принципы массообменных процессов. Моделирование процессов теплообмена.
- •Молекулярная диффузия. Первый закон Фика
- •Турбулентная диффузия
- •Уравнение массоотдачи
- •Уравнение массопередачи
- •Связь коэффициента массопередачи и коэффициентов массоотдачи (или уравнение аддитивности фазовых сопротивлений)
- •Подобие массобменных процессов
- •3. Химическое производство как сложная система. Иерархическая организация процессов в химическом производстве
- •3.1. Химико-технологические системы (хтс). Элементы хтс. Структура и описание хтс. Методология исследования хтс, синтез и анализ хтс.
- •Методология исследование химико-технологических систем.
- •3.2. Сырьевая и энергетическая подсистема хтс
- •1. Классификация химических реакторов по гидродинамической обстановке.
- •2. Классификация химических реакторов по условиям теплообмена.
- •3. Классификация химических реакторов по фазовому составу реакционной массы.
- •4. Классификация по способу организации процесса.
- •5. Классификация по характеру изменения параметров процесса во времени.
- •6. Классификация по конструктивным характеристикам.
- •3.4. Промышленные химические реакторы. Реакторы для гомогенных процессов, гетерогенных процессов с твердой фазой, гетерогенно-каталитических процессов, гетерофазных процессов.
- •Реакторы для гетерогенных процессов с твердой фазой.
- •Реакторы для гетерогенно-каталитических процессов.
- •4. Основные математические модели процессов в химических реакторах
- •4.1. Идеальные химические реакторы. Непрерывный реактор идеального вытеснения. Непрерывный реактор идеального смешения
- •4.2. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения. Обоснование использования каскада реакторов.
- •Каскад реакторов смешения.
- •Влияние степени конверсии.
- •Влияние температуры.
- •5. Применение кинетических моделей для выбора и оптимизации условий проведения процессов
- •5.1. Экономические критерии оптимизации и их применение для оптимизации реакционных узлов.
- •Оптимальные концентрации инициатора и температуры в радикально-цепных реакциях
- •Оптимизация степени конверсии.
- •7. Важнейшие промышленные химические производства
- •7.1 Проблема фиксации атмосферного азота. Синтез аммиака, Физико-химические основы производства и обоснование выбора параметров и типа реакционного узла. Технологическая схема процесса.
- •Синтез аммиака
- •Сырье для синтеза аммиака.
- •Технология процесса.
- •Основные направления в развитии производства аммиака.
- •7.2. Получение азотной кислоты. Физико-химические основы химических стадий процесса, обоснование выбора параметров и типа реакторов. Технологическая схема процесса.
- •Физико-химические основы процесса.
- •Контактное окисление аммиака.
- •Обоснование роли параметров и их выбор.
- •Окисление оксида азота (II) до диоксида.
- •Абсорбция диоксида азота.
- •Технология процесса.
- •7.3. Производство минеральных удобрений. Классификация минеральных удобрений
- •Классификация минеральных удобрений.
- •7.3.1. Азотные удобрения. Физико-химические основы производства нитрата аммония. Устройство реакционного узла. Теоретические основы процесса и его технологическое оформление
- •Производство нитрата аммония.
- •7.3.2. Производство фосфорной кислоты. Физико-химические основы процесса. Технологическая схема
- •Функциональная схема производства эфк.
- •Сернокислотное разложение апатита.
- •7.3.3. Фосфорные удобрения. Физико-химические основы процессов их производства. Типы реакционных узлов.
- •Производство простого суперфосфата.
- •Производство двойного суперфосфата
- •Азотнокислое разложение фосфатов. Получение сложных удобрений
- •Обжиг серосодержащего сырья.
- •Обоснование роли параметров и их выбор.
- •Сжигание серы.
- •Окисление диоксида серы.
- •Обоснование роли параметров и их выбор.
- •Технология контактного окисления so2.
- •Абсорбция триоксида серы.
- •Перспективы развития сернокислотных производств.
- •7.5. Электрохимические производства. Теоретические основы электролиза водных растворов и расплавленных сред. Технология электролиза раствора хлорида натрия.
- •Основные направления применения электрохимических производств
- •Электролиз раствора хлорида натрия
- •Электролиз раствора NaCl с твердым катодом и фильтрующей диафрагмой
- •Электролиз раствора хлорида натрия с ртутным катодом
- •7.6. Промышленный органический синтез
- •Первичная переработка нефти.
- •Каталитический риформинг углеводородов.
- •7.6.2. Производство этилбензола и диэтилбензола. Теоретические основы процесса и обоснование выбора условий процесса. Технология процесса
- •7.6.3. Синтезы на основе оксида углерода. Производство метанола. Теоретические основы процесса.
- •Окисление изопропилбензола (кумола)
- •Технологическая схема получения фенола и ацетона кумольным способом.
- •7.6.5. Биохимические производства. Особенности процессов биотехнологии.
- •7.6.5.1. Производство уксусной кислоты микробиологическим синтезом
- •7.6.5.2. Производство пищевых белков
- •8. Химико-технологические методы защиты окружающей среды
- •8.1. Утилизация и обезвреживание твердых отходов
- •8.2. Утилизация и обезвреживание жидких отходов
- •8.3. Обезвреживание газообразных отходов
Влияние степени конверсии.
Большое влияние на удельную
производительность реакторов оказывает
степень конверсии. Так, для простой
необратимой реакции с кинетическим
уравнением
![]() при проведении ее в аппарате идеального
смешения при
при проведении ее в аппарате идеального
смешения при
![]() имеем
имеем
![]() .
Следовательно, с повышением степени
конверсии удельная производительность
падает тем более резко, чем выше суммарный
порядок (рисунок, кривые 2 и 3), причем
при
.
Следовательно, с повышением степени
конверсии удельная производительность
падает тем более резко, чем выше суммарный
порядок (рисунок, кривые 2 и 3), причем
при
![]() производительность стремится к нулю.
Для реакторов идеального вытеснения
ее снижение с конверсией выражено не
так сильно (см. рисунок, кривые 1 и 2),
вследствие чего эти реакторы предпочтительны
для процессов, где особенно желательна
высокая степень конверсии сырья.
производительность стремится к нулю.
Для реакторов идеального вытеснения
ее снижение с конверсией выражено не
так сильно (см. рисунок, кривые 1 и 2),
вследствие чего эти реакторы предпочтительны
для процессов, где особенно желательна
высокая степень конверсии сырья.
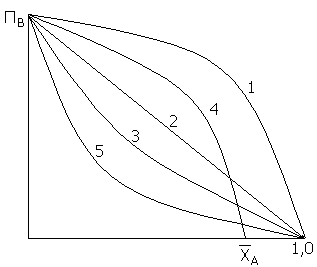
Рисунок. Зависимость удельной производительности от степени конверсии для реакций первого (2) и второго (3) порядков в РИС; для реакций первого (1) и второго (2) в РИВ; для обратимой реакции (4); для реакций, тормозимых образующимися продуктами (5).
В случае обратимых реакций (кривая 4)
удельная производительность стремится
к нулю, когда степень конверсии
приближается к равновесной, а движущая
сила обратимой реакции
![]() – к нулю. Для реакций, которые тормозятся
образующимися продуктами, удельная
производительность падает с повышением
степени конверсии особенно сильно
(кривая 5) (кинетическое уравнение
– к нулю. Для реакций, которые тормозятся
образующимися продуктами, удельная
производительность падает с повышением
степени конверсии особенно сильно
(кривая 5) (кинетическое уравнение
![]() ).
).
Таким образом, для реакций, характеризующихся
суммарным порядком
![]() удельная производительность существенно
зависит от степени конверсии, падая до
нуля при ХА=1 для необратимых
реакций
удельная производительность существенно
зависит от степени конверсии, падая до
нуля при ХА=1 для необратимых
реакций
![]() – для обратимых реакций. Последнее
показывает, что для полного завершения
реакции требуется бесконечно большой
объем реактора, что практически
невозможно. Это – одна из причин широко
распространенного в промышленности
неполного превращения реагентов, которые
после разделения смеси возвращаются в
процесс (рецикл исходных реагентов).
– для обратимых реакций. Последнее
показывает, что для полного завершения
реакции требуется бесконечно большой
объем реактора, что практически
невозможно. Это – одна из причин широко
распространенного в промышленности
неполного превращения реагентов, которые
после разделения смеси возвращаются в
процесс (рецикл исходных реагентов).
Влияние температуры.
В уравнение скорости реакции, и,
соответственно производительности,
входит константа скорости, существенно
зависящая от температуры. В подавляющем
большинстве случаев константа скорости
сильно возрастает с ростом температуры.
Поэтому температура является важнейшим
фактором производительности процессов.
Если в основе процессов лежат обратимые
или необратимые эндотермические реакции,
то производительность процессов
возрастает с ростом температуры во всем
мыслимом ее диапазоне. В случае обратимых
эндотермических реакций температура
одновременно действует как фактор
ускорения реакции и как фактор смещения
равновесия в сторону продуктов. Это
хорошо иллюстрируется кинетическим
уравнением таких реакций, например, для
реакции
![]()
![]() (1)
(1)
С ростом температуры возрастает и
константа скорости реакции
![]() и константа равновесия К. В результате
растет сомножитель
и сомножитель, заключенный в квадратную
скобку.
и константа равновесия К. В результате
растет сомножитель
и сомножитель, заключенный в квадратную
скобку.
По иному обстоит дело у обратимых экзотермических реакций (Н>0), когда требования кинетики и термодинамики взаимно противоположны. В этой случае с ростом температуры возрастает член , но уменьшается константа равновесия К, что приводит уменьшению значения сомножителя, заключенного в квадратные скобки. Противоборство этих двух факторов обусловливает экстремальную зависимость производительности от температуры. Очевидно, что положение температурного экстремума зависит от степени конверсии реагентов, так как входящие в уравнение (1) концентрации компонентов зависят от глубины протекания процесса
![]()
Оптимальная температура тем ниже, чем выше степень конверсии и для данного случая выгодно постепенно понижающийся профиль температур (рис.1 )
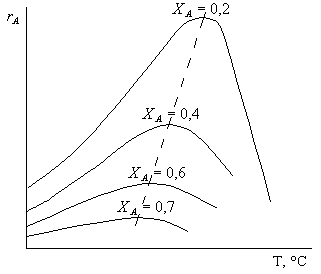
Рисунок 1. Зависимость скорости обратимой реакции от температуры при разной степени конверсии.
Последний вывод относится к реакторам периодического действия идеального вытеснения. В первом случае необходимо в течение операции по мере увеличения степени понижать температуру. При использовании робототехники с анализаторами состава реакционной массы должна быть закоммутирована «следящая система», дающая сигнал на исполнительный орган (вентиль горячего пара) на уменьшение интенсивности теплового потока в соответствии с требуемым значением оптимума. Во втором случае можно разбить реакционное пространство на секции и понижать температуру после каждой секции путем подачи части захоложенного реагента в реакционный поток или снимать избыточное тепло с помощью теплообменников. Можно предусмотреть также дифференциальный подогрев реакционного потока по высоте реактора.
При безградиентных условиях, когда реактор работает при постоянной температуре, оптимум последней определяется ординатой кривой при заданной степени превращения, а при использовании каскада реакторов идеального смешения температуру менять ступенчато в соответствии с принятой для каждого реактора степенью конверсии.
