
- •Содержание
- •1. Введение.
- •1.1 Общие закономерности химических процессов. Классификация процессов общей химико-технологических процессов
- •Требования к химическим производствам
- •Компоненты химического производства
- •Разделение на две твердые фазы:
- •Разделение жидкости и твердого вещества:
- •1.2 Промышленный катализ
- •Основные положения теории катализа.
- •1.3. Сырьевая база химической промышленности.
- •Классификация сырья
- •Характеристика минерального сырья
- •Химическое сырье
- •Растительное и животное сырье
- •Характеристика разработок минерального сырья
- •Качество сырья и методы его обработки
- •Способы сортировки:
- •Способы обогащения:
- •Сырьевая база химических производств
- •1.4 Энергетическая база химических производств
- •1.5 Критерии оценки эффективности производства
- •1.5.1. Интегральные уравнения баланса материальных потоков в технологических процессах. Понятие о расходных коэффициентах. Относительный выход продукта
- •1.5.2. Балансы производства
- •1. Материальный баланс
- •2. Энергетический (тепловой) баланс
- •3. Экономический баланс
- •1.5.3. Технологические параметры химико-технологических процессов.
- •1.6.Принципы создания ресурсосберегающих технологий
- •2. Теоретические основы химической технологии
- •2.1. Энергия в химическом производстве. Тепловой эффект реакции в технологических расчетах. Направленность реакции в технологических расчетах
- •2.2 Массообменные процессы. Основные принципы массообменных процессов. Моделирование процессов теплообмена.
- •Молекулярная диффузия. Первый закон Фика
- •Турбулентная диффузия
- •Уравнение массоотдачи
- •Уравнение массопередачи
- •Связь коэффициента массопередачи и коэффициентов массоотдачи (или уравнение аддитивности фазовых сопротивлений)
- •Подобие массобменных процессов
- •3. Химическое производство как сложная система. Иерархическая организация процессов в химическом производстве
- •3.1. Химико-технологические системы (хтс). Элементы хтс. Структура и описание хтс. Методология исследования хтс, синтез и анализ хтс.
- •Методология исследование химико-технологических систем.
- •3.2. Сырьевая и энергетическая подсистема хтс
- •1. Классификация химических реакторов по гидродинамической обстановке.
- •2. Классификация химических реакторов по условиям теплообмена.
- •3. Классификация химических реакторов по фазовому составу реакционной массы.
- •4. Классификация по способу организации процесса.
- •5. Классификация по характеру изменения параметров процесса во времени.
- •6. Классификация по конструктивным характеристикам.
- •3.4. Промышленные химические реакторы. Реакторы для гомогенных процессов, гетерогенных процессов с твердой фазой, гетерогенно-каталитических процессов, гетерофазных процессов.
- •Реакторы для гетерогенных процессов с твердой фазой.
- •Реакторы для гетерогенно-каталитических процессов.
- •4. Основные математические модели процессов в химических реакторах
- •4.1. Идеальные химические реакторы. Непрерывный реактор идеального вытеснения. Непрерывный реактор идеального смешения
- •4.2. Сравнение эффективности проточных реакторов идеального смешения и идеального вытеснения. Обоснование использования каскада реакторов.
- •Каскад реакторов смешения.
- •Влияние степени конверсии.
- •Влияние температуры.
- •5. Применение кинетических моделей для выбора и оптимизации условий проведения процессов
- •5.1. Экономические критерии оптимизации и их применение для оптимизации реакционных узлов.
- •Оптимальные концентрации инициатора и температуры в радикально-цепных реакциях
- •Оптимизация степени конверсии.
- •7. Важнейшие промышленные химические производства
- •7.1 Проблема фиксации атмосферного азота. Синтез аммиака, Физико-химические основы производства и обоснование выбора параметров и типа реакционного узла. Технологическая схема процесса.
- •Синтез аммиака
- •Сырье для синтеза аммиака.
- •Технология процесса.
- •Основные направления в развитии производства аммиака.
- •7.2. Получение азотной кислоты. Физико-химические основы химических стадий процесса, обоснование выбора параметров и типа реакторов. Технологическая схема процесса.
- •Физико-химические основы процесса.
- •Контактное окисление аммиака.
- •Обоснование роли параметров и их выбор.
- •Окисление оксида азота (II) до диоксида.
- •Абсорбция диоксида азота.
- •Технология процесса.
- •7.3. Производство минеральных удобрений. Классификация минеральных удобрений
- •Классификация минеральных удобрений.
- •7.3.1. Азотные удобрения. Физико-химические основы производства нитрата аммония. Устройство реакционного узла. Теоретические основы процесса и его технологическое оформление
- •Производство нитрата аммония.
- •7.3.2. Производство фосфорной кислоты. Физико-химические основы процесса. Технологическая схема
- •Функциональная схема производства эфк.
- •Сернокислотное разложение апатита.
- •7.3.3. Фосфорные удобрения. Физико-химические основы процессов их производства. Типы реакционных узлов.
- •Производство простого суперфосфата.
- •Производство двойного суперфосфата
- •Азотнокислое разложение фосфатов. Получение сложных удобрений
- •Обжиг серосодержащего сырья.
- •Обоснование роли параметров и их выбор.
- •Сжигание серы.
- •Окисление диоксида серы.
- •Обоснование роли параметров и их выбор.
- •Технология контактного окисления so2.
- •Абсорбция триоксида серы.
- •Перспективы развития сернокислотных производств.
- •7.5. Электрохимические производства. Теоретические основы электролиза водных растворов и расплавленных сред. Технология электролиза раствора хлорида натрия.
- •Основные направления применения электрохимических производств
- •Электролиз раствора хлорида натрия
- •Электролиз раствора NaCl с твердым катодом и фильтрующей диафрагмой
- •Электролиз раствора хлорида натрия с ртутным катодом
- •7.6. Промышленный органический синтез
- •Первичная переработка нефти.
- •Каталитический риформинг углеводородов.
- •7.6.2. Производство этилбензола и диэтилбензола. Теоретические основы процесса и обоснование выбора условий процесса. Технология процесса
- •7.6.3. Синтезы на основе оксида углерода. Производство метанола. Теоретические основы процесса.
- •Окисление изопропилбензола (кумола)
- •Технологическая схема получения фенола и ацетона кумольным способом.
- •7.6.5. Биохимические производства. Особенности процессов биотехнологии.
- •7.6.5.1. Производство уксусной кислоты микробиологическим синтезом
- •7.6.5.2. Производство пищевых белков
- •8. Химико-технологические методы защиты окружающей среды
- •8.1. Утилизация и обезвреживание твердых отходов
- •8.2. Утилизация и обезвреживание жидких отходов
- •8.3. Обезвреживание газообразных отходов
Уравнение массопередачи
Сложность расчета по уравнениям массоотдачи состоит в том, что практически невозможно измерить концентрации фаз непосредственно у границы их раздела. По этой причине количество вещества М, переносимого из фазы в фазу, рассчитывают по основному уравнению массопередачи, которое записывают в форме:
![]()
![]()
здесь Кх и Ку – коэффициенты массопередачи, выраженные, соответственно, через концентрации фаз Фх и Фу,
у* и х* - равновесные концентрации в данной фазе, соответствующие концентрациям распределяемого вещества в ядре другой фазы.
Физический смысл коэффициента массопередачи (Кх и Ку). Он показывает, какое количество вещества переходит из фазы в фазу за единицу времени через единицу поверхности контакта фаз при движущей силе массопередачи, равной 1.
Коэффициенты и К различаются по физической сущности, но выражаются одинаковыми единицами измерения.
![]()
Так как концентрации фаз изменяются при их движении вдоль поверхности раздела, изменяется и движущая сила массопередачи. Поэтому в уравнение массопередачи вводят среднюю движущую силу (хср или уср) и уравнения принимают вид:
![]()
![]()
Из уравнений массопередачи можно рассчитать скорость процесса по известным размерам аппарата.
![]()
![]()
Из основного уравнения массопередачи обычно рассчитывают размеры аппарата, если можно определить
Кх и Ку.
Связь коэффициента массопередачи и коэффициентов массоотдачи (или уравнение аддитивности фазовых сопротивлений)
Рассмотрим случай переноса вещества из фазы Фу в фазу Фх; движущая сила массопередачи выражена в единицах концентрации фазы Фу. Количество вещества М, переносимое из фазы в фазу, рассчитываем из уравнения массопередачи. Допустим, что равновесная зависимость между концентрациями в фазах линейна (8) у* = mx, где m – tg угла наклона линии равновесия.
Примем,что концентрации распределяемого вещества в фазах у границы раздела (хгр., угр.) равновесны друг другу.
Тогда из уравнения линии равновесия следует, что:
хгр. = угр./m и х = у*/m
где хгр. и угр - концентрации каждой фазы, у*- концентрация фазы Фу, равновесная с концентрацией х фазы Фх.
Подставляя
значения хгр.
и х в уравнение массоотдачи
![]() ,
получим
,
получим![]() .
.
Определим движущую силу процесса:
![]()
Из
уравнения
движущая сила процесса в фазе Фу ![]()
Суммируем почленно уравнения получим:
![]()
Уравнение массопередачи для рассматриваемого случая имеет следующий вид:
или ![]()
Приравнивая правые части уравнений, находим зависимость между коэффициентами массопередачи Ку и массоотдачи х и у:
![]()
При выражении коэффициента массопередачи в конценрациях фазы Фх будем иметь
![]()
Левые части уравнений представляют собой общее сопротивление массопередаче, а их правые части – сумму сопротивлений массоотдаче в фазах.
При m = сonst разделим уравнение на m, получим:
![]() или
или
![]() ,
т.е.
,
т.е.
![]()
Уравнение (39) аналогично уравнению аддитивности термических сопротивлений, которое устанавливает связь между коэффициентом теплопередачи К и коэффициентами теплоотдачи 1 и 2. В уравнении член 1/у выражает диффузионное сопротивление переходу вещества в фазе Фу, член m/y – сопротивление в фазе Фх. Если коэффициент у велик, то член 1/у мал и, как видно из уравнения,
![]() .
В этом случае сопротивлением в фазе Фу
можно пренебречь.
.
В этом случае сопротивлением в фазе Фу
можно пренебречь.
При большом коэффициенте х
член m/х
мал и как видно из
уравнения,
![]() .
В этом случае сопротивлением Фх
можно пренебречь.
.
В этом случае сопротивлением Фх
можно пренебречь.
При выводе уравнения было принято условие линейной зависимости между равновесными концентрациями у* и х. В случае отсутствия такой зависимости линия равновесия не будет прямой и константу равновесия надо брать как тангенс угла наклона касательной к линии равновесия в данной точке. При этом величины m и Ку будут изменяться по длине аппарата. При расчетах берут среднее значение коэффициента распределения m.
Пример. В массообменном аппарате, работающем под давлением Рабс = 3,1 ат, коэффициенты массоотдачи имеют следующие значения:
![]() ,
,![]() .
Равновесные составы газовой и жидкой
фаз характеризуются законом Генри: р*
= 0,08106х
. Определить:а) коэффициенты массопередачи
Кх
и Ку;
б) во сколько раз диффузионное сопротивление
жидкой фазы отличается от диффузионного
сопротивления газовой фазы.
.
Равновесные составы газовой и жидкой
фаз характеризуются законом Генри: р*
= 0,08106х
. Определить:а) коэффициенты массопередачи
Кх
и Ку;
б) во сколько раз диффузионное сопротивление
жидкой фазы отличается от диффузионного
сопротивления газовой фазы.
Решение. Используем уравнение Генри-Дальтона
у* = mх:
![]()
Находим коэффициенты массопередачи:
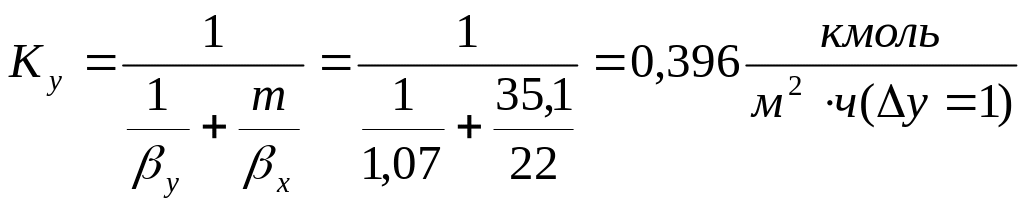
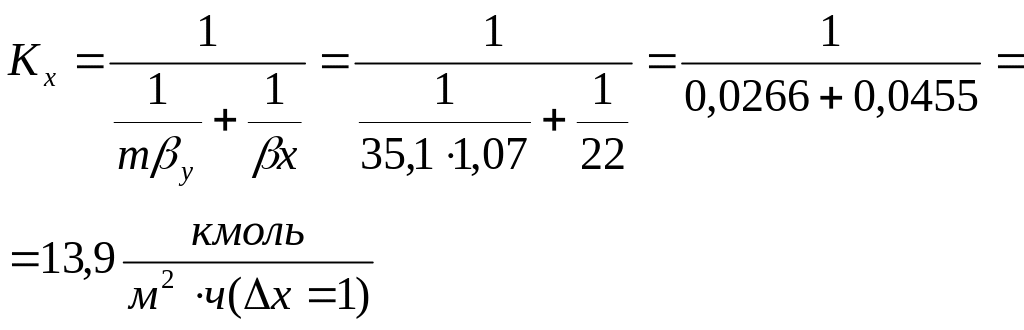
Проверка:![]()
Отношение диффузионных сопротивлений жидкой и газовой фаз при движущей силе у:
![]()
Такое же отношение будет и при движущей силе х.
Диффузионное сопротивление жидкой фазы в 1,71 раза больше сопротивления газовой фазы.
