
- •2.4. Який клінічний матеріал може бути використаний при лабораторній діагностиці вірусних інфекцій у живих системах.
- •Вкажіть мішені дії противірусних препаратів у життєвому циклі вірусів.
- •3.1. Особливості росту клітин в культурі.
- •Особенности образования монослоя трансформированными клетками (клетки образуют мультислой)
- •Методи прямої і непрямої імунофлюоресценції.
- •Метод "летающих стекол"
- •Стандартизація лабораторних тварини за генетичними характеристиками.
- •1. Инбредные (линейные):
- •Отбор клинического материала для исследования
- •Основні групи сучасних дезінфікуючих засосбів, їх характеристики, механізми дії.
- •Галоїдовмісні сполуки
- •Альдегідовмісні сполуки
- •Пероксиданти
- •Четвертинні амонієві сполуки
- •Похідні гуанідину
- •Третинні алкіламіни (амфотензиди)
- •Композиційні препарати
- •4.5. Протигерпетичні препарати
- •5.3. Відповідно класифікації всі лабораторні тварини поділяються на 4 категорії
- •Що таке сд50, лд50, мпк, особливості їх визначення у біологічних системах.
- •6.1.Джерела одержання клітинних культур
- •Види клінічного матеріалу, що використовуються у лабораторній діагностиці вірусних інфекцій
- •6.3. Гнотобіоти і гнотобіологія
- •Які існують способи введення інфекційного матеріалу лабораторним тваринам
- •6.5.Категорії дезінфікуючих засобів в залежності від кінцевої мети їх застосування
- •7.2. Підготовка клінічного матеріалу до лабораторних досліджень в біологічних системах.
- •7.3. Стандартні умови утримання і годівлі лабораторних тварин.
- •7.4 За якими ознаками можна визначити, що в організмі лабораторної тварини відбувається репродукція вірусів.
- •7.5. Вимоги до тест-вірусів при дослідженні віруліцидної дії дезінфікуючих засобів.
- •8.1. Живильні середовища для культивування клітинних культур, їх призначення і основні характеристики.
- •8.2. Особливості деконтамінації клінічного матеріалу, що містить складні віруси.
- •8.3. Яке значення має вибір певного виду і кількості лабораторних тварин для валідації вірусологічних досліджень.
- •8.4. .Що таке лд50 та інфекційний титр вірусу, визначений на лабораторних тваринах, як між собою пов’язані ці величини.
- •8.5.Чому необхідно використовувати тест-віруси при дослідженні віруліцидної дії дезінфікуючих засобів.
- •Билет №9
- •Сольові розчини для культивування клітинних культур, їх призначення і основні характеристики.
- •9.2. Що таке стандартні умови утримання лабораторних тварин.
- •Алгоритми дослідження віруліцидної дії дезінфікуючих засобів.
- •Які основні принципи гуманного ставлення до лабораторних тварин викладені у Європейській конвенції про захист лабораторних тварин.
- •13.4.В чому полягають основні методичні прийоми при типуванні вірусів в рн у біологічних системах.
- •13.5.Визначення віруліцидної дії дезінфікуючих засобів суспензійним методом.
- •Роль ростових факторів при культивуванні культур клітин, джерела їх одержання.
- •14.2.Титрування вірусів в культурі клітин.
- •14.3.Категорій лабораторних тварин відповідно до наявності у них патогенів та умов утримання.
- •14.4.Противірусні препарати розширеного спектру дії.
- •Призначення живильних середовищ в залежності від вмісту в них сироватки.
- •15.2.Який взаємозв’язок існує між генетичним статусом тварин і об’ємом їх вибірки у групах при проведенні вірусологічних досліджень.
- •15.3.Що таке типування вірусів і як воно проводиться на лабораторних тваринах.
- •15.4Алгоритми визначення специфічної дії противірусних препаратів.
- •Визначення віруліцидної дії дезінфікуючих засобів методом тест-об"єктів.
- •Сироватка тварин як джерело ростових факторів.
- •В чому полягають основні небезпечні чинники при роботі з лабораторними тваринами.
- •16.3 Що є критерієм визначення серотипу вірусу при його типуванні в рн.
- •16.4 Як визначити оптимальний режим дії противірусних хіміопрепаратів у культурі клітин.
- •16.5 Визначення віруліцидної дії дезінфікуючих засобів при знезаражуванні білизни.
- •Билет 17
- •17.1 Основні етапи підготовки сироватки крові тварин до використання у біотехнології клітинних культур.
- •17.2 Яких правил слід дотримуватись при роботі з кров’ю та біологічними рідинами інфікованих або померлих тварин.
- •17.3 Особливості виділення вірусів з клінічного матеріалу, їх титрування та типування у біологічних системах
- •17.4 Розрахунок хіміотерапевтичного індексу противірусного хіміопрепарату.
- •17.5 Визначення віруліцидної дії дезінфікуючих засобів при знезаражуванні води. (в лекциях просто приведены все методы, именно для воды нету)
Білет №2
2.4. Який клінічний матеріал може бути використаний при лабораторній діагностиці вірусних інфекцій у живих системах.
- Фекалии: кишечные вирусы (рота-, адено-, астро-, калицивирусы (норовирусы), энтервирусы (полио, Коксаки, ECHO-вирусы)
- Содержимое везикул : гепресвирусы человека 1, 2, 3 антигенных типов.
- Кожные образования: папиломавирусы
- Носоглоточные смывы : ортомиксо- (грипп), парамиксовирусы (корь, паротит)
ОСНОВНЫЕ ВИДЫ КЛИНИЧЕСКОГО МАТЕРИАЛА ЧЕЛОВЕКА
‾ Носоглоточные смывы
‾ Мазок с глотки
‾ Спинномозговая жидкость
‾ Фекалии и ректальные тампоны
‾ Кровь
‾ Сыворотка крови
‾ Моча
‾ Жидкость из серозных полостей
‾ Мазок с конъюнктивы
‾ Содержимое везикул
‾ Секционный материал
ДРУГИЕ ВИДЫ КЛИНИЧЕСКОГО МАТЕРИАЛА
‾ Органы и ткани животных
‾ Биологические жидкости животных
‾ Насекомые-переносчики вирусных инфекций
‾ Пищевые продукты
‾ Объекты окружающей среды
Вкажіть мішені дії противірусних препаратів у життєвому циклі вірусів.
ПРОТИВОВИРУСНАЯ ХИМИОТЕРАПИЯ
‾ Мишень – инфицированная клетка
ХОРОШИЕ ПРЕПАРАТЫ ДОЛЖНЫ
‾ Ингибировать специфическую активность ферментов вирусов, необходимых для их репликативного цикла (РНК-зависимой-РНК-полимеразы, ревертазы, интегразы и др.)
‾ Подавлять функции клеточных структур, которые вирус использует в своем репликативном цикле.
‾ Направлено разрушать только инфицированные вирусами клетки.
‾ Активироваться (как лекарства-предшественники) только в инфицированных клетках и оставаться в не активной форме в здоровых.
Билет №3.
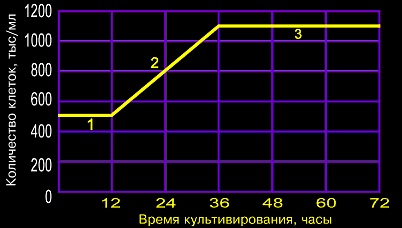
3.1. Особливості росту клітин в культурі.
Первичные клеточные культуры
Преимущества:
- Высокая чувствительность к многим вирусам
- Безопасность в онкогенном отношении
- Могут быть получены в больших количествах
Недостатки:
- Трудоемкость и длительность получения
- Ограниченное число пассажей (до 10)
- Возможность контаминации:
+ в процессе получения
+ латентными вирусами
Диплоидные клеточные культуры (клеточные штаммы)
Преимущества:
- Высокая чувствительность к многим вирусам
- Свободны от контаминантов
- Диплоидный набор хромосом
- Безопасность в онкогенном отношении
Недостатки:
- Ограниченное число пассажей (до 100)
- Исключительная требовательность к условиям культивирования
Перевиваемые клеточные культуры (клеточные линии)
Преимущества:
- Потенциальное безсмертие
- Свободны от контаминантов
- Относительная простота и стандартизация условий культивирования
Недостатки:
- Избирательная чувствительность к вирусам
- Не диплоидный набор хромосом
- Потенциально онкогенны
Трансформация
Совокупность изменений, приводящих к появлению у клеток первичной культуры новых свойств, в результате которых появляются клеточные линии.
Отношение клеток к субстрату
1. Субстратзависимые
2. Субстратнезависимые (суспензионные)
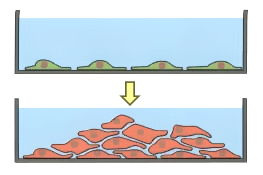
Особенности образования монослоя трансформированными клетками (клетки образуют мультислой)
Методи прямої і непрямої імунофлюоресценції.
Иммунофлюоресценция Иммунофлюоресцентный анализ применяют для выявления как антигенов, так и антител. Этот метод основан на использовании реагентов, меченных флюоресцентным красителем. Антитела чаще всего метят флюоресцеина изотиоцианатом. Меченые антитела связываются с антигеном, образуя комплексы, которые можно выявить с помощью флюоресцентной микроскопии. Существуют три модификации иммунофлюоресцентного анализа:
Метод непрямой иммунофлюоресценции позволяет выявить антитела к известному антигену. Антиген, сорбированный на твердой подложке, связывается с немечеными антителами. Комплексы антиген-антитело выявляются с помощью меченых антител к иммуноглобулинам.
Метод прямой иммунофлюоресценции применяют для выявления антигенов. Он основан на непосредственном связывании антигена, сорбированного на твердой подложке, с мечеными антителами. Реакцию оценивают с помощью флюоресцентного микроскопа.
Метод конкурентной иммунофлюоресценции основан на связывании стандартного меченого и присутствующего в исследуемой пробе немеченого антигенов с антителами, сорбированными на твердой подложке. Поскольку меченый и немеченый антигены конкурируют за связывание с антителами, по количеству связанного меченого антигена можно определить концентрацию антигена в исследуемой пробе.
