
- •Введение
- •1. Коррозия обектов магистрального трубопроводного транспорта нефти и газа
- •1.1. Коррозионные процессы и продукты коррозии
- •1.2. Классификация процессов коррозия
- •1.3. Виды коррозионных разрушений
- •1.4. Способы выражения скорости коррозии
- •1.5. Способы защиты стальных сооружений от коррозии
- •Контрольные вопросы
- •2. Химическая коррозия стальных сооружений
- •2.1. Термодинамическая возможность химической коррозии
- •2.2. Механизм химической коррозии
- •2.3. Влияние окисных пленок на процесс коррозии
- •2.4. Законы роста пленок на поверхности стальных сооружений
- •2.4.1. Закон роста несплошных пленок
- •2.4.2. Закон роста сплошных пленок
- •2.4.3. Закон роста пленок при одинаковых скоростях диффузии окислителя коррозионной среды и ионов металла
- •Контрольные вопросы
- •3. Электрохимическая коррозия стальных сооружений
- •3.1. Термодинамическая возможность электрохимической коррозии металлов
- •3.2. Электродные потенциалы металлов в электролитах
- •3.3. Кинетика электрохимической коррозии металлов
- •3.4. Механизм катодной поляризации
- •3.5. Атмосферная коррозия стальных сооружений
- •3.6. Коррозия стальных трубопроводов в болотной и речной воде
- •Результаты химического анализа почвенного электролита грунтов нефтегазодобывающих регионов
- •3.8. Подземная коррозия стальных сооружений
- •3.9. Микробиологическая коррозия стальных подземных сооружений
- •3.10. Коррозия подземных стальных сооружений блуждающими токами
- •Контрольные вопросы
- •4. Коррозионные изыскания
- •4.1. Методы определения коррозинной активности грунтов
- •Сопоставление коррозионного состояния действующих нефтегазопроводов Западной Сибири с удельным электрическим сопротивлением грунта и плотностью предельного тока кислорода
- •Полевой метод определения удельного электрического сопротивления грунта
- •Полевой метод определения предельного тока по кислороду в толще грунта
- •Лабораторно-полевой метод определения коррозионной активности грунтов по поляризационным кривым и по потере массы стальных образцов
- •4.2. Определение опасности коррозии, вызываемой блуждающими токами, при помощи электрических измерений
- •Определение величины поляризационного потенциала подземных стальных сооружений
- •Определение качества изоляции подземного стального трубопровода методом катодной поляризации
- •Контрольные вопросы
- •5. Изоляционные покрытия
- •5.1. Назначение изоляционных покрытий
- •5.2. Требования к изоляционным покрытиям.
- •5.3. Мастичные покрытия.
- •5.4. Полимерные покрытие
- •5.5. Комбинированные покрытия
- •5.6. Прочие виды изоляционных покрытий
- •Покрытия из эмали и стеклоэмали
- •Покрытия из напыленного или экструдированного полиэтилена
- •5.7. Пооперационный контроль качества изоляционных работ
- •Приборы для контроля изоляционных покрытий
- •Техническая характеристика адгезиметров
- •Техническая характеристика искателя повреждений ип-95
- •Техническая характеристика искрового дефектоскопа идм-1м
- •Техническая характеристика искровых дефектоскопов
- •Контрольные вопросы
- •6. Подготовка поверхности металла перед нанесением защитных покрытий
- •Состояние поверхности металла
- •Способы подготовки поверхности
- •6.1. Механическая очистка Очистка с помощью инструментов
- •Струйная очистка
- •6.2. Термическая очистка
- •6.3. Химическая очистка Обезжиривание
- •Травление
- •6.4. Полирование
- •Степени чистоты поверхности стали
- •Контрольные вопросы
- •7. Противокоррозионная защита полости рвс
- •Л итература
- •Содержание
- •Противокоррозионная защита объектов трубопроводного транспорта нефти и газа
3.5. Атмосферная коррозия стальных сооружений
Атмосферная коррозия стальных сооружений (наземных трубопроводов, резервуаров, газгольдеров и др.) - наиболее распространенный вид коррозии. Она зависит от степени увлажненности корродирующей поверхности стального сооружения и по этому признаку подразделяется на три типа:
мокрая атмосферная коррозия (при относительной влажности воздуха ~ 100 %) при наличии видимой пленки влаги на поверхности металла;
влажная атмосферная коррозия при наличии на корродирующей поверхности невидимой пленки влаги, которая образуется при капиллярной, адсорбционной или химической конденсации;
сухая атмосферная коррозия при полном отсутствии влаги на поверхности стального сооружения.
В реальных условиях все эти типы коррозии взаимно переходят друг в друга. Характер изменения скорости атмосферной коррозии в зависимости от толщины пленки влаги показан на рис. 3.5.1. Эта скорость изменяется от нуля для сухой атмосферной коррозии, достигает максимума для влажной атмосферной коррозии и снижается до некоторого постоянного значения, характеризующего скорость коррозии стального сооружения под пленкой влаги. По данным Ю.Н. Михайловского на свежеобразованной оголенной поверхности стального сооружения в атмосфере водяных паров последовательно протекают следующие реакции:
![]()
![]() (3.5.1)
(3.5.1)
или
![]() (3.5.2)
(3.5.2)
Прямым подтверждением большой вероятности протекания реакции (3.5.1) на корродирующей поверхности стального сооружения в атмосферных условиях является обнаруженное при эксперименте увеличение электропроводности тонких пленок металла при адсорбции на них воды.
Механизм атмосферной коррозии включает электрохимическую (мокрая и влажная) и химическую (сухая) коррозию. Мокрая и влажная атмосферная коррозия носит электрохимический характер и протекает в основном с катодной деполяризацией.
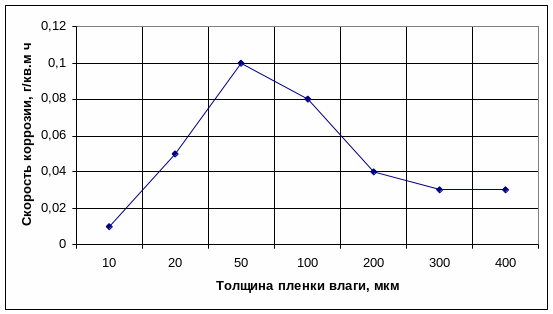
Риc. 3.5.1. Зависимость скорости атмосферной коррозии
от толщины пленки влаги
Особенность атмосферной коррозии металлов - малая толщина слоя электролита на поверхности металла (вода + соли + продукты коррозии). В связи с этим кислород воздуха достаточно легко проникает к поверхности корродирующего металла. Отсюда следует, что с уменьшением толщины слоя электролита катодный процесс атмосферной коррозии стального сооружения облегчается, а анодный процесс затрудняется. Таким образом, малая толщина слоя пленки влаги приводит к большому омическому сопротивлению при работе коррозионных микропар (см. рис. 3.5.1). Следовательно, для атмосферной коррозии контролирующим фактором является катодно-анодно-омический контроль.
На скорость атмосферной коррозии металлов влияет большое число факторов:
влажность воздуха (создание электролита);
примеси воздуха (газы S02, S03,H2S, NH, C12,HC1 и др. в контакте с водой действуют как депассиваторы, комплексообразователи или катодные деполяризаторы; твердые частицы увеличивают электропроводность пленки электролита и облегчают адсорбцию газов и влаги из воздуха);
характер атмосферы (чистая, грязная, сухая, влажная);
географическая зона (тропики, субтропики, средняя полоса, пустыня, полюс);
состояние поверхности корродирующего металла (наличие продуктов коррозии);
наличие инородных включений в металле (одни из них защищают от коррозии — катодные включения, например Си, Pb, Pd, a другие способствуют разрушению металла);
температура (с повышением температуры скорость коррозии и влажность снижаются).
При
«сухой» атмосферной коррозии железо
образует три окисла: вюстит FeO,
магнетит Fe3O4
и гематит Fe2O3.
Концентрация отдельных окислов в
окалине, образующейся при окислении
железа, зависит от состава и давления
атмосферы, от температуры. В общем
случае сухая атмосферная коррозия
представляет собой химическую реакцию
между стальным сооружением и кислородом
воздуха, например:
![]() .
Однако, несмотря на кажущуюся простоту
этой реакции, характер окисления и
кинетика роста оксидной пленки зависят
от ряда факторов, существенно усложняющих
механизм процесса окисления. С позиций
термодинамики, возникновение оксида
возможно в том случае, когда давление
кислорода превышает давление диссоциации
оксида при данной температуре. На
протекание этой реакции существенное
влияние оказывает предварительная
подготовка поверхности, температура,
давление кислорода, наличие примесей
в стали. При нагревании стального изделия
на воздухе образующаяся окалина не
содержит вюстита, если температура
нагрева не превысила 5700С.
Окалина, возникающая при более высоких
температурах, содержит все три вида
окислов. См. рис. 3.5.2.
.
Однако, несмотря на кажущуюся простоту
этой реакции, характер окисления и
кинетика роста оксидной пленки зависят
от ряда факторов, существенно усложняющих
механизм процесса окисления. С позиций
термодинамики, возникновение оксида
возможно в том случае, когда давление
кислорода превышает давление диссоциации
оксида при данной температуре. На
протекание этой реакции существенное
влияние оказывает предварительная
подготовка поверхности, температура,
давление кислорода, наличие примесей
в стали. При нагревании стального изделия
на воздухе образующаяся окалина не
содержит вюстита, если температура
нагрева не превысила 5700С.
Окалина, возникающая при более высоких
температурах, содержит все три вида
окислов. См. рис. 3.5.2.
Основную часть окалины составляет слой FeO, который непосредственно примыкает к неокисленной стальной поверхности; несколько более богат кислородом средний слой Fe3O4, наконец в наружном слое окалины содержится окисел с максимальным содержанием кислорода Fe2O3. На рис. 3.5.2 отчетливо видно, что слой вюстита неоднороден и состоит из двух подслоев, причем подслой, прилегающий к неокисленной стальной поверхности, характеризуется значительной пористостью. При окислении деталей топок, стальных труб котельных установок на НПС, КС и т.д. в среде СО – СО2 возникает окалина, состоящая из одного окисла FeO.

Рис. 3.5.2. Состав оксидных слоев, образующихся на стальных
сооружениях при температуре выше 620 С
Взаимодействие корродирующей поверхности стального сооружения в атмосфере характеризуется следующими стадиями:
нарушение защитного покрытия и образование оголенной поверхности;
адсорбция молекулярного кислорода на оголенной поверхности стального сооружения с последующей диссоциацией на атомы и их хемосорбция;
возникновение зародышей оксидов на локальных участках оголенной поверхности стального сооружения;
формирование и рост сплошной пленки оксида.
При наличии пленки
влаги течение атмосферной коррозии
существенно облегчается и протекает
при обычной температуре:
![]() .
Окисление ионов двухвалентного железа
кислородом воздуха стимулирует развитие
коррозии стальных сооружений на открытом
воздухе, так как снижает щелочность
пленки влаги, которой покрыта корродирующая
поверхность и резко уменьшает содержание
в ней ионов двухвалентного железа
(Fe2+):
.
Окисление ионов двухвалентного железа
кислородом воздуха стимулирует развитие
коррозии стальных сооружений на открытом
воздухе, так как снижает щелочность
пленки влаги, которой покрыта корродирующая
поверхность и резко уменьшает содержание
в ней ионов двухвалентного железа
(Fe2+):
![]() .
По мере роста оксидных слоев на
корродирующей поверхности скорость
атмосферной коррозии уменьшается. В
почвенно-климатических регионах с
большой влажностью и высокой температурой,
где, кроме того, воздух загрязнен разного
рода промышленными выбросами, практически
всегда можно предполагать интенсивную
коррозию стальных сооружений. С другой
стороны, в тропической сухой зоне, где
низкая влажность и высокая температура,
скорость атмосферной коррозии минимальна.
Характерным примером является
восьмиметровая железная колонна,
установленная в столице Индии г.Дели
2500 лет тому назад, которая несмотря на
солидный возраст, лишь в незначительной
степени повреждена язвенной коррозией
в нижней части (на высоту 70 см). На этой
высоте во время дождя на колонну попадают
грязные брызги с земли. В целом же своей
долговечностью колонна обязана невысокой
влажности и чистоте окружающего воздуха,
которые способствовали образованию на
колонне плотного защитного слоя.
.
По мере роста оксидных слоев на
корродирующей поверхности скорость
атмосферной коррозии уменьшается. В
почвенно-климатических регионах с
большой влажностью и высокой температурой,
где, кроме того, воздух загрязнен разного
рода промышленными выбросами, практически
всегда можно предполагать интенсивную
коррозию стальных сооружений. С другой
стороны, в тропической сухой зоне, где
низкая влажность и высокая температура,
скорость атмосферной коррозии минимальна.
Характерным примером является
восьмиметровая железная колонна,
установленная в столице Индии г.Дели
2500 лет тому назад, которая несмотря на
солидный возраст, лишь в незначительной
степени повреждена язвенной коррозией
в нижней части (на высоту 70 см). На этой
высоте во время дождя на колонну попадают
грязные брызги с земли. В целом же своей
долговечностью колонна обязана невысокой
влажности и чистоте окружающего воздуха,
которые способствовали образованию на
колонне плотного защитного слоя.
В области низких и умеренных температур коррозионная стойкость стальных сооружений в сухой атмосфере определяется преимущественно кинетическими факторами. Присутствие в атмосфере промышленных загрязнений и воды в виде жидкой или газообразной фазы существенно изменяет физико-химическую природу коррозионного процесса и увеличивает скорость коррозионного разрушения стального сооружения.
Методы защиты металлов от атмосферной коррозии сводятся к следующему:
нанесению защитных покрытий (смазки, лаки, пленки, цинкование, никелирование, хромирование, фосфотирование, окисные пленки);
воздействию на контролирующие процессы (пассивация анода Cr, Al, Ti, Ni, катодные включения Си, Pd);
уменьшению слоя электролита на поверхности стального сооружения (осушка и очистка воздуха);
применение специальных жаростойких сталей Х25Т, Х28, 0Х18Н10;
применению замедлителей коррозии (NaN02, нитриты, карбонаты, бензоаты дициклогексиламина и моноэтаноламина) в основном при хранении металлов и транспортировании их в контейнерах или упаковке из оберточных материалов.
