
- •3.Перетворення Лоренца. Власний час. Додавання швидкостей.
- •2.2. Взаємо- і самоіндукція. Єрс індукції. Магнітна енергія струму
- •2.3. Основні експериментальні фактори, що привели до створення квантової механіки. Фізичний зміст хвильової функції. Умова нормування хвильової функції.
- •1. Теорія Ейнштейна і Дебая для теплоємності твердого тіла.
- •2. Електрорушійна сила. Контактна різниця потенціалів. Термоелектрика.
- •3. Основні ядерні реакції: розщеплення ядер зарядженими частинками та нейтронами. Ядерний фотоефект. Поділ ядер. Штучна радіоактивність.
- •4.1. Число зіткненнь, ефетивний переріз та довжина вільного пробігу молекул.
- •4.3. Будова атома. Дослід резерфорда по розсіювання альфа-частинок. Спектральні закономірності випромінювання світла атомами. Теорія Бора. Спектр водню.
- •2. Рівняння Максвела. Електромагнітні хвилі, хвильове рівняння. Енергія електромагнітних хвиль. Вектор Умова-Пойтінга.
- •3.Теорія Збурень. (Ez volt az 5-ös tétel 3. Kérdése!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!)
- •6.1 Стаціонарні і нестаціонарні явища переносу в газах. Дифузія. Внутрішне тертя. Теплопровідність.
- •6.2 Електростатичний потенціал. Енергія електронного поля.
- •6.3. Будова атомного ядра. Ізотопи. Ізобари. Ізомери. Масспектрографія.
- •7(1). Цикли Карно. Ккд циклів Карно.
- •7(2).Ємність, способи її вимірювання. Ємність різних конденсаторів, послідовне та паралельне їх сполучення.
- •7(3). Атом гелію. Тотожність однакових частинок. Симетричні та антисиметричні стани. Частинки Бозе та частинки Фермі.
- •8(2). Електричне поле. Вектори напруження і зміщення. ТеоремаОстроградського-Гауса.
- •9(1). Розподіл Максвела і Максвела-Больцмана. Бозе-газ. Бозе-конденсація. Статистика Бозе-Енштейна і Фермі-Дірака.
- •9(2). Діелектрики. Електричне поле в однорідному діелектрику. Молекулярна картина поляризації діелектрика.
- •9(3). Досліди Франка і Герца по визначенню потенціального збудження атомів.
- •10(2). Електромагнітна індукція. Закон електромагнітної індукції. Правило Ленца.
- •10(3). Електронні оболонки атома. Магнітний і механічний момент електронів. Квантові числа. Принцип Паулі. Періодична система елементів Менделєєва.
- •1.Статичний метод у фізиці. Стат. Функції розподілу. Статичне середнє. Канонічний розподіл Гібса.
- •2.Дисперсія світла.Нормальна і аномальна дисперсія, методи її спостереження.Електронна теорія дисперсії.
- •3.Енергія зв’язку частинок у ядрі . Дефект маси ядра. Ядерні сили та їх основні властивості.
- •1.Динаміка точки. Закони Ньютона. Закон всесвітнього тяжіння.
- •2.Становлення і розвиток квантової теорії світла. З-ни теплового випромінювання.
- •3.Радіоактивність. З-он радіоакт розпаду. Типи радоакт розпаду. Методи і прилади для спостер елементарних частинок.
- •13.1.Закон збереження кількості руху. Закон збереження і перетворення енергії в механіці в нерелятивістській і релятивіській.
- •13.2. Спонтанне и вимушене випромінювання коефіцієнт Ейнштейна. Механізми процесів у оптично квантових генераторів і підсилювачах.
- •13.3.Теорія основного стану молекулярного водню. Адіабатичне наближення.
- •1.Принципи відносності Галілея та Ейнштейна. Інерціальні системи. Відцентрова та коріолісова сила.
- •2.Дифракція. Принцип Гюйгенца-Френеля. Дифракція Фраунгофера.
- •16.1. Динаміка твердого тіла. Тензор Інерції. Гіроскопи.
- •16.2.Електромагнітна природа світла. Швидкість світла. Астрономічні і лабораторні методи вимірювання швидкості світла.
- •16.3. Термоядерні реакції. Проблеми некерованого термоядерного синтезу.
- •17(1). Рівняння руху та інтегральні варіаційні принципи. Принцип найменшої дії. Основи релятивіської механіки.
- •17(2). Гази з міжмолекулярними взаємодіями. Рівняння Ван-дер-Вальса.
- •17(3). Поляризаційні прилади. Пластинки в четвертину хвилі і в півхвилі. Обертання площини поляризації.
- •19(1). Власні і вимушені коливання з однією ступенню вільності. Резонанс коливання зв’язаних систем. Розповсюдження коливань в густому середовищі.
- •19(2). Поняття про голографію і її застосування.
- •19(3). Елементарні частнки, протони, нейтрони, позитрони, гіперони, античастинки .Поняття про кварки і глюони. Кваркова структура адронів.
- •1. Особливе місце фізики серед інших наук і ї зв’язок з виробництвом.
- •2. Основи мкт газів. Теорема Нернста. Абсолютна термодинамічна шкала температур.
- •3. Люмінесценція та її застосування.
- •1. Предмет і завдання фізики. 4 типи взаємодії.
- •2. Принцип суперпозиції. Інтерференція світла. Експериментальне вивчення інтерференції світла.
- •3. Експериментальні методи визначення швидкості газових молекул. Методи визначення числа Авогадро.
- •1. Експерименталльне і математичне формулювання фундаментальних законів механіки.
- •2. Подвійне променеве заломлення.
- •3. Принцип відносності. Шв-сть розпосюдження взаємодії.
БІЛЕТ 1
1. Фазовий перехід 1-го та 2-го роду. Залежність температури фазового переходу 1- го роду від тиску. Рівняння Клапейрона-Клаузіуса.
Фаза – це однорідна частина термодинамічної системи властивості якої однакові в усіх напрямках. Фазові переходи – це переходи речовини з однієї фази в іншу. Фазовий перехід 1-го роду супроводжуються стрибко подібною зміною внутрішньої енергії та густини і пов”язані з виділенням теплоти. Тиск і температура протягом усього фазового переходу 1-го роду залишається сталим. Плавлення твердого тіла в кристалічному стані відбуваються при певній але незмінній протягом плавлення температурі. Питома теплота плавлення Q = Up – UT + p(VP – VT) де Up, UT – внутрішні енергії одиниці маси рідини і твердої фази. VP і VT питомі об”єми рідини і твердого тіла, P – сталий тиск газового переходу. Температура плавлення залежить від тиску:
![]()
Якщо об”єм речовини в рідкому стані перевищує її об”єм у твердому стані, то Т/Р 0, тобто із зростанням тиску підвищується температура плавлення. Фазовий перехід 2-го роду не пов”язаний із зміною густини внутрішньої енергії та виділенням тепла, але пов”язані з зміною теплоємності і внутрішньої будови. При цих переходах стан тіла змінюється плавно а симетрія стрибком
Т
Р
Фп1
Фп2


Рівняння Клапейрона-Клаузіуса – Термодинамічне співвідношення яке встановлює зв”язок між зміною тиску і зміною температури по кривій фазового переходу 1-го роду для чистого матеріалу
![]() де р –
тиск, Т – абсолютна температура Q
– теплота фазового переходу. Фазовий
перехід який супроводжується збільшенням
об”єму V
0 і випаровування, та підвищенням теплоти
Q
0 супроводитиметься збільшенням тиску
насиченої пари (бо Р/Т
0). При плавленні похідна
де р –
тиск, Т – абсолютна температура Q
– теплота фазового переходу. Фазовий
перехід який супроводжується збільшенням
об”єму V
0 і випаровування, та підвищенням теплоти
Q
0 супроводитиметься збільшенням тиску
насиченої пари (бо Р/Т
0). При плавленні похідна
![]() може бути додатньою для більшості
речовин та від”ємною (для води, вісмуту,
чавуну). В останніх об”єм рідини менший
від об”єму твердої фази, тому збільшення
тиску приведе до зниження точки плавлення.
Для низьких тисків коли приріст об”єму
V
дорівнює об”єму парової фази рівняння
К-К набуває вигляду
може бути додатньою для більшості
речовин та від”ємною (для води, вісмуту,
чавуну). В останніх об”єм рідини менший
від об”єму твердої фази, тому збільшення
тиску приведе до зниження точки плавлення.
Для низьких тисків коли приріст об”єму
V
дорівнює об”єму парової фази рівняння
К-К набуває вигляду![]() . Рівняння К-К застосовують для застосунку
певних параметрів речовини при фазових
переходах.
. Рівняння К-К застосовують для застосунку
певних параметрів речовини при фазових
переходах.
2.Основи електронної теорії металів, діелектриків напівпровідників. Надпровідність.
Надпровідність – явище різкого зменшення електричного опору деяких металів (сплавів, сполук) при температурі близькій до абсолютного нуля. Експериментальні вимірювання показали, що при надпровідності питомий опір менший за 10 –25 Ом·м. Вперше надпровідність спостерігали в 1911 р. на ртуті. Надпровідність характеризується не тільки майже зникненням електронного опору зразка, а й одночасно зміною його магнітних і теплових параметрів. Діелектрики – речовини в яких концентрація вільних носіїв струму дуже мала, а тому вони не проводять струм. Такі речовини можуть перебувати в різних агрегатних станах про те речовина буває дієлектриком за певних умов, а при інтенсивних впливах (іонізації, фотоіонізації, термодисоціації) може стати напівпровідником, або провідником. Проникність діелектрика залежить від швидкості зміни зовнішнього поля. Кожен діелектрик характеризується напругою пробою, яка веде до лавинного зростання струму крізь діелектрик. Метали – речовини які в конденсованому стані характеризуються великою питомою електропровідністю. З підвищенням температури електропровідність металів зменшується. Метали – це переважна більшість хімічних елементів. У твердому стані метали є кристалами переважно з щільною упаковкою атомів. При внесені металів в електричне поле електрони легко зміщуються утворюючи струм. Напівпровідники – Широкий клас речовини, які засвоєю електропровідністю займають проміжне місце між металами і діелектриками. Напів провідники мають такі основні властивості:
Їхня електропровідність а одже і концентрація носіїв струму сильно залежить від зовнішніх впливів(температури, випромінювання, домішки та ін.)
З підвищенням температури електропровідність напівпровідників різко зростає;
Електропровідність не пов язана з перенесенням речовини і має електронний механізм;
Провідність напівпровідникі залежить, як від концентрації дирок або електронів так і від рухливості їх. Напівпровідники досить поширенні у природі. Поділяються на: атомарні (германій, алмаз) іонні (сульфіди свинцю або цинку) молекулярні (селен, нафталін. Серед напівпровідників можуть бути рідини і аморфні речовини. Застосовуються у техніці (діоди, тріоди, терморезистори, детектори, підсилювачі).
3.Перетворення Лоренца. Власний час. Додавання швидкостей.
Перетворення Лоренца – це сукупність формул за якими треба перетворювати координати і час подій в одній інерціальній системі щоб правильно описати її в іншій інерціальній системі. Відповідно до спеціальної теорії відностності Перетворення Лоренца дають перехід від однієї інерціальної системи відліку до іншої, пов”язують фізичні величини в двох інерціальних системах відліку коли рухома система відліку зберігаючи паралельність відповідних осей рухається вздовж осі ОХ, ці формули мають вигляд:
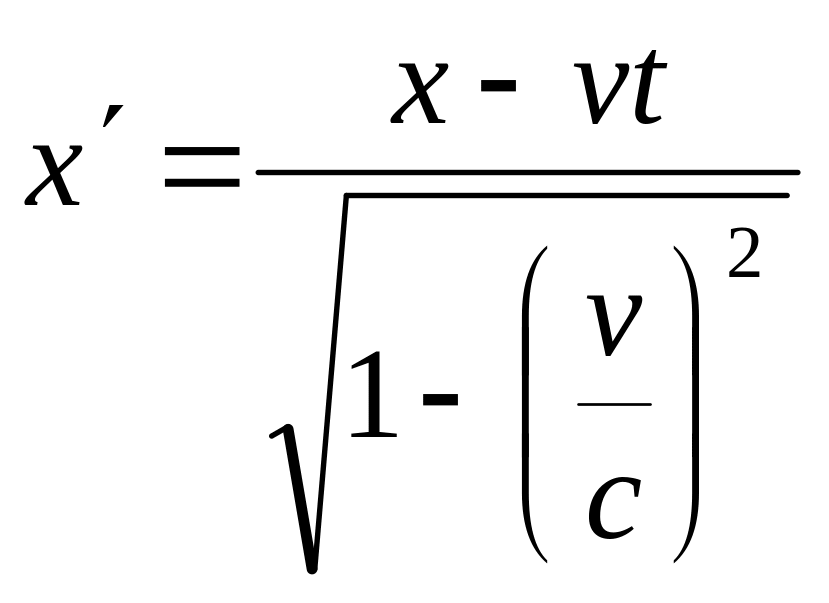 ;
;
![]()
![]() ;
;

Де
v
– переноснашвидкість рухомої системи,
с – швидкість світла у вакуумі, x,y,z,t
– координати і час події в нерухомій
системі відліку,
![]() ,
,
![]() ,
,![]() ,
,
![]() - в рухомійсистемі відліку. Формули
Лоренца втрачають свій зміст коли v
= c
.
Оскільки тоді в знаменнику з”являється
нуль а ділення на нуль неможливе. Це
означає, що ніякі 2 системи відліку
неможуть мати відносну швидкість яка
б дорівнювала швидкості світла. Власний
час – час Δ
t
′ який
відлічується годиником що рухається
разом з рухомим об”єктом або системою
відліку в якій годинник нерухомий. Якщо
інерціальна система К умовно нерухома,
а відносно неї рухається інша інерціальна
система відліку К′ (з якою нерухомо
зв”язаний годинник з відносною швидкістю
v
то час Δ
t
′ показаний цим годинником менший від
часу Δ
t
який показують годинником в системі К
- в рухомійсистемі відліку. Формули
Лоренца втрачають свій зміст коли v
= c
.
Оскільки тоді в знаменнику з”являється
нуль а ділення на нуль неможливе. Це
означає, що ніякі 2 системи відліку
неможуть мати відносну швидкість яка
б дорівнювала швидкості світла. Власний
час – час Δ
t
′ який
відлічується годиником що рухається
разом з рухомим об”єктом або системою
відліку в якій годинник нерухомий. Якщо
інерціальна система К умовно нерухома,
а відносно неї рухається інша інерціальна
система відліку К′ (з якою нерухомо
зв”язаний годинник з відносною швидкістю
v
то час Δ
t
′ показаний цим годинником менший від
часу Δ
t
який показують годинником в системі К
![]() < Δ
t
.
< Δ
t
.
одже власний час рухомого об”єкту завжди менший ніж відповідний проміжок часу в нерухомій системі, а рухомий годинник іде повільніше ніж нерухомий. Нехай у двох системах відліку К і К′ вивчається рух тіла яке переміщується прямолінійно і рівномірно паралельно осям х і х′ обох систем відліку. Нехай швидкість тіла визначена в системі К є u а швидкість того самого тіла визначена в системі К′ рівна u′ . Швидкість системи К′ відносно К позначимо v. Тоді Релятивіська формула додавання швидкостей:
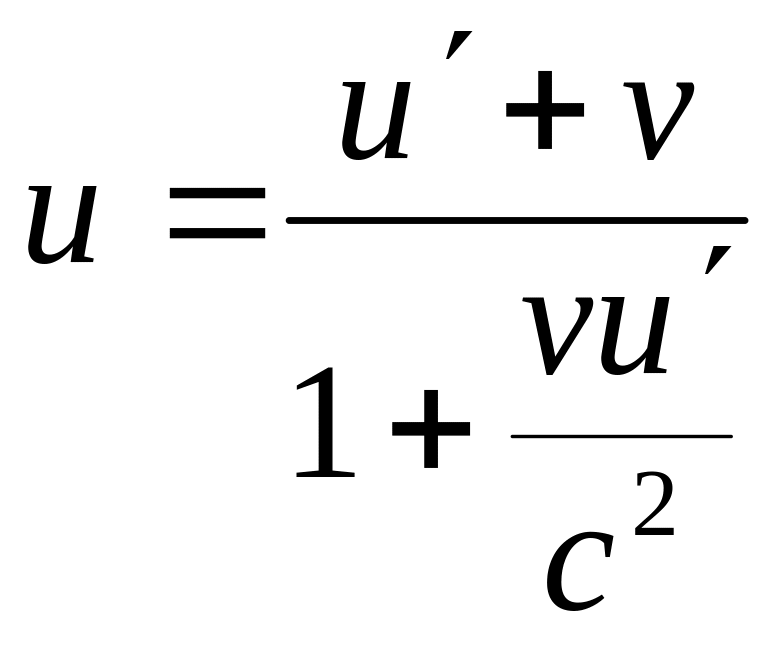 .
.
БІЛЕТ 2
2.1. 2-ий принцип ТД. Ентропія. Статистичне тлумачення 2-го принципу ТД.
Формулювання Клаузіуса: Теплота неможе самодовільно переходити від більш холодного до більш нагрітого тіла. Формулювання Томсона: Неможливий циклічний двигун який б виконував роботу лише за рахунок охолодження джерела. Формулювання Больцмана: природа прямує від стані зменш імовірного до стані більш імовірного. Ентропія є функцією стану системи, диференціал якої в елеиентарному оборотномук процесі рів відношенню нескінч малої к-сті теплоти, приведеної до стану, до абсол Т-рі. dS = dq/T, при скінченому оборотному процесі S1-S2=?dQ/T. Це твердження справедливе для системи, яка знаходиться при постій температурі і виконує перехід в інший стан завдяки тепловій взаємодії dq. Фіз. зміст етропії: люба сист яку залишаємо на саму себе буде прямувати до рівноважного стану. Рівноважний стан є найбільш імовірним і ентропія буде максималь. Ентропія визначає напрям протікання природничних процесів. Л.. Больцман виявив звязок між Ен. і імовірністю S=klnw w – ТД-на імовірність.
