
- •Содержание
- •Тканевый уровень организации …………………………….…78
- •3.Свойства живых организмов
- •4.Уровни организации живого
- •1. Биологические молекулы. Последовательность молекулярной организации клеток
- •2 Биологическая специфика молекулярного уровня
- •1 История изучения клетки
- •2 Основные положения: современной клеточной теории
- •3 Типы существующих клеток и их общая структура.
- •Строение биологических мембран.
- •Функции биологических мембран. Транспорт через мембрану
- •Транспортная функция мембран
- •Строение животной и растительной клетки
- •7 Ядерный аппарат клетки и рибосомы.
- •Мембранные органоиды клетки
- •Питание клетки. Фагоцитоз и пиноцитоз.
- •1. Эпителиальная ткань.
- •2. Соединительные ткани
- •5. Мышечная ткань
- •6. Нервная ткань
- •2.Периоды онтогенеза
- •3 Старение организма и продолжительность жизни.
- •3. Наследственность и изменчивость и методы их изучения.
- •2 Роль и значение микроорганизмов вокруг нас.
- •3 Отличительные признаки прокариот и эукариот
- •4 Грибы. Строение клетки и тела гриба. Способы размножения грибов.
- •5 Элементы классификации грибов. Представители низших грибов, особенности их строения.
- •6 Аскомицеты. Дрожжи.
- •7 Несовершенные грибы
- •5. Поверхностные структуры бактерий
- •6.Капсула бактерий
- •Клеточная стенка
- •Биологическая химия
- •1. Основы химии
- •Строение атома
- •1.1.1. Ионная связь
- •1.1.2 Ковалентные связи
- •1.1.3. Химические уравнения
- •1.1.4 Кислоты, основания, соли, рН и буферы
- •Окисление и восстановление
- •1.2.1 Окисление
- •1.2.2 Восстановление
- •1.4 Растворы и коллоидное состояние
- •1.5 Диффузия и осмос
- •1.5.1 Диффузия
- •1.6. Законы термодинамики
- •1.6.1 Энергетические соотношения в живых системах
- •1.6.2 Потенциальная энергия
Биологическая химия
1. Основы химии
Атом — это мельчайшая частица любого элемента, способная принимать участие в химических реакциях.
Элементом называется вещество, которое не может быть расщеплено химическими методами на более простые вещества; к элементам относятся, например, углерод, кислород и азот.
Вещество, состоящее из двух или нескольких химически связанных элементов, называется соединением, например:
Соединение Элементы
Вода Водород и кислород
Глюкоза Углерод, водород и кислород
Хлорид натрия Натрий и хлор
Молекула — это наименьшая частица данного элемента или соединения, способная самостоятельно существовать при обычных условиях. В качестве примеров молекул можно привести следующие: Н2, С2, СО2, Н2О.
Строение атома
Все элементы состоят из атомов. Слово «атом» происходит от греческого аtоmоs, что значит «неделимый».
В состав атома входят протоны, нейтроны и электроны (табл. 1.). Массы протонов и нейтронов равны и в сумме составляют массу атомного ядра. Масса электронов во много раз меньше, чем масса протонов и нейтронов, поэтому под массой атома подразумевают только массу его ядра.
Нейтрон состоит из одного протона и одного электрона, поэтому он электрически нейтрален, т. е. его заряд равен нулю.
Таблица 1. Положение в атоме, масса и заряд протонов, нейтронов и электронов

Атом электрически нейтрален, потому что число протонов в его ядре равно числу электронов, движущихся вокруг ядра.
Число протонов в ядре атома называется атомным номером данного элемента. Он также равен числу электронов этого атома. Сумма числа протонов и числа нейтронов данного атома называется его массовым числом.
Таблица 2. Первые 20 элементов (в порядке возрастания их атомных номеров)
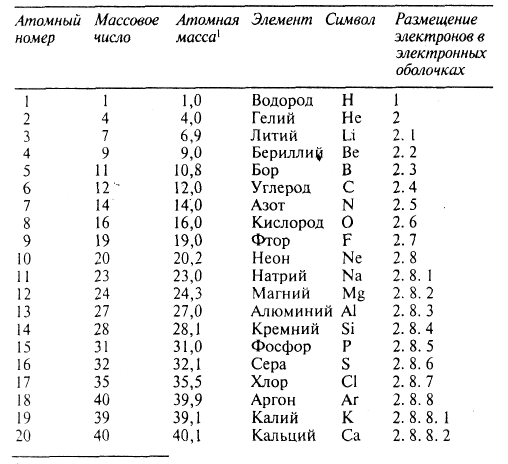
Атомы одного и того же элемента существуют в разных формах, называемых изотопами, которые отличаются друг от друга массовым числом. Атомной массой называют среднюю массу данного атома; обычно под этим понимается средняя величина для природной смеси его изотопов. Хлор, например, представляет собой смесь изотопов с массовыми числами 35 и 37; соотношение этих изотопов таково, что у встречающегося в природе хлора атомная масса равна 35,5.
В настоящее время известно свыше 100 элементов. Их можно расположить в порядке возрастания атомных номеров, как это сделано в таблице 2.
Атомная масса называлась раньше атомным весом. Величины атомных масс даны до первого десятичного знака. Ниже перечислены (в порядке возрастания их атомных номеров) некоторые наиболее известные элементы и указаны их символы: хром (Сr), марганец (Мn), железо (Fе), кобальт (Со), никель (Ni), медь (Сu), цинк (Zn), мышьяк (Аs), бром (Вr), молибден (Мо), серебро (Аg), кадмий (Сd)), иод (I), барий (Ва), платина (Рt), ртуть (Нg), свинец (Рb), радий (Rа), уран (U), плутоний (Рu).
Как видно из этой таблицы, электроны размещаются вокруг ядра, заполняя ряд электронных оболочек. В первой электронной оболочке (ближайшей к ядру и потому наименьшей) могут удерживаться два электрона, во второй — до восьми, в третьей — до 18 и в четвертой — до 32.
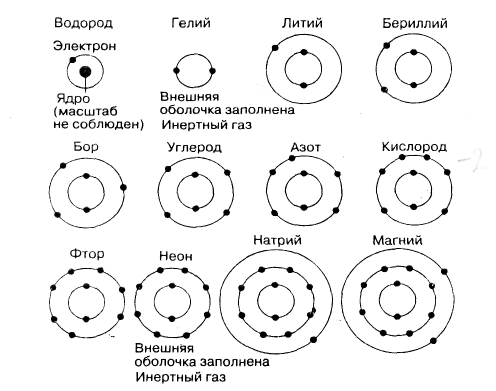
Рис. 1. Размещение электронов в электронных оболочках первых 12 элементов. (Ядро показано только у атома водорода.)
У более крупных атомов число электронных оболочек больше четырех. На рис. П. 1.1. представлено размещение электронов в электронных оболочках первых 12 элементов.
Любой элемент, у которого внешняя электронная оболочка заполнена целиком, практически нереакцион-носпособен. По этой причине гелий и неон (табл. П. 1.2) крайне редко вступают в соединение с другими атомами. Вследствие этого их называют инертными или благородными газами.
Все прочие элементы стремятся заполнить свои электронные оболочки, вступая в реакцию с другими элементами. Когда два атома реагируют друг с другом, между ними может возникнуть либо ионная, либо ковалентная связь.
