
- •З біологічної хімії
- •Рецензент проф. В.Д. Бовт
- •Питання до іспиту……………………………………………………………… 79
- •Тематичне розподілення навчального матеріалу а. Тематичне розподілення лекційного матеріалу
- •В. Тематичний план лабораторних і семінарських занять
- •Техніка безпеки при роботі у біохімічній лабораторії
- •Забороняється з метою уникнення травм, опіків, нещасних випадків:
- •Перша домедична допомога
- •Вимоги до оформлення лабораторного журналу і робочого місця
- •Теоретична частина:
- •Практична частина:
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Практична частина:
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Цитозін
- •Практична частина:
- •Контрольні питання
- •Теоретична частина:
- •Властивості ферментів:
- •Реакція
- •Практична частина:
- •Теоретична частина:
- •Практична частина:
- •Контрольні питання
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Тканьовий подих
- •Практична частина:
- •Контрольні питання
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Катаболізм амінокислот:
- •Біосинтез сечовини (орнітиновий цикл)
- •Практична частина:
- •Теоретична частина:
- •Практична частина:
- •Питання до семінарського заняття:
- •Теоретична частина:
- •Взаємний зв'язок різних форм обміну речовин в організмі
- •Практична частина
- •Контрольні питання
- •Питання до семінарського заняття:
- •Питання до іспиту
- •Список рекомендованої літератури
- •Практикум з біологічної хімії до лабораторних і семінарських занять для студентів біологічного факультету денної та заочної форм навчання
Перша домедична допомога
-
Відключити електричний струм, що діє на постраждалого; загасити спиртовий пальник; якщо зайнявся одяг, то необхідно накрити ділянку, що горить, підручним предметом (рушник, халат, піджак) або постраждалий має лягти на підлогу і перекочуватися, намагаючись загасити вогонь. Після цього постраждалому надати медичну допомогу.
2. При відсутності після електротравми у постраждалого пульсу і дихання, терміново здійснюють штучне дихання з рота в рот і закритий масаж серця (на одне вдмухування 4-5 натиснень на нижню третину грудини; ритм - одне натиснення на секунду).
3. Перев'язувальні матеріали (вата, бинти, серветки), необхідні розчини і медикаменти знаходяться в аптечці, встановленій у лабораторії.
4. При термічних опіках зробити примочки розчином перманганата калію або етилового спирту і змазати маззю від опіків.
5. При опіках кислотою старанно промити обпалене місце спочатку проточною водою, а потім обробити розчином гідрокарбонату натрію.
6. При опіках їдкими лугами промити обпалене місце водою, а потім обробити розведеною оцтовою кислотою.
7. Якщо кислоти або луги потраплять у очі, слід миттєво їх промити дистильованою водою, а потім обробити 1 % розчином гідрокарбонату натрію у випадку потрапляння кислоти або 1 % розчином борної кислоти при потраплянні лугу, після чого знову старанно промити дистильованою водою.
8. При порізах склом видалити скалки з рани, змазати йодною настойкою і, якщо потрібно, накласти пов'язку.
9. При отруєнні парами отрути, постраждалого винести на свіже повітря, дати 30 крапель кардиаміну, міцний чай або каву.
Вимоги до оформлення лабораторного журналу і робочого місця
1. Студенти ведуть лабораторні журнали, в яких описаний хід роботи, механізм реакцій і роблять висновки за виконаними дослідженнями.
2. На титульному аркуші журналу студенти пишуть прізвище й ініціали, назву факультету, номер курсу і групи.
3. Всі спостереження і висновки за експериментальними роботами оформляються у вигляді таблиці, що містить графи, зазначені в лабораторних роботах, у даній методичній вказівці.
4. Робочий журнал наприкінці заняття студенти здають викладачеві для підпису.
5. Після закінчення роботи старанно вимити посуд, яким користувалися, закрити газові й водопровідні крани, виключити електроприлади, відключити електрику, упорядкувати робоче місце і лабораторію.
Зміст лабораторного заняття:
1. Контроль засвоєних знань з теми (див. залікові питання з теми).
2. Заняття.
3. Контроль виконання лабораторної роботи.
Заняття № 1.
Тема: ЯКІСНІ (КОЛЬОРОВІ) РЕАКЦІЇ НА білки та
АМІНОКИСЛОТИ
Теоретична частина:
Вивчення біохімії доцільно почати саме із цього розділу, оскільки білки мають особливо важливе значення для процесів життєдіяльності.
Білки, або протеїни, - азотовмісні полімерні органічні сполуки великої молекулярної ваги, які мають специфічну тримірну структуру (конформацію) і розпадаються при гідролізі на α-амінокислоти. Студент повинен знати фізико-хімічні властивості білків: молекулярна вага, амфотерність, ізоелектрична крапка, розчинність, колоїдний характер водяних розчинів білків, осадження та кристалізацію білків.
Переходячи до хімічного складу й будови білків, треба насамперед знати будову і властивості амінокислот. Структурними елементами, з яких складаються білки, являються двадцять -амінокислот. Усі амінокислоти, які входять до складу білків, являються амінопохідними карбонових кислот, у яких один атом водню в радикалі біля -вуглецевого атома заміщений на аміногрупу. Наприклад:
пропіонова
кислота

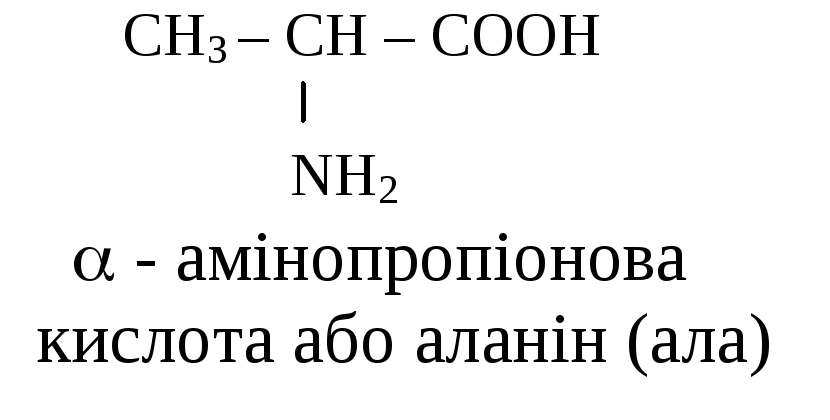
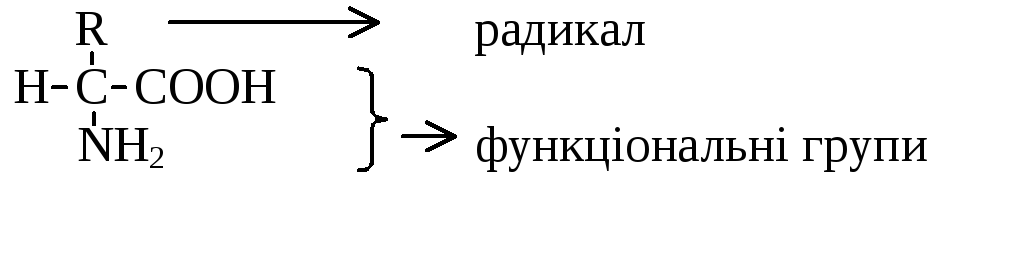
Амінокислоти існують переважно у вигляді біполярних іонів (цвітеріонів):
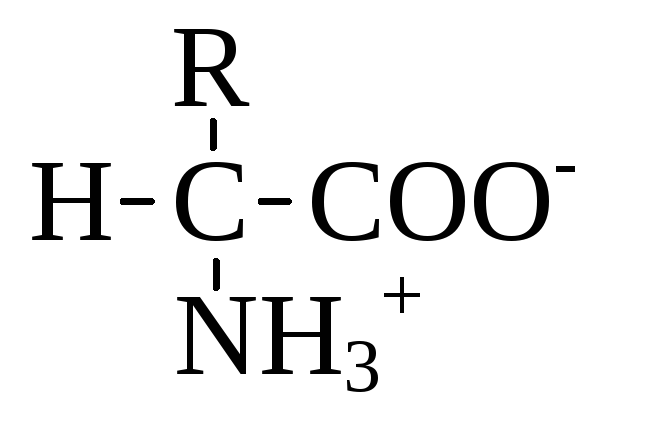
R-групи амінокислот мають різну хімічну структуру і багато в чому визначають хімічні і фізичні властивості білків. Існують різноманітні способи класифікації амінокислот, серед яких найбільш раціональним варто визнати спосіб, заснований на розходженнях у полярності R-груп. Всі амінокислоти діляться на чотири класи.
1 клас - неполярні, або гідрофобні: аланін, лейцин, ізолейцин, валін, пролін, фенілаланін, триптофан, метіонін.
2 клас - полярні, але незаряджені: гліцин, серін, треонін, цистеїн, тирозин, аспарагін, глютамін.
3 клас - негативно заряджені (кислі): глютамінова і аспарагінова кислоти.
4 клас - позитивно заряджені (основні): лізин, аргінін, гістидин.
У залежності від природи радикалу відрізняють також амінокислоти аліфатичного та циклічного рядів.
Деякі амінокислоти не можуть синтезуватися в організмі людини та повинні поступати разом із їжею. Їх називають незамінними. До них відносяться: валін, ізолейцин, лейцин, лізин, метіонін, треонін, триптофан, фенілаланін, тирозин, цистеїн. Інші амінокислоти в організмі синтезуються і їх називають замінними: аланін, аспарагін, аспарагінова кислота, гідроксилізин, гідроксипролін, гліцин, глютамінова кислота, глютамін, пролін, серін. Наполовину замінні: аргінін, гістидин.
Амінокислоти мають амфотерні властивості та можуть виступати у ролі як кислот, так і основ.
Повний (сумарний) заряд (алгебраїчна сума всіх позитивних та негативних зарядів) амінокислоти залежить від рН, тобто, від концентрації протонів в оточуючому розчині. Значення рН, при якому сумарний заряд амінокислоти дорівнює нулю й тому вона не переміщується у постійному електричному полі, називається її ізоелектричною крапкою.
