
lekcii dlya zaochnogo farmfakulteta
.pdf
При мембраногенных отеках основным средством терапии являются препараты, снижающие сосудистую проницаемость. Таким эффектом обладают АКТГ, грюкокортикоиды и другие противовоспалительные препараты. При аллергических отеках применяются антигистаминные препараты.
Ãидростатические (застойные) отеки. Если главную роль в патогенезе отека играет повышение ЭГД, то такие отеки называют гидростатическими. Они возникают при местной венозной гиперемии (венозном застое). При этом в зависимости от степени повышения давления в венозном отделе капилляра резорбция интерстициальной жидкости либо снижается, либо даже прекращается (когда ЭГД становится равным, либо даже превышает ЭОД).
Одним из экспериментальных доказательств правомочности этого заключения являются опыты с перевязкой или пережатием некоторых вен, имеющих незначительное количество коллатералей. Например, при зажатии венозного сплетения семенного канатика очень быстро развивается отек тестикул; при зажатии венозного синуса сердца быстро развивается водянка перикарда. Считается, что гидростатический механизм играет существенную роль во многих случаях, когда создаются условия для развития венозной гиперемии. Поэтому отеки при флеботромбозах, тромбофлебитах, застойной сердечной недостаточности относятся к гидростатическим (механическим). Вместе с тем известно, что увеличение гидростатического давления в артериальной части капилляра, характерное для артериальной гиперемии, как правило, не приводит к развитию отека. В этих условиях увеличение транссудации компенсируется усилением резорбции интерстициальной жидкости через лимфососуды.
Компенсаторное увеличение лимфооттока наблюдается при перевязке венозных сосудов при моделировании венозной гиперемии, характерным признаком которой (в отличие от артериальной) является развитие отека окружающих тканей.
Дальнейшее исследование этого различия показало, что в патогенезе застойных отеков принимает участие не только гидростатический фактор, но и некоторые другие. Так как венозная гиперемия приводит к гипоксии тканей (чего нет при артериальной), то она сопровождается увеличением проницаемости сосудистой стенки, поэтому к гидростатическому механизму подключается мембраногенный. Кроме того, при длительной венозной гиперемии развивается комплекс метаболических изменений, характерных для гипоксии тканей. В этих условиях на фоне резкого усиления катаболических процессов в тканях и тканевого ацидоза увеличивается молекулярная и ионная концентрация интерстиция, что сопровождается повышением осмотического давления, которое начинает превышать осмотическое давление плазмы крови. Повышение осмолярности тканевой жидкости включает, так называемый, осмотический механизм перемещения воды в строну повышенного осмотического давления тканей.
Следовательно, в патогенезе застойных отеков принимает участие не только гидростатический, но и мембраногенный, осмотический и лимфатический
71
механизмы. По сути эти отеки являются смешанными, но в ряде случаев при доминировании гидростатического фактора.
Повышение тканевого осмотического давления, вызванное повреждением тканевых элементов, имеетместо также в случае токсических и воспалительных отеков, когда вследствие превращения и распада клеток сложные комплексы различных молекул (в том числе и белковых) распадаются на более простые молекулы, поэтому молекулярная и ионная концентрация в тканях (а следовательно и осмотическое давление) повышается.
Таким образом, с позиций участия местных сосудисто-тканевых факторов отеки подразделяются на мембраногенные, лимфогенные, онкотические, гидростатические и осмотические.
Анализ встречающихся в клинической практике генерализованных форм отеков показал, что они в конечном счете являются смешанными по патогенезу
èразвиваются еще и с участием факторов, регулирующих водноэлектролитный баланс на уровне целостного организма.
Известно, что регуляция постоянства жидких сред организма, величины осмотического давления и объема осуществляется взаимодействием двух механизмов: антидиуретического и антинатрийуретического.
Антидиуретический механизм представлен антидиуретическим гормоном (АДГ), он имеется в нейрогипофизе, а его синтез и секреция осуществляется нейронами супраоптического и паравентригулярного ядер гипоталамуса. АДГ усиливает реабсорбцию воды из дистальных отделов канальцев нефронов. При повышении осмотического давления (например, в условиях повышенного потребления натрия) АДГ обеспечивает задержку воды и восстановление осмолярности жидкости.
Антинатрийуретический механизм представлен альдостероном, продукция которого происходит в клубочковой зоне коры надпочечников. Усиленное образование его наблюдается при гиповолемии, гипонатриемии, гипотензии, что зависит от стимуляции осмо-, баро- и волюменрецепторов (рецепторы объема). Адекватным раздражителем волюменрецепторов являются изменения объемов жидких сред организма (главным образом объема циркулирующей крови). Стимулируют секрецию альдостерона ренин и ангиотензин, продукция которых существенно зависит от интенсивности почечного кровообращения. Альдостерон усиливает реабсорбцию натрия в проксимальных отделах канальцев нефронов. При гипернатриемии выделение альдостерона тормозится, что снижает реабсорбцию натрия, и повышенное ранее осмотическое давление нормализуется. Наоборот, при гипонатриемии за счет гиперпродукции альдостерона выведение натрия через почки ограничивается, что устраняет гипоосмию.
Существует тесное взаимодействие между механизмами антидиуретической
èантинатрийуретической рагуляциями. Например, при потере жидкости организмом через волюменрецепторы стимулируется секреция альдостерона, за счет чего происходит задержка натрия и повышается осмолярность внеклеточной жидкости. Раздражение осморецепторов стимулирует секрецию
72
АДГ, что ограничивает диурез, а задерживающаяся жидкость устраняет гиповолемию и одновременно восстанавливается осмолярность внеклеточной жидкости.
Таким образом, взаимодействие этих механизмов обеспечивает адаптивные реакции, направленные на поддержание водного и электролитного равновесия организма. Однако в условиях патологии эти же механизмы могут функционировать неадекватно так, что их эффекты не устраняют, а, наоборот, усиливают нарушение водно-электролитного обмена и стимулируют развитие отеков. Такая ситуация возникает в частности при развитии сердечных и почечных отеков.
Сердечные отеки. Эти отеки развиваются у больных с сердечной недостаточностью. При левожелудочковой недостаточности может развиваться кардиогенный отек легких, при правожелудочковой - отеки развиваются, как правило, на нижних конечностях, туловище, часто развивается асцит.
Патогенез этих отеков представлен на схеме 2 и включает в себя:
-гидростатический механизм, так как повышается центральное венозное
èгидротическое давление в венозных отделах капилляров;
-лимфогенный механизм, так как при повышении центрального венозного давления и спазме лимфососудов лимфоотток затрудняется;
-мембраногенный механизм, так как на фоне гипоксии тканей могут появляться факторы, повышающие проницаемость сосудов;
-осмотический механизм, зависящий, с одной стороны, от усиления катаболических процессов в тканях, характерных для их гипоксии, а, с другой, - с развитием вторичного гиперальдостеронизма, что приводит к активной задержке натрия и через стимуляцию АДГ – к задержке воды.
Последнему механизму принадлежит важное значение в развитии сердечных отеков. Во-первых, известно, что развитие этих отеков может предшествовать повышению венозного давления и развитию застойных явлений. Во-вторых, сердечный отек часто удается ликвидировать только с помощью антагонистов альдостерона. Сходным эффектом обладают препараты, ингибирующие образование или эффекты ангиотензина. Тем не менее, коррекция застойных отеков у больных с сердечной недостаточностью должна быть направлена на устранение ведущего патогенетического фактора, т.е. на восстановление сократительной функции сердца и нормализацию показателей системного кровообращения.
Почечные отеки. Различают две разновидности отеков при заболеваниях почек, приводящих к их недостаточности: нефротические и нефритические. При так называемом нефротическом синдроме (преимущественное поражение канальциевого аппарата) развивается массивная потеря белка с мочой (гиперпротеинурия). Это приводит к гипопротеинемии и гипоонкии крови. Снижение онкотического давления в сосудистом русле включает онкотический механизм отека, потому увеличивается транссудация жидкости из капилляров
èограничивается ее резорбция в сосудистое русло из тканей. Развивается гиповолемия, что является стимулом для включения нейроэндокринных
73
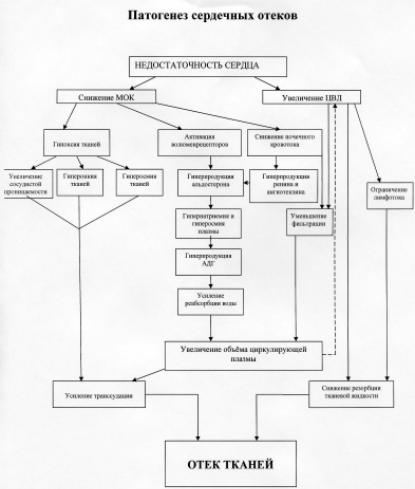
Схема 2
74
механизмов (с участием волюмен- и осморецепторов), усиливающих задержку натрия и воды, что направленно на восстановление объема циркулирующей крови. Но так как при этом онкотическое давление плазмы не повышается (и даже может за счет гемодилюции снижаться), то жидкость в сосудистом русле не удерживается и снова перемещается в интерстициальное пространство, поэтому отек нарастает. По мере развития нефротических отеков к указанным механизмам присоединяется и лимфатический (перегрузка лимфооттока и сдавление лимфатических сосудов отечной жидкостью), что в еще большей степени стимулирует их развитие.
Нефритические отеки наблюдаются при заболеваниях почек с преимущественно диффузным поражением клубочкового аппарата воспалительного или аллергического происхождения.
В олигурической стадии при остром глюмерунефрите в развитии отеков участвует несколько факторов:
-уменьшение величины клубочковой фильтрации, что само по себе может приводить к задержке воды и солей в организме;
-активация продукции альдостерона и антидиуретического гормона, что зависит от снижения почечного кровотока, усиления продукции ренина и ангиотензина;
-генерализованное повышение сосудистой проницаемости (генерализованный капиллярит), что связывают с влиянием токсических и биологически активных веществ, задерживающихся в организме при недостаточности их экскреции с мочой.
Особенностью почечных отеков является их локализация преимущественно на лице. В тяжелых случаях отеки становятся генерализованными, поэтому на фоне анурии у больных может развиться отек всего тела (анасарка), сочетающийся с накоплением жидкости в полостях тела (асцит, гидроторакс, гидроперикардиум). Может развиваться отек легких
èмозга.
Основными принципами терапии отеков являются:
-устранение причины, вызвавшей развитие отека (по возможности);
-снижение секреции альдостерона путем использования его антагонистов;
-снижение эффектов активации синтеза АДГ – назначение диуретиков (фуросемид);
-ограничение водной и солевой нагрузки;
-воздействия на ведущие звенья патогенеза, специфические для различных видов отеков.
75

НАРУШЕНИЯ РЕГИОНАРНОГО КРОВООБРАЩЕНИЯ
К местным расстройствам регионарного кровообращения относят: артериальную гиперемию, венозную гиперемию, ишемию, стаз.
1. Артерильная гиперемия
Артериальная гиперемия - это увеличение кровенаполнения органа или ткани за счет избыточного поступления крови по артериальным сосудам.
Виды артериальных гиперемий:
1.Физиологическая артериальная гиперемия возникает под действием обычных физиологических раздражителей (увеличение нагрузки на орган, психогенные воздействия). К физиологической гиперемии относят рабочую и реактивную гиперемию. Рабочая гиперемия - это увеличение кровотока в органе, сопровождающее усиление его функции (например, гиперемия скелетной мышцы во время ее сокращения, прилив крови к головному мозгу при психической нагрузке). Реактивная гиперемия представляет собой увеличе- ние кровотока после его кратковременного ограничения.
2.Патологическая артериальная гиперемия возникает под действием патогенных раздражителей (химические вещества, токсины, продукты нарушенного обмена, образующиеся при воспалении или ожоге, лихорадка, механические факторы). В зависимости от фактора, вызывающего патологическую артериальную гиперемию, различают, например, воспалительную, тепловую гиперемию, ультрафиолетовую эритему.
Этиология и патогенез. Причинами являются различные факторы внешней среды, включая биологические, физические, химические; увеличение нагрузки на орган или участок ткани, а также психогенные воздействия.
Выделяют три основных механизма артериальных гиперемий:
1.Нейрогенная артериальная гиперемия нейротонического типа
может возникать рефлекторно в органах и тканях, сосуды которых иннервируются парасимпатическими нервными волокнами (язык, наружные половые органы). Симпатические холинэргические нервы расширяют мелкие артерии и артериолы скелетных мышц, мышц лица, слизистой оболочки щек, кишок. Их медиатором также является ацетилхолин.
2.Нейрогенную артериальную гиперемию нейропаралитического типа можно наблюдать в клинике и эксперименте на животных ïðè перерезке симпатических адренергических волокон и нервов, обладающих сосудосуживающим действием. Артериальную гиперемию нейропаралитического типа можно получить и химическим путем, блокируя передачу центральных нервных импульсов в области симпатических узлов (с помощью ганглиоблокаторов) или на уровне симпатических нервных окончаний (с помощью симпатолитических или адреноблокирующих средств).
3.Артериальная гиперемия (физиологическая è патологическая), обусловленная местными метаболическими (химическими) факторами,
76
основывается на том, ÷òî ряд метаболитов вызывают расширение сосудов, действуя непосредственно на неисчерченные мышечные элементы их стенки, независимо îò иннервационных влияний. Важная роль в увеличении кровотока при местных сосудистых реакциях отводится изменению рН тканевой среды
— сдвиг реакции среды в сторону ацидоза способствует расширению сосудов. Основные проявления артериальной гиперемии следующие: разлитая краснота, расширение мелких артерий, вен и капилляров, пульсация мелких артерий и капилляров, увеличение числа видимых глазом сосудов, повышение местной температуры, увеличение объема гиперемированного участка, повышение тургора ткани, увеличение давления в артериолах, капиллярах и венах, ускорение кровотока, повышение обмена веществ и усиление функции
органа.
Последствия для организма. Исход артериальной гиперемии может быть различным. В большинстве случаев артериальная гиперемия сопровождается усилением обмена веществ и функции органа, что является приспособительной реакцией. Однако возможны и неблагоприятные последствия. При артеросклерозе, например, резкое расширение сосуда может сопровождаться разрывом его стенки и кровоизлиянием в ткань. Особенно часто подобные явления наблюдаются в головном мозге.
2. Венозная гиперемия
Венозная гиперемия развивается вследствие увеличения кровенаполнения органа или участка ткани в результате затрудненного оттока крови по венам.
Этиология. Этиологическими факторами венозной гиперемии являются: закупорка вен тромбом или эмболом, сдавление вен извне опухолью, рубцом, увеличенной маткой. Тонкостенные вены могут сдавливаться также в участках резкого повышения тканевого гидростатического давления (в очаге воспаления,
âпочках при гидронефрозе).
Âотдельных случаях предрасполагающим моментом венозной гиперемии является конституциональная слабость эластического аппарата вен, недостаточное развитие и пониженный тонус гладкомышечных элементов их стенок. Нередко такое предрасположение носит семейный характер.
Профессии, требующие ежедневного длительного (в течение многих часов) пребывания в вертикальном положении, способствуют венозной гиперемии в дистальных отделах нижних конечностей у лиц с конституционально обусловленной неполноценностью эластических и гладкомышечных элементов стенки венозных сосудов.
Венозная гиперемия развивается также при ослаблении функции правого желудочка сердца, уменьшении присасывающего действия грудной клетки (экссудативный плеврит, гемоторакс), затруднении кровотока в малом круге кровообращения (пневмосклероз, эмфизема легких, ослабление функции левого желудочка).
77
Патогенез. Длительное расширение вен приводит к растяжению их стенки, что может сопровождаться гипертрофией мышечной оболочки и явлениями флебосклероза и варикозного расширения вен.
Продолжительный венозный застой сопровождается значительными изменениями функциональных элементов стенки вены, их атрофией и гибелью. Наряду с этим на участке венозной гиперемии происходит заместительное разрастание соединительной ткани. Классическим примером является цирроз печени при недостаточности функции сердца, вызванный венозным застоем.
Гипоксия при этом первоначально обусловлена ограничением притока артериальной крови, затем действием на тканевые ферментные системы продуктов нарушения обмена, следствием ÷åãî является нарушение утилизации кислорода. Кислородное голодание ïðè венозной гиперемии обусловливает нарушение тканевого обмена, вызывает атрофические и дистрофические изменения è избыточное разрастание соединительной ткани. Биологическая целесообразность избыточного разрастания соединительной ткани заключается в сохранении целостности участка ткани или органа в условиях затрудненной трофики.
Основные проявления и последствия для организма. Клинически венозная гиперемия проявляется увеличением органа или участка ткани, цианозом, местным понижением температуры, отеком, повышением давления в венах и капиллярах застойной области, замедлением кровотока, диапедезом эритроцитов. На завершающем этапе гиперемии возможно маятникообразное движение крови и стаз.
Основным фактором, обусловливающим местные изменения при венозной гиперемии, является кислородное голодание (гипоксия) ткани. Особенно тяжелые последствия возникают при одновременном венозном и лимфатическом застое. Наряду с местными изменениями ïðè венозной гиперемии, особенно åñëè îíà имеет генерализованный характер, возможен и ряд общих гемодинамических нарушений с весьма тяжелыми последствиями. Чаще всего они возникают при закупорке крупных венозных коллекторов — воротной, нижней полой âåíû. Скопление крови в указанных сосудистых резервуарах (äî 90 % всего ОЦК) сопровождается резким снижением артериального давления, нарушением питания жизненно важных органов (сердце, ìîçã). Вследствие недостаточности сердца èëè паралича дыхания возможен смертельный исход.
78
3. Ñòàç
Ñòàç (îò ãðå÷. stasis — стояние) — это замедление и остановка тока крови в капиллярах, мелких артериях и венах. Различают истинный (капиллярный) ñòàç, возникающий вследствие патологических изменений в капиллярах или нарушения реологических свойств крови, ишемический — вследствие полного прекращения притока крови из соответствующих артерий в капиллярную сеть и венозный.
Венозный и ишемический стаз является следствием простого замедления и остановки кровотока. Эти состояния возникают по тем же причинам, что и венозная гиперемия и ишемия. Венозный стаз может быть результатом сдавления вен, закупорки их тромбом или эмболом, à ишемический — следствием спазма, сдавления или закупорки артерий. Устранение причины стаза ведет ê восстановлению нормального кровотока. Напротив, прогрессирование ишемического и венозного стаза способствует развитию истинного.
При истинном стазе столбик крови в мелких венах становится неподвижным, кровь гомогенизируется, эритроциты набухают и теряют значительную часть своего пигмента. Плазма вместе с освободившимся гемоглобином выходит за пределы сосудистой стенки. В тканях очага капиллярного стаза отмечаются признаки резкого нарушения питания, омертвение.
Причиной истинного стаза могут быть физические (холод, тепло), химические (яды, концентрированный раствор натрия хлорида и других солей, скипидар, горчичное и кротоновое масло) и биологические (токсины микроорганизмов) факторы.
Механизм развития истинного стаза объясняется внутрикапиллярной агрегацией эритроцитов, т. е. их склеиванием и образованием конгломератов, затрудняющих кровоток. Ïðè ýòîì повышается периферическое сопротивление.
Агрегация возникает в результате изменения физических свойств плазмолеммы эритроцитов под непосредственным действием факторов, проникающих внутрь капиллярного сосуда. При электронно-микро- скопическом изучении феномена агрегации эритроцитов оказалось, что их поверхность, гладкая â нормальных условиях, становится при усиленной агрегации неровной, «пушистой». При этом изменяются сорбционные свойства эритроцитов ïî отношению к некоторым красителям, что свидетельствует î нарушении их физико-химического состояния.
В патогенезе истинного стаза важное значение придается замедлению кровотока â капиллярах вследствие сгущения крови. Ведущую роль при этом играет повышенная проницаемость стенки капилляров сосудов, расположенных â зоне стаза. Этому способствуют этиологические факторы, вызывающие стаз, и метаболиты, образующиеся в тканях. Особое значение в механизме стаза отводится биологически активным веществам (серотонин,
79
брадикинин, гистамин), а также ацидотическому сдвигу тканевой реакции среды и ее коллоидному состоянию. В результате отмечается повышение проницаемости сосудистой стенки и расширение сосудов, ведущие к сгущению крови, замедлению кровотока, агрегации эритроцитов è, как следствие, — стазу.
Особенно важным является выход в ткани плазменных альбуминов, способствующий понижению отрицательного заряда эритроцитов, что может сопровождаться их агрегацией.
4. Ишемия
Нарушение периферического кровообращения, â основе которого лежит ограничение èëè полное прекращение притока артериальной крови, называется ишемией (îò ãðå÷. ischein - задерживать, останавливать; haima - кровь), или местным малокровием. Ишемия характеризуется следующими признаками: побледнением ишемизированного участка органа, снижением температуры, нарушением чувствительности в виде парестезии (ощущение онемения, покалывания, «ползания мурашек»), болевым синдромом, уменьшением скорости кровотока, уменьшением органа в объеме, понижением артериального давления на участке артерии, расположенном ниже препятствия, понижением напряжения кислорода в ишемизированном участке органа èëè ткани, уменьшением образования межтканевой жидкости и снижением тургора ткани, нарушением функции органа èëè ткани, дистрофическими изменениями.
Причиной ишемии могут быть различные факторы: сдавление артерии, обтурация просвета, действие на нервно-мышечный аппарат артериальной стенки. В соответствии с этим различают компрессионный, обтурационный и ангиоспастический типы ишемии.
1.Компрессионная ишемия возникает от сдавления приводящей артерии лигатурой, рубцом, опухолью, инородным телом и др.
2.Обтурационная ишемия является следствием частичного сужения или полного закрытия просвета артерии тромбом или эмболом. Продуктивноинфильтративные и воспалительные изменения стенки артерии, возникающие при атеросклерозе, облитерирующем эндартериите, узловатом периартериите, также приводят к ограничению местного кровотока ïî òèïó обтурационной ишемии.
Ангиоспастическая ишемия возникает вследствие раздражения сосудосуживающего аппарата артерий è их рефлекторного спазма, вызванного эмоциональным воздействием (страх, боль, гнев), физическими факторами (холод, травма), химическими агентами, биологическими раздражителями (токсины бактерий) и т. д. Â условиях патологии ангиоспазм характеризуется относительной продолжительностью и значительной выраженностью, что может быть причиной резкого замедления кровотока, вплоть до полной его остановки. Чаще всего ангиоспазм развивается в артериях относительно
80
