
lekcii dlya zaochnogo farmfakulteta
.pdfСпециалисты различного профиля продолжают независимо от интересов генетиков изучать человека, что, несомненно, помогает генетику легко распознавать многие формы наследственных отклонений.
- Возможность использовать все методы, применяемые в медицине (биохимические, морфологические, иммунологические, электрофизиологические, клинические и др.), т.е. любые методы, которые дают возможность регистрировать признак и выражать его количественно.
Для решения сугубо генетических задач применительно к человеку в настоящее время используют следующие методы:
1.Генеалогический (генеалогия - греч. genealogia; от genea рождение, происхождение, поколение + logos слово, изложение - установление родственных связей между индивидумами в пределах одного поколения или в ряду поколений, или родословная) - метод родословных, т.е. прослеживание болезни (или признака) в семье или роду с указанием типа родственных связей между членами родословной. В медицинской генетике его часто называют клиникогенеалогическим, так как речь идет об изучении патологических признаков в семье с помощью клинических приемов обследования. Он относится к наиболее универсальным методам в генетике человека. Этот метод используется для установления наследственного характера признака, определения типа наследования и пенетрантности гена, при анализе сцепления генов и картирования хромосом, при изучении интенсивности мутационного процесса, при расшифровке механизмов взаимодействия генов, при медико-генетическом консультировании. Суть этого метода сводится к выяснению родственных связей и к прослеживанию признака или болезни среди близких и дальних, прямых и непрямых родственников. Он включает два этапа: составление родословных и генеалогический анализ.
Составление родословной начинается с пробанда (лицо, первое попавшее
âполе зрения исследователя). Чаще всего это больной или носитель изучаемого признака. Дети одной родительской пары называются сибсами (братья-сестры). Семьей в узком смысле называют родительскую пару и их детей. Обычно родословная собирается по одному или нескольким признакам. Она может быть полной (составление по восходящему, нисходящему и боковым направлениям) и ограниченной. Для наглядности готовят графическое изображение родословной. Грубой ошибкой является искусственное укорочение звеньев родословной в связи с трудностями обследованных родственников II и III степени. Генеалогический анализ позволяет установить генетические закономерности: наследственный характер признака и тип наследования.
2.Близнецовый метод - исследование генетических закономерностей на близнецах. Он был предложен Galton в 1875 г. При использовании этого метода производится сопоставление монозиготных близнецов с дизиготными, партнеров монозиготных пар между собой, данных анализа близнецовой выборки с общей популяцией.
Монозиготными близнецами (однояйцевые, идентичные) называются
61

индивиды, выросшие из одной зиготы, разделившейся на ранних стадиях дробления на 2 части; они обладают поэтому идентичными генотипами. Дизиготные близнецы (двуяйцевые, неидентичные) возникают за счет оплодотворения двух яйцеклеток, развивающихся в течение одной беременности. Они имеют в среднем 50% идентичных генов, но отличаются от обычных сибсов значительно большей общностью факторов среды.
Общая частота двойнями равна приблизительно 1%, из которых 1/4-1/3 приходится на рождение монозиготных близнецов. Близнецовый метод применяется для:
-оценки соотносительной роли наследственности и среды в развитии признака;
-установления наследственного характера признака и определения пенетрантности гена;
-оценки действия некоторых внешних факторов: лекарственных препаратов, методов воспитания, обучения.
Этот метод включает 3 этапа: 1) сопоставление близнецовой выборки, 2) установление зиготности, 3) сопоставление пар и групп близнецов по рассматриваемым признакам.
Диагностика основывается на анализе наиболее изученных моногенных полиморфных признаков (эритро- и лейкоцитарные антигены, группы белков сыворотки крови и т.д.). Дизиготные близнецы в отличие от монозиготных отличаются по этим признакам. Если какой-либо качественный признак встречается у обоих близнецов данной пары - это конкордантная пара, а если только у одного из них - это дискордантная пара близнецов.
3. Популяционно-статистический метод основан на использовании наследственных признаков в больших группах населения из одной или нескольких популяций, в одном или нескольких поколениях. Изучаются выборки из конкретных популяций с применением статистической обработки полученного материала. Этот метод используется для изучения:
• частоты генов в популяции, включая частоту наследственных болезней,
• мутационного процесса,
• роли наследственности и среды в возникновении болезней, особенно болезней с наследственным предрасположением,
• роли наследственности и среды в формировании фенотипического полиморфизма по нормальным признакам,
• значения генетических факторов в антропогенезе.
Возможные ошибки этого метода могут быть связаны с недоучетом миграции населения и с тем, что выбранные группы отличаются по большему число признаков, чем сравниваются.
4. Цитогенетический метод основан на микроскопическом изучении хромосом. Его начали широко использовать в генетике человека только с 20-
õгодов ХХ века для:
-диагностики хромосомных болезней,
-составления карт хромосом,
62
-изучения мутационного процесса,
-решения некоторых эволюционных проблем в генетике человека,
-изучения нормального хромосомного полиморфизма в человеческой популяции.
Именно с этим методом связано открытие всех форм хромосомных болезней. С его помощью изучается частота хромосомных и геномных мутаций
âзародышевых клетках и частота хромосомных аберраций в соматических клетках. Культуры соматических клеток человека являются хорошими объектами для проверки мутагенности факторов среды (физических, химических, биологических). Цитогенетическими методами изучаются механизмы мутагенеза.
Основные сведения о морфологии хромосом человека получены при их изучении в метафазе митоза и профазе-метафазе мейоза. Для прямого хромосомного анализа можно использовать клетки костного мозга и гонад (семенников), полученные путем биопсии, что ограничивает цитогенетические исследования без культивирования. Поэтому основные цитогенетические работы выполнены на культурах клеток человека, особенно на лимфоцитах периферической крови.
Культивирование лейкоцитов периферической крови в течение 2-3 суток
âприсутствии фитогемагглютинина (ФГА) позволяет получить большое число метафаз. Кроме лейкоцитов, можно культивировать клетки эпидермиса, амниотической жидкости. «Сортировка» хромосом (во время метафазы) прямо под микроскопом или чаще всего на микрофотографиях позволяет построить кариотип - т.е. упорядоченно расположить хромосомы по их отличительным признакам.
5.Методы генетики соматических клеток. Поскольку соматические клетки содержат весь объем генетической информации, на них можно изучать генетические закономерности целостного организма. Соматические клетки человека характеризуются 5 основными свойствами, позволяющими их использовать в генетических исследованиях:
- быстрое размножение их на питательных средах, что позволяет получать необходимое их количество для анализа,
- они подвергаются клонированию - можно получать генетически идентичное потомство,
- разные клетки могут сливаться, образуя гибридные клоны, - легко подвергаются селекции на специальных питательных средах, - хорошо и долго сохраняются при глубоком замораживании.
Культуру соматических клеток человека получают для генетических исследований из материала биопсий или аутопсий (кожа, опухоли, периферическая кровь, костный мозг, ткань эмбрионов, клетки из околоплодной жидкости). В настоящее время чаще используются фибробласты и лимфоидные клетки. В генетике человека используют 4 метода из генетики соматических клеток: простое культивирование, клонирование, гибридизация
63
èселекция.
Âнастоящее время обосновано 4 подхода в борьбе с наследственными болезнями:
1. Массовое «просеивание» новорожденных на наследственные дефекты обмена веществ.
2. Пренатальная диагностика.
3. Медико-генетическое консультирование.
4. Контроль за мутагенной опасностью факторов окружающей среды.
1. Массовое «просеивание» новорожденных на наследственные болезни обмена веществ наряду с другими методами является основой профилактики наследственных болезней в популяциях. «Просеивание» (аналог - скрининг) означает предположительное выявление недиагностированной ранее болезни с помощью тестов, обследований или других процедур, дающих быстрый ответ.
Проще говоря, просеивание - это обследование контингентов с целью подразделения их на группы с высокой и низкой вероятностью заболевания. «Просеивают» заболевания, для которых установлена связь между мутантным геном и поврежденной биохимической функцией. Изменения в биохимических параметрах по срокам своего проявления предшествуют возникновению клинических симптомов.
Современные программы массового просеивания предусматривают выявление фенилкетонурии, гипотиреоза, врожденной гипоплазии надпочечников, галактоземию, муковисцидоз, гомоцистинурию, лейциноз,
гистидинемию, аминоацидопатии, недостаточность альфа1-антитрипсина. В практике массового просеивания на наследственные болезни обмена веществ используется кровь (пуповинная, капиллярная, венозная) и сыворотка крови. Например, в программах массового просеивания на фенилуксусную кислоту
èдругие аминоацидопатии используют три метода: микробиологический по Гатри (на его долю приходится 90%), хроматографический и флюорометрический.
2. Пренатальная диагностика осуществляется с помощью разных методов исследования в I и II триместрах. В ней нуждается 10-15% семей, обращающихся в медико-генетическую консультацию. Показания к проведению пренатальной диагностики:
- пожилой возраст родителей, - гетерозиготное носительство хромосомной аномалии,
- предыдущее рождение ребенка с болезнью Дауна, врожденными пороками развития или умственной отсталостью,
- Х-сцепленная патология, - наследственные дефекты метаболизма, - тератогенные воздействия.
Пренатальная диагностика представляет собой комплексное исследование, основанное на использовании лабораторных и инструментальных методов:
1) ультразвуковое исследование (врожденные пороки развития),
64
2)фетоскопия используется для взятия образцов крови, кожи или других органов плода (показания - токсоплазмоз, вирусная краснуха, гемофилия, талассемия, осложнения связанные с самопроизвольным прерыванием беременности,
3)фетоамниография использовалась до появления УЗИ для диагностики врожденных пороков развития костной системы, спинномозговых и пупочных грыж и особенно атрезий желудочно-кишечного тракта. Использование контрастных веществ вызывает осложнения как у беременной, так и у плода,
4)диагностический амниоцентез (в сроки 14-20 недель беременности) - это акушерско-хирургическая процедура, позволяющая получить амниотическую жидкость для последующих лабораторных исследований (в 1- 2% случаев после амниоцентеза наблюдается гибель плода). Амниотические клетки используют для культивирования и цитогенетических исследований, для диагностики лизосомных болезней, альфа-фетопротеина, для диагностики более 60 форм наследственных ферментопатий,
5)диагностическая биопсия хориона (хориоцентез). Оптимальный срок для биопсии - 17-я неделя беременности, а результаты, связанные с культивированием амниотических клеток, могут быть получены спустя 3-5 недель. Используют З основных методики получения биоптата хориона: с помощью щипцов, методом эндоцервикальной аспирации и с помощью браши (по типу лабораторного ершика для пробирок). Этот метод используют для диагностики хромосомных и биохимических (молекулярных) нарушений.
3. Медико-генетическое консультирование включает:
- выявление наследственной формы патологии на основании осмотра больного, составления родословной, цитологических, биохимических, кариологических и других методов диагностики наследственных болезней,
- определение степени риска появления потомства с наследственными дефектами развития у лиц из семей, отягощенных наследственной патологией, вступающих в брак и желающих иметь детей. В обоснованных случаях рекомендуется воздержаться от заключения брака,
- выявления нарушений в геноме, обменных процессов у плода с помощью методов пренатальной диагностики с возможным дальнейшим прерыванием беременности, если риск рождения больного ребенка достаточно высок. Однако, принятие окончательного решения о прерывании или сохранении беременности остается за супругами,
- искусственное осеменение от генетически здорового донора применимо
âтех случаях, когда рождение здорового потомства невозможно из-за доминантного характера наследования патологии.
4. Контроль за мутагенной опасностью факторов окружающей среды
осуществляют генетики, экологи, врачи гигиенического профиля, учитывая естественный фон радиации и его колебания, дрейф мутаций и т.п.
Принципы лечения наследственных заболеваний:
1. Симптоматическое лечение - хирургическое лечение расщелины верхней губы и твердого неба, сросшихся пальцев, корригирующие линзы при
65
близорукости и др.
2.Патогенетическая терапия - воздействие на те механизмы, которые формируют наследственное заболевание:
- заместительная терапия - восполнение недостающего компонента (введение инсулина при сахарном диабете, свертывающих факторов при гемофилии и т.д.) или удаление части железы при гиперфункции;
- когда повышен синтез тех или иных веществ, то уменьшаютих образование путем применения медикаментов, угнетающих их образование;
- диетотерапия - при нарушении расщепления тех или иных веществ (галактозы, фенилаланина) их исключают из диеты;
- медикаментозное лечение направлено на удаление продуктов, избыточно накапливающихся в организме. Например, при поражении печени в ней накапливаются ионы меди, поэтому применяют ионообменные смолы, которые препятствуют всасыванию меди в кишечнике.
3.Генная инженерия - это направление исследований в молекулярной биологии и генетике, конечной целью которого является получение с помощью лабораторных методов организмов с новыми комбинациями наследственных свойств. В основе лежит целенаправленное манипулирование с фрагментами нуклеиновых кислот, т.е. конструируется из различных фрагментов генетического материала нужные фрагменты и вводятся в реципиентный организм.
66

ОТЕК И ВОДЯНКА
Отек – избыточное накопление жидкости в тканях, которое может иметь либо местный, либо генерализованный характер. Генерализованные отеки являются одним из проявлений тех форм патологии, которые сопровождаются задержкой жидкости в организме. Они чаще всего сочетаются с избыточным накоплением жидкости в естественных полостях тела, что называется водянкой. Скопившаяся в полостях или тканях воспалительная жидкость именуется экссудатом, а невоспалительная – транссудатом. Примерами генерализованных отеков могут служить отеки, развивающиеся при голодании, заболеваниях сердца и почек, а местных – воспалительные и аллергические отеки.
Развитие отека создает неблагоприятные условия для жизнедеятельности тканей, нарушая кровообращение в них и механически сдавливая клетки. Избыток интерстициальной жидкости затрудняет газообмен и другие виды обмена веществ между кровью и тканями. Длительное поддержание отека может приводить к разрастанию соединительной ткани. Вызывая нарушение трофики, отечная жидкость легко инфицируется. Опасность отека в значительной мере зависит от его локализации. Так отек гортани, легких, головного мозга приводит к серьезным нарушениям, создающим угрозу жизнедеятельности. Значительно нарушаются функции жизненноважных органов при гидроцефалии, гидроперикарде, гидротораксе. Вместе с тем, воспалительные, аллергические и токсические отеки имеют защитноприспособительные элементы, так как в этих случаях накапливающаяся в тканях жидкость ограничивает распространение токсических веществ и, понижая их концентрацию, уменьшает их повреждающее действие на тканевые элементы.
Таким образом, отек отвечает всем критериям типового патологического процесса и как многие из таковых обладает как повреждающими свойствами, так и элементами защиты. На практике, однако, медикам чаще приходится использовать различные средства и методы противоотечной терапии, основанные на знании механизмов, существенно отличающихся при различных видах отеков.
1. Роль местных сосудисто-тканевых факторов в патогенезе отека
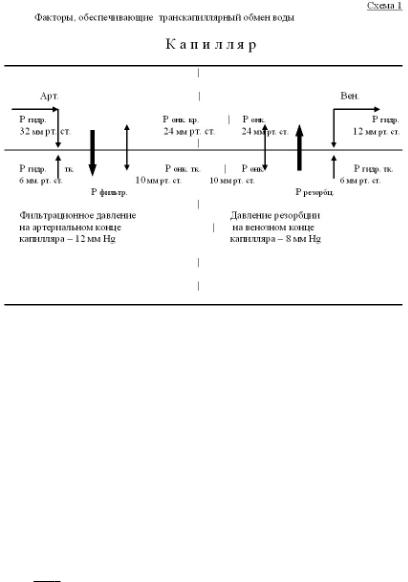
Патогенетической основой как местных, так и генерализованных отеков являются нарушения тех факторов, которые обеспечивают транскапиллярный обмен воды, проанализированных Э. Старлингом (1896). Речь идет о движущих силах транссудации и резорбции. Суть в том, что на уровне капилляров происходит два процесса перемещения жидкости: транссудация (фильтрация) жидкой части крови в интерстициальное пространство и резорбция жидкости из ткани в кровь. В норме эти два процесса должны быть сбалансированы, поскольку содержание жидкости в ткани является величиной относительно постоянной. Отек является результатом нарушения этого баланса с
67

преобладанием транссудации над резорбцией.
Согласно концепции Э. Старлинга, участниками этих процессов являются три фактора:
1.Гидростатическое давление крови и величина тканевого сопротивления;
2.Коллоидно-осмотическое (онкотическое) давление плазмы и тканевой жидкости;
3.Проницаемость сосудистой стенки
Так как через стенки капилляров относительно легко перемещается вода, электролиты, некоторые органические соединения (мочевина), но труднее транспортируются белки, то величина онкотического давления крови (зависящая от содержания белка) значительно выше онкотического давления интерстициальной жидкости (~ 24 мм рт.ст. против 10 мм рт. ст. соответственно). Разность этих давлений (14 мм рт. ст.) называется эффективным онкотическим давлением (ЭОД), представляющее собой силу, которая «тянет» воду в капилляры из интерстициального пространства. Но направление движения жидкости (сосуд - ткань) определяется взаимодействием этой притягивающей силы с величиной гидростатического давления, которое зависит от движения крови в сосудах, в результате чего создаются силы, стремящиеся вывести воду из капилляров в окружающие ткани. Эффект гидростатического давления будет тем больше, чем выше кровяное давление и чем меньше сопротивление со стороны тканей, окружающих капилляры.
В отличие от онкотического, величина гидростатического давления в капиллярах не одинаковая. Она составляет в артериальном конце капилляра ~ 32 мм рт. ст., а в венозном ~ 12 - 14 мм рт. ст. Сопротивление тканей (давление тканевой жидкости) составляет ~ 8 мм рт. ст. Следовательно, величина эффективного гидростатического давления (ЭГД) в артериальной части капилляра выше, чем в венозной и соответственно составляет ~ (32 - 6) = 26 и (12 – 6) = 6 мм рт. ст.*
Из взаимоотношений между данными факторами (схема 1), следует, что преобладание в артериальной части капилляра ЭГД над ЭОД обеспечивает фильтрацию жидкости под давлением ~ 12 мм рт. ст., а преобладание присасывающей силы в венозном конце капилляра обеспечивает обратный процесс, т.е. резорбцию интерстициальной жидкости в сосуды.
Представленные расчеты позволяют также понять, что баланс между транссудацией и резорбцией может быть достигнут только с учетом того, что процесс резорбции тканевой жидкости совершается в двух направлениях: в кровеносные сосуды и в лимфатические сосуды. Установлено, что у здорового человека за сутки из крови в ткани фильтруется до 20 литров жидкости, 17 из
* Здесь были представлены цифровые характеристики давлений по Старлингу; по
современным представлениям величина тканевого давления жидкости отрицательная, т.к. она на 6-7 мм. рт. ст. ниже величины атмосферного давления.
68
которых возвращаются обратно в капилляры и около трех литров выводится из тканей через лимфатические сосуды и далее возвращается в сосудистое русло.
Таким образом, недостаточность оттока лимфы может приводить к развитию отеков, получивших название лимфатических (лимфогенных). Затруднения лимфооттока может носить как местный, так и генерализованный характер. Местное нарушение может быть связано с врожденной гипоплазией лимфатических сосудов, их сдавлением рубцовой тканью, опухолями и метастазами. Затруднение лимфооттока (абсолютная или механическая лимфатическая недостаточность) возникает также при закупорке сосудов паразитами или тромбами, а также в случае спазма лимфососудов. Длительный лимфатический отек ведет к накоплению в ткани белка с последующим разрастанием коллагеновых волокон и деформацией органа (например, «синдром слоновости»). Кроме абсолютной, может иметь место и относительная (динамическая) лимфатическая недостаточность. Она возникает при перегрузке лимфооттока и участвует в патогенезе некоторых генерализованных форм отеков.
Îíêîтические отеки. Эти отеки возникают от снижения концентрации белков в плазме (гипопротеинемии). Гипоонкия крови развивается в связи с:
а) недостаточностью поступления белка в организм (алиментарное голодание, заболевания желудочно-кишечного тракта);
69

б) нарушением синтеза белков при заболеваниях печени; в) потерями белков плазмы через повреждения кожного покрова при
ожогах или в связи с почечными потерями, максимально выраженными при нефротическом синдроме.
Гипоонкия плазмы может быть связана с диспротеинемией, когда резко снижается альбумин-глобулиновый коэффициент (в норме 2:1). В этом случае дефицит альбуминов может возмещаться избытком глобулина так, что уровень общего белка плазмы сохраняется в пределах нормы. Следовательно, величина онкотического давления в значительной степени зависит от содержания мелкодисперсных белков – альбуминов. Поэтому замещение дефицита альбуминов другими белками не предотвращает гипоонкии крови.
Спозиции концепции Э. Старлинга, снижение ЭОД одновременно изменяет оба процесса транскапиллярного обмена: усиливается транссудация в артериальном конце капилляра при параллельном снижении и даже прекращении резорбции в венозном отделе капилляров. Усиление лимфооттока в этих условиях может оказаться недостаточным для поддержания баланса между транссудацией и резорбцией. Далее, в связи с прогрессированием отека и компрессией тканевых элементов и лимфососудов, динамическая лимфатическая недостаточность может трансформироваться в абсолютную, что резко усиливает отечность тканей. В патогенезе онкотических (гипоальбуминемических) отеков участвуют также и гормональные механизмы, регулирующие водно-электролитный обмен на уровне целостного организма (см. патогенез почечных и сердечных отеков).
Мембраногенные отеки – это отеки, в патогенезе которых главную роль играет повышение проницаемости сосудистой стенки для белка, что чаще связано с действием яда змей, насекомых, некоторых бактериальных токсинов, боевых отравляющих веществ. Таким же эффектом обладают и биологически активные вещества (известные как медиаторы воспаления и аллергии – гистамин, серотонин, брадикинин и др.).
Повышение проницаемости сосудов для белка отмечается при тяжелой гипоксии (общей и местной), которая ассоциируется с накоплением кислореагирующих продуктов и ацидозом.
Усиленный выход белков не всегда компенсируется их адекватным оттоком через лимфатические сосуды, поэтому онкотическое давление интерстициальной жидкости увеличивается, что закономерно снижает величину ЭОД. Если речь идет о генерализованном увеличении сосудистой проницаемости (например, при системном действии медиаторов), то это может приводить и к снижению онкотического давления плазмы, что еще в большей степени снижает ЭОД. Поэтому мембраногенные отеки иногда называют вторично онкотическими.
Таким образом, множество причин, повышающих проницаемость сосудистой стенки, предопределяет участие мембраногенного фактора в развитии разных отеков, но ведущим фактором он является для воспалительных, аллергических и токсических отеков.
70
