
- •1.Исторический обзор развития термодинамики и статистической физики.
- •2.Простые модельные системы. Конфигурации. Макросостояние и микросостояние системы. Однородное и неоднородное состояние системы
- •3.Распределение вероятностей для случайной физической величины. Теоремы сложения и умножения вероятностей.
- •4. Понятие вероятности. Статистическая независимость и квадратичная флуктуация
- •5.Равновесное и неравновесное состояния системы. Флуктуации. Необратимость. Энтропия.
- •6.Классическое описание движения механических систем. Канонические уравнения движения гамильтона
- •7.Фазовое пространство. Точка фазового пространства. Объем фазового пространства. Фазовая траектория. Статистический ансамбль.
- •8.Теорема лиувилля. Функция статистического распределения
- •11. Распределение Максвелла
- •12. Распределение Максвелла-Больцмана
- •13.Микроканонический ансамбль.
- •17. Уравнение состояния идеального газа
- •18. Одноатомный идеальный газ.
- •19. Двухатомный идеальный газ. Вращательная и колебательная степени свободы.
- •20.Классическая теория теплоемкости многоатомного идеального газа.
- •23.25. Квантово-механическое описание систем. У.Ш. Рассчет числа возможных состояний ид.Газа.
- •29.21 Теплоемкость твердых тел. Теория эйнштейна.
- •30. Теплоемкость твердых тел. Теория Дебая.
- •31. Теория флуктуаций
- •32.Термодинамическая система. Равновесные состояния и равновесные процессы. Температура. Нулевое начало.
- •33.Изопроцессы. Работа.
- •35. Теплоемкость газа.
- •36. Круговые процессы. Цикл Карно.
- •38. Процесс джоуля-томсона
- •40. Второе начало термодинамики.
- •41.Энтропия. З-н возраст.Э-пии
- •42. Неравенство клаузиуса. Общие условия термодин-го равновесия и устойчивости однородной системы.
- •43. Третье начало термод. И его следствия
- •44.Системы с переменным количеством вещества. Химический потенциал.
- •45.Равновесие фаз. Фазовые переходы первого рода
- •47. Броуновское движение. Уравнение фоккера-планка
- •48. Фазовые переходы второго рода. Теория ландау
- •51.Явления переноса. Уравнение фурье. Нестационарное уравнение теплопроводности.
- •52. Каноническое распределение и термодин. Функции.
4. Понятие вероятности. Статистическая независимость и квадратичная флуктуация
Пусть
в течение длительного времени изменения
состояния системы Т
измеряется значение величины L.
Как уже отмечали из-за различных
процессов, происходящих в системе, при
неизменных внешних условиях ее состояние
изменяется непрерывным образом. То
есть, величины, характеризующие состояние
системы, пробегают непрерывный ряд
значений. Поэтому в каждом состоянии,
в котором величина
L
имеет какое-то точной значение, система
будет проводить бесконечно малое время
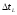 .
Поэтому необходимо говорить не о точном
значении величиныL,
а некотором интервале ее значений, то
есть о вероятности того, что величина
L
имеет значение, лежащее в интервале
между L
и
L+dL.
Эту вероятность обозначают
.
Поэтому необходимо говорить не о точном
значении величиныL,
а некотором интервале ее значений, то
есть о вероятности того, что величина
L
имеет значение, лежащее в интервале
между L
и
L+dL.
Эту вероятность обозначают
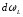 .
По определению
.
По определению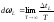 где
где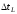 -
время, в течение которого система
находится в состояниях соответствующих
значениямL,
лежащим между L
и L
+
dL.
Очевидно, что время
-
время, в течение которого система
находится в состояниях соответствующих
значениямL,
лежащим между L
и L
+
dL.
Очевидно, что время
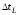 ,
а следовательно, и вероятность
,
а следовательно, и вероятность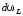 ,
будут при прочих равных условиях
пропорциональны величине интервалаdL.
Поэтому удобно представить
,
будут при прочих равных условиях
пропорциональны величине интервалаdL.
Поэтому удобно представить
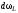 в виде
в виде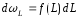 гдеf
(L)-
вероятность того, что значение L
лежит в некотором “единичном” интервале.
гдеf
(L)-
вероятность того, что значение L
лежит в некотором “единичном” интервале.
f
(L)
называется плотностью
вероятности
или функцией
распределения.
Если обозначить через
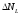 число измерений, для которых физическая
величинаL
попала в интервал между L
и
L+dL,
а через N
- полное число измерений за время T,
то можно кроме временного определения
вероятности дать и такое, эквивалентное
ему
число измерений, для которых физическая
величинаL
попала в интервал между L
и
L+dL,
а через N
- полное число измерений за время T,
то можно кроме временного определения
вероятности дать и такое, эквивалентное
ему
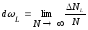 Статистич.
независимость
означает, что состояние, в котором
находится одна из подсистем, никак не
влияет на вероятности различных состояний
других подсистем.
p12
=
p1
p2,
где p12
– стат. распределение составной
подсистемы, а p1
и p2
– отдельных подсистем.
Статистич.
независимость
означает, что состояние, в котором
находится одна из подсистем, никак не
влияет на вероятности различных состояний
других подсистем.
p12
=
p1
p2,
где p12
– стат. распределение составной
подсистемы, а p1
и p2
– отдельных подсистем.
Флуктуации – случ. отклонения динамич. переменных от средних значений. (f)2 = f 2 – f 2 т.е. сред. квадратич. флуктуация определяется разностью между сред. квадратом величины и квадратом ее сред. значения.
5.Равновесное и неравновесное состояния системы. Флуктуации. Необратимость. Энтропия.
Состояние макросистемы характеризуют величинами, которые называют термодинамическими параметрами (р, V, Т и др.). Если эти параметры имеют опред-ые и постоянные значения для любой части макросистемы, то ее состояние называют равновесным. Будучи выведена из состояния равновесия, система в дальнейшем возвращается в равновесное состояние. Это происходит за время, равное по порядку величины времени релаксации (τ). Для каждого параметра состояния время τ имеет свое значение. Таким образом, состояние системы является равновесным, если все параметры ее имеют определенные и постоянные значения при неизменных внешних условиях. Равновесное состояние можно представить точкой в пространстве, по координатным осям которого откладываются значения параметров состояния. Если независимыми являются всего две переменные (например, р и V), то равновесное состояние изображают точкой на диаграмме р, V.
По существу все процессы в макросистемах являются необратимыми. Необратимым называется процесс, который нельзя провести в противоположном направлении через все те же самые промежуточные состояния. Все реальные процессы необратимы.Примеры необратимых процессов: диффузия, термодиффузия, теплопроводность, вязкое течение и др.Возникает вопрос в чем причина необратимости! Это выглядит особенно странно, если учесть, что все законы механики обратимы во времени.Решение этой сложной проблемы пришло с открытием новой термодинамической величины - энтропии - и раскрытием ее физического смысла.Второе начало вводит новую функцию состояния - энтропию S, изменение которой для обратимых равновесных процессов равно приведенному теплу dS=δQ/T Если тепловой обмен между системой и термостатом исключен (δQ=0), то dS=0. В изолированных системах это условие является критерием равновесия. В статистической физике, в отличие от термодинамики, основным является предположение о структуре вещества: оно состоит из атомов, молекул,которые участвуют в хаотическом движении и взаимодействуют между собой. Главная принципиальная черта как самого теплового движения, так и его макроскопических (для всего вещества, тела) проявлений – это флуктуационный характер. Под этим понимаем абсолютную случайность движений, невозможность предсказания состояния молекул в будущем по известному состоянию молекул в данный момент времени. Для макроскопических проявлений степень случайности уменьшается, но полностью не исчезает никогда. В любом веществе (системе) постоянно происходят отклонения характеризующих его величин от их средних значений которые называют флуктуациями. Флуктуации – случ. отклонения динамич. переменных от средних значений. (f)2 = f 2 – f 2 т.е. сред. квадратич. флуктуация определяется разностью между сред. квадратом величины и квадратом ее сред. значения.
