
- •►ПОВРЕЖДЕНИЕ И ГИБЕЛЬ КЛЕТОК И ТКАНЕЙ◄
- •ДИСТРОФИИ
- •ПАРЕНХИМАТОЗНЫЕ (ВНУТРИКЛЕТОЧНЫЕ) ДИСТРОФИИ
- •ПАРЕНХИМАТОЗНЫЕ БЕЛКОВЫЕ ДИСТРОФИИ (ДИСПРОТЕИНОЗЫ)
- •ПАРЕНХИМАТОЗНЫЕ ЖИРОВЫЕ ДИСТРОФИИ
- •ПАРЕНХИМАТОЗНЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ
- •СТРОМАЛЬНО-СОСУДИСТЫЕ (МЕЗЕНХИМАЛЬНЫЕ, ВНЕКЛЕТОЧНЫЕ) ДИСТРОФИИ
- •СТРОМАЛЬНО-СОСУДИСТЫЕ БЕЛКОВЫЕ ДИСТРОФИИ
- •СТРОМАЛЬНО-СОСУДИСТЫЕ ЖИРОВЫЕ ДИСТРОФИИ
- •СТРОМАЛЬНО-СОСУДИСТЫЕ УГЛЕВОДНЫЕ ДИСТРОФИИ
- •СМЕШАННЫЕ ДИСТРОФИИ
- •НАРУШЕНИЕ ОБМЕНА ХРОМОПРОТЕИДОВ (ЭНДОГЕННЫХ ПИГМЕНТОВ)
- •НАРУШЕНИЕ ОБМЕНА НУКЛЕОПРОТЕИДОВ
- •НАРУШЕНИЯ ОБМЕНА МИНЕРАЛОВ
- •КЛЕТОЧНАЯ ГИБЕЛЬ. СМЕРТЬ
- •НЕКРОЗ
- •АПОПТОЗ
- •СМЕРТЬ, ПРИЗНАКИ СМЕРТИ
- •НАРУШЕНИЯ КРОВООБРАЩЕНИЯ
- •НАРУШЕНИЯ КРОВЕНАПОЛНЕНИЯ
- •АРТЕРИАЛЬНАЯ ГИПЕРЕМИЯ
- •ВЕНОЗНАЯ ГИПЕРЕМИЯ
- •ИШЕМИЯ
- •НАРУШЕНИЯ ПРОНИЦАЕМОСТИ СОСУДИСТОЙ СТЕНКИ
- •КРОВОТЕЧЕНИЕ
- •ПЛАЗМОРРАГИЯ
- •НАРУШЕНИЯ ТЕЧЕНИЯ И СОСТОЯНИЯ КРОВИ
- •СТАЗ, СЛАДЖ-ФЕНОМЕН
- •ТРОМБОЗ
- •СИНДРОМ ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ
- •ЭМБОЛИЯ
- •ЭТИОЛОГИЯ. МОРФОГЕНЕЗ
- •ВОСПАЛЕНИЕ
- •ЭКССУДАТИВНОЕ ВОСПАЛЕНИЕ
- •ПРОЛИФЕРАТИВНОЕ (ПРОДУКТИВНОЕ) ВОСПАЛЕНИЕ
- •ИММУНОПАТОЛОГИЯ
- •КОМПЕНСАТОРНО-ПРИСПОСОБИТЕЛЬНЫЕ ПРОЦЕССЫ
- •АТРОФИЯ
- •ГИПЕРТРОФИЯ
- •ГИПЕРПЛАЗИЯ
- •РЕГЕНЕРАЦИЯ
- •ОРГАНИЗАЦИЯ
- •МЕТАПЛАЗИЯ
- •ДИСПЛАЗИЯ
- •I. ЭПИТЕЛИАЛЬНЫЕ ОПУХОЛИ
- •II. МЕЗЕНХИМАЛЬНЫЕ ОПУХОЛИ
- •III. ОПУХОЛИ МЕЛАНИНОБРАЗУЮЩЕЙ ТКАНИ
- •IV. ОПУХОЛИ НЕРВНОЙ СИСТЕМЫ И ОБОЛОЧЕК МОЗГА
- •V. ОПУХОЛИ КРОВИ
- •VI. ТЕРАТОМЫ
- •ОПУХОЛИ ДЕТСКОГО ВОЗРАСТА
- •ГЕМОБЛАСТОЗЫ
- •ЛЕЙКОЗЫ
- •ЛИМФОМЫ
- •АНЕМИИ
- •СОДЕРЖАНИЕ
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Медицинская академия имени С.И. Георгиевского
Федеральное государственное автономное образовательное учреждение высшего образования
"Крымский федеральный университет им. В.И. Вернадского"
КРАТКИЙ КУРС ПАТОМОРФОЛОГИИ
ЧАСТЬ I: ОБЩАЯ ПАТОЛОГИЯ. УЧЕНИЕ ОБ ОПУХОЛЯХ
учебно-методическое пособие для студентов высших учебных медицинских учреждений
Симферополь, 2017
УДК 616–091 (072) ББК 52.5
Авторы: Кривенцов М.А., Филоненко Т.Г., Шаланин В.В., Давыдова А.А., Голубинская Е.П., Ермола Ю.А.
Рецензенты:
Заведующий кафедрой общей и клинической патофизиологии Медицинской академии им. С.И. Георгиевского (структурное подразделение) ФГАОУ ВО "Крымский федеральный университет им. В.И. Вернадского", профессор, доктор медицинских наук, Кубышкин Анатолий Владимирович;
Профессор кафедры гистологии и эмбриологии Медицинской академии им. С.И. Георгиевского (структурное подразделение) ФГАОУ ВО "Крымский федеральный университет им. В.И. Вернадского", профессор, доктор медицинских наук, Троценко Борис Викторович.
Краткий курс патоморфологии. Часть I: общая патология. Учение об опухолях. Учебно-методическое пособие для студентов высших учебных медицинских учреждений / Кривенцов М.А., Филоненко Т.Г., Шаланин В.В., Давыдова А.А., Голубинская Е.П., Ермола Ю.А. – Симферополь, 2016. – 250 стр.
Учебно-методическое пособие по патологической анатомии подготовлено на кафедре патологической анатомии с секционным курсом Медицинской академии имени С. И. Георгиевского (структурное подразделение) ФГАОУ ВО "Крымский федеральный университет им. В.И. Вернадского". В учебно-методическом пособии изложены основные сведения по вопросам общей патологии и учения об опухолях в соответствии с ныне действующей рабочей программой по дисциплине "Патологическая анатомия", согласно образовательному стандарту ФГОС3+.
Преимуществом данного учебно-методического пособия для студентов является лаконичность и структурированность излагаемого материала с большим количеством поясняющих рисунков, таблиц и диаграмм. Представленный материал является достаточным для полного усвоения знаний по дисциплине "Патологическая анатомия" в рамках ее преподавания для студентов высших медицинских учебных заведений III–IV уровня аккредитации.
Кривенцов М.А., Филоненко Т.Г., Шаланин В.В., Давыдова А.А., Голубинская Е.П., Ермола Ю.А.

ПОСВЯЩАЕТСЯ УЧИТЕЛЮ
ДОКТОРУ МЕДИЦИНСКИХ НАУК ПРОФЕССОРУ
ЗАГОРУЛЬКО АЛЕКСАНДРУ КИМОВИЧУ

4
РАЗДЕЛ I
►ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ: ОПРЕДЕЛЕНИЕ, ИСТОРИЯ РАЗВИТИЯ, ЗАДАЧИ, МАТЕРИАЛ И МЕТОДЫ
ИССЛЕДОВАНИЯ, ЗНАЧЕНИЕ ДЛЯ МЕДИЦИНСКОЙ НАУКИ И ПРАКТИКИ◄
ОПРЕДЕЛЕНИЯ
Патология (от греч.: παθος – страдание, боль, болезнь и
λογος – изучение) – наука, изучающая закономерности возникновения, течения и исхода заболеваний и отдельных патологических процессов в организме.
Другие названия: патологическая анатомия, патоморфология, морбидная анатомия, анатомическая патология, гистопатология, хирургическая патология и др.
Патологическая анатомия – научно-прикладная дисциплина, изучающая патологические процессы и болезни с помощью научного, главным образом микроскопического, исследования изменений, возникающих в клетках и тканях, органах и системах органов организма.
При этом под патологическим процессом понимают любое нарушение структуры и функции, а болезнь – это сочетание одного или нескольких патологических процессов, приводящих к нарушению нормального состояния и жизнедеятельности организма.
КРАТКИЕ СВЕДЕНИЯ ОБ ИСТОРИИ РАЗВИТИЯ
История научной патологической анатомии включает три этапа:
1.Макроморфологический этап (XVI–XVIII века) – основные представители: Теофил Боне, Джованни Батиста Морганьи, Жозеф Льето и др.;
2.Микроскопический этап (XIX век – первая половина XX века) – основные представители: Ксавье Биша, Карл фон Рокитански, Рудольф Вирхов и др.;
3.Молекулярно-биологический этап (с середины XX века).
Основой периодизации являются используемые для диагностики
ведущие методы морфологического исследования патологических процессов – аутопсия, микроскопическое исследование и молекулярная диагностика. При этом патологическая анатомия активно использовала достижения смежных дисциплин: анатомии, гистологии и биохимии (молекулярной биологии).
5
Возможность изучения патологических изменений органов человеческого тела появилась в ХV-XVII веках благодаря возникновению и развитию научной анатомии и связана с работами А. Везалия, Г. Фаллопия, Р. Коломбо и Б. Евстахия. В 1676 г. Т. Боне сделал первую попытку на значительном материале (3000 вскрытий) показать существование связи между клиническими проявлениями и обнаруженными морфологическими изменениями. В 1761 г. вышел в свет труд Дж. Б. Морганьи «О местоположении и причинах болезней, выявленных анатомом», что и определило выделение патологической анатомии в самостоятельную науку.
Переломным моментом в развитии этой дисциплины явилось создание в 1855 г. Р. Вирховым теории клеточной патологии. В качестве материального субстрата болезни были впервые признаны клетки тканей. Всё последовавшее развитие методических приёмов исследования и патологии в целом углубляло и расширяло представления о болезнях, начинающихся на клеточном или субклеточном, в том числе молекулярном уровне.
ВРоссии первые попытки организации прозекторского дела относятся к XVIII веку и связаны они главным образом с деятельностью И. Фишера и П.З. Кондоиди. В 1849 г на медицинском факультете Московского университета была открыта первая в России кафедра патологической анатомии, которую возглавил профессор Полунин А.И., прошедший подготовку в Германии. В дальнейшем кафедрой заведовали И.Ф. Клейн, М.Н. Никифоров, В.И. Кедровский, А.И. Абрикосов, А.И. Струков, В.В. Серов. Видными представителями школы патологоанатомов в Петербурге были М.М. Руднев, Г.В. Шор, Н.Н. Аничков, Ф.Ф. Сысоев, В.Г. Гаршин, В.Д. Цинзерлинг, О.К. Хмельницкий.
В1841 г. в связи с созданием нового медицинского факультета в Киеве Н.И.Пирогов поставил вопрос о необходимости открытия кафедры для преподавания патологии в Университете Св. Владимира. В 1845 г. кафедру патологической анатомии и патологической физиологии возглавил ученик Н.И.Пирогова – Н.И.Козлов.
ВКрыму преподавание патологической анатомии началось в 1921 году на медицинском факультете Таврического университета, открытого в мае-октябре 1918 г., в разгар гражданской войны. Руководил кафедрой в 1921–1924 гг. выдающийся отечественный патолог Владимир Германович Штефко – ученик и последователь проф. А.И. Абрикосова. В дальнейшем кафедру возглавляли видные деятели Браул Я.Е., Есипова И.К., Виноградов С.А. Профессор Есипова И.К. занималась вопросами легочной патологии, которые в последующем стали основным направлением научной деятельности большинства сотрудников кафедры.
6
С1967 по 1988 год кафедру патологической анатомии возглавлял профессор Биркун Алексей Алексеевич. Научные интересы проф. А. А. Биркуна и его учеников были сконцентрированы главным образом на патологии легких и патологии детского возраста. Наиболее значительные работы посвящены изучению регенерации и компенсаторной гипертрофии легких, патоморфологии туберкулеза легких, сурфактантной системы легких при различных заболеваниях у детей и взрослых, развития легких и их морфофункциональной незрелости. Впервые подробно изучены патологическая анатомия и патогенез разных форм и неспецифических процессов в легких, которые сопровождают и осложняют течение туберкулеза. Данная проблема приобрела особую актуальность в связи с патоморфозом туберкулеза и тенденцией к учащению неспецифических изменений в легких при нем.
С1988 по 1993 год кафедру возглавлял профессор Нестеров Евгений Никанорович, который продолжил разработку проблемы легочной патологии и изучения поверхностно-активного вещества легких (сурфактанта). Проф. Е.Н. Нестеров опубликовал в 1967 году первый в отечественной литературе научный обзор по этой теме, вызвавший большой интерес патологов, патофизиологов, педиатров и пульмонологов. Начиная с 70-х годов ХХ века, проблема легочного сурфактанта стала основной в научной тематике кафедры патологической анатомии.
С1993 по 2011 год кафедру патологической анатомии возглавлял выдающийся ученый, профессор Загорулько Александр Кимович. Основными направлениями научной деятельности проф. Загорулько А.К. явились ультраструктурная морфология легких в норме и патологии, а также изучение сурфактантной системы легких при различных заболеваниях. К наиболее весомым результатам работы следует отнести создание в Крымском медицинском университете лаборатории электронной микроскопии, опубликованную монографию «Сурфактантная система легких и заместительная сурфактантная терапия», а также создание первого препарата естественного экзогенного сурфактанта «Сукрим», который был официально зарегистрирован в качестве нового лечебного средства в апреле 2000 года.
ЗАДАЧИ ПАТОЛОГИЧЕСКОЙ АНАТОМИИ
Выделяют следующие задачи патологической анатомии:
1.Выявление этиологии (причины) патологических процессов и условий их развития.
7
2.Изучение патогенеза – механизма развития патологических процессов:
морфогенез – последовательность и механизмы развивающихся морфологических изменений;
саногенез – механизмы выздоровления (реконвалесценции);
танатогенез – механизмы умирания (смерти).
3.Характеристика морфологической картины болезни (макро- и микроморфологических признаков).
4.Изучение осложнений и исходов заболеваний.
5.Исследование патоморфоза заболеваний. Патоморфоз – стойкое и закономерное изменение картины болезни под влиянием условий жизни (естественный патоморфоз) или лечения (индуцированный патоморфоз).
6.Изучение ятрогений – патологических процессов, развившихся в результате проведения диагностических или лечебных процедур.
7.Разработка вопросов теории диагноза.
8.Прижизненная и посмертная диагностика патологических процессов при помощи морфологических методов (задача патологоанатомической практики).
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
МАТЕРИАЛ ИССЛЕДОВАНИЯ
Объекты, изучаемые патоморфологом, можно разделить на три группы:
трупный материал;
субстраты, полученные от больных при их жизни (органы, ткани и их части, клетки и их части, продукты секреции, жидкости);
экспериментальный материал.
I)Трупный материал. Традиционно органы и ткани трупов умерших являются предметом изучения в ходе патологоанатомических вскрытий (аутопсий, секций) лиц, умерших от болезней. Случаи смерти, произошедшей не от болезней, а в результате преступлений, катастроф, несчастных случаев или неясных причин, исследуют судебные медики. Трупный материал исследуют на анатомическом и гистологическом уровнях. Реже используются рентгенологические, микробиологические, биохимические и другие методы.

8
Аутопсия – посмертное вскрытие и исследование тела умершего, в том числе и внутренних органов, для установления причины смерти.
Цели и задачи аутопсии:
установление окончательного диагноза и причин смерти больного;
оценка правильности или ошибочности клинического диагноза, эффективности лечения (по критериям расхождений клинического и патологоанатомического диагнозов, а также классификации причин расхождений);
взаимное обогащение научно практического опыта клиницистов и патоморфологов.
Значение секционной работы патоморфолога состоит не только в контроле над качеством лечебно-диагностической деятельности клиницистов, но и в накоплении статистических и научно-практических данных о болезнях и патологических процессах.
II) Материал, взятый при жизни больного. Гораздо больший объём в работе патоморфолога занимает микроскопическое изучение материала, полученного с диагностической целью при жизни больного (биопсия). Чаще всего такой материал поступает от оперирующих клиницистов: хирургов, гинекологов, урологов, оториноларингологов, офтальмологов и др. Диагностическая роль патоморфолога здесь велика и его заключение нередко определяет как формулировку клинического диагноза, так и тактику дальнейшего лечения пациента.
Биопсия (от греч.: βίος – жизнь и ὄψις – внешний вид) – метод исследования, при котором проводится прижизненный забор клеток или тканей (биоптата) из организма с диагностической, прогностической или исследовательской целью.
Виды биопсии
1.По способу получения материала:
Забор материала для гистологического исследования:
эксцизионная биопсия – забор для исследования патологического образования целиком;
инцизионная биопсия – забор для исследования части патологического образования путем его иссечения;
пункционная биопсия – забор для исследования
материала путем прокола (трепан-биопсия – с помощью полой трубки с заостренным краем – трепана;
9
сердцевинная (core-биопсия) – забор столбика материала из мягких тканей при помощи специального трепана);
скарификационная (поверхностная) биопсия – забор материала путём срезания с поверхности образования тонкого пласта ткани;
соскоб (кюретаж) – взятие материала с помощью специального инструмента из полостных органов (матка, цервикальный канал).
Забор материала для цитологического исследования:
отпечаток с патологического образования (эрозии, язвы)
– материал переносится на предметное стекло путем его прикладывания к изъязвленной поверхности;
мазок-отпечаток – материал соскребается с патологического образования шпателем и переносится на предметное стекло;
тонкоигольная аспирационная биопсия – забор материала с помощью пункционной иглы и шприца;
2.По контролю точности:
классическая биопсия;
прицельная биопсия: эндоскопическая, под контролем УЗИ, под рентгенологическим контролем, стереотаксическая биопсия.
3.По срочности:
плановая – результат через несколько дней);
срочная (цито-биопсия, интраоперационная биопсия) – результат не позднее 30 минут для быстрого установления гистологического диагноза с целью определения дальнейшей тактики хирурга.
III) Экспериментальный материал. Исследуя ткани, взятые при жизни или после смерти больного человека, патологоанатом наблюдает изменения в момент изъятия ткани. Что было до этого и могло быть после – остаётся неизвестным. Исследование экспериментальной патологии с достаточным количеством лабораторных животных позволяет моделировать и изучать болезни и патологические процессы на любом этапе их развития.
МЕТОДЫ ИССЛЕДОВАНИЯ
Для изучения основ патологического процесса выделяют несколько уровней структурной организации:
организменный;
системный;
10
органный;
тканевой;
клеточный;
субклеточный;
молекулярный.
На каждом из уровней структурной организации в арсенале патоморфологии имеется ряд методов исследования, среди которых:
I) Метод макроморфологического исследования
Оценивают:
локализацию патологического процесса в органе (при поражении не всего органа, а его части) или системе органов;
величину органа, его фрагмента и его патологически измененного участка (линейные размеры, объем, масса);
конфигурацию (очертания, форму) патологически измененного органа или его части;
цветовую характеристику ткани с поверхности и на разрезе;
консистенцию патологически измененной ткани;
степень однородности патологически измененной ткани по цвету
иконсистенции.
II) Метод гистологического исследования
Срезы для обычного светооптического исследования готовят при помощи специальных приборов (микротомов) и окрашивают различными методами. Оптимальная толщина таких срезов до 5 мкм. Гистологический препарат представляет собой окрашенный тканевый срез, заключенный между предметным и покровным стеклом в прозрачные среды (бальзам, полистирол и т.п.).
Методы гистологической окраски, наиболее часто применяющиеся в патоморфологии:
обзорная окраска гематоксилином и эозином: ядра клеток, отложения солей извести, бактерии и др. окрашиваются в синий цвет (базофильные структуры) гематоксилином; цитоплазма клеток, волокна, эритроциты, белковые массы, большинство видов слизи окрашиваются в красный цвет (эозинофильные структуры) эозином.
дифференциальные (специальные) методы окраски, в том числе гистохимические (см. табл. 1, табл. 2):
11
Таблица 1. Некоторые дифференциальные (специальные) методы гистологической окраски
Наименование |
Красители |
|
Результат |
|
|||||
окраски |
|
|
|
|
|
|
|
|
|
Окраска по ван Гизон |
Пикриновая |
|
кислота, |
Коллагеновые |
|
|
|||
|
|
кислый фуксин |
волокна |
– |
ярко- |
||||
|
|
|
|
|
красный |
цвет; |
другие |
||
|
|
|
|
|
элементы |
– |
желтый |
||
|
|
|
|
|
цвет |
|
|
|
|
Окраска по Маллори |
Кислый |
|
фуксин, |
Коллагеновые |
|
|
|||
|
|
анилиновый |
|
синий, |
волокна – темно-синий |
||||
|
|
оранжевый G |
|
цвет; |
другие элементы |
||||
|
|
|
|
|
– |
оранжевый |
или |
||
|
|
|
|
|
красный цвет |
|
|
||
Импрегнация |
|
Аммиачный |
|
раствор |
Ретикулярные |
|
|
||
серебром |
|
серебра |
|
|
волокна, |
элементы |
|||
|
|
|
|
|
нервной |
ткани |
– |
||
|
|
|
|
|
черный |
цвет; |
другие |
||
|
|
|
|
|
элементы |
– |
желто- |
||
|
|
|
|
|
коричневый цвет |
|
|||
Окраска орсеином |
Орсеин |
|
|
Эластические волокна |
|||||
|
|
|
|
|
– темно-красный цвет; |
||||
|
|
|
|
|
другие |
элементы |
– |
||
|
|
|
|
|
светло-розовый цвет |
|
|||
Окраска по Шморлю |
Алюмокалиевые |
Стенки |
костных |
||||||
|
|
квасцы, тионин |
полостей и канальцев |
||||||
|
|
|
|
|
– красно-бурый цвет |
|
|||
Окраска |
по |
Альциановый |
синий, |
Кератин |
– |
красно- |
|||
Крейбергу |
|
сафранин, эритрозин |
оранжевый цвет; слизь |
||||||
|
|
|
|
|
– сине-зеленый цвет |
|
|||
Окраска |
по |
Азур II, эозин |
|
Эритроциты |
|
– |
|||
Романовскому |
|
|
|
|
красный |
|
цвет; |
||
|
|
|
|
|
лейкоциты – голубой |
||||
|
|
|
|
|
или синий цвет |
|
|
||
Окраска по |
Цилю- |
Соляная |
|
кислота, |
Кислотоустойчивые |
|
|||
Нильсону |
|
фуксин |
основной, |
бактерии |
|
|
|
||
|
|
метиленовый синий |
(микобактерии |
|
|
||||
|
|
|
|
|
туберкулеза, лепры) – |
||||
|
|
|
|
|
ярко-красный цвет |
|
|||
12
Таблица 2. Некоторые методы гистохимической окраски
Выявляемые |
Методы окраски |
|
|
|
Результат |
|
|
|
||
соединения |
|
|
|
|
|
|
|
|
|
|
|
Судан III |
|
Нейтральные жиры – |
|||||||
|
|
красно-оранжевый цвет |
||||||||
|
|
|
||||||||
|
Судан черный В, |
|
Нейтральные жиры – |
|||||||
|
осмиевая кислота |
|
черный цвет |
|
|
|
|
|||
|
(тетраоксид осмия) |
|
|
|
|
|
|
|
|
|
|
|
|
Нейтральные жиры – |
|
||||||
Жиры |
|
|
розовый |
цвет; |
эфиры |
|
||||
|
|
холестерина – |
розово- |
|
||||||
|
|
|
|
|||||||
|
|
|
фиолетовый |
|
цвет; |
|
||||
|
Нильский синий |
|
фосфатиды |
|
|
и |
|
|||
|
|
|
цереброзиды – голубой |
|
||||||
|
|
|
цвет; |
жирные кислоты |
|
|||||
|
|
|
и мыла – темно-синий |
|
||||||
|
|
|
цвет |
|
|
|
|
|
|
|
Амилоид |
|
|
Амилоид |
– |
|
ярко- |
||||
|
|
красный |
цвет; |
|
в |
|||||
(патологический |
Конго красный |
|
|
|||||||
|
поляризационном |
свете |
||||||||
белок) |
|
|
||||||||
|
|
– ярко-зеленый цвет |
|
|
||||||
|
|
|
|
|
||||||
Железосодержащие |
|
|
Гемосидерин |
– |
сине- |
|||||
соединения |
Реакция Перлса |
|
зеленый цвет |
|
|
|
|
|||
(гемосидерин) |
|
|
|
|
|
|
|
|
|
|
Кальций |
Ализарин красный |
|
Кальций |
– |
красно- |
|||||
|
оранжевый цвет |
|
|
|
||||||
|
|
|
|
|
|
|||||
Фосфаты |
Окраска по Коссе |
|
Фосфаты |
кальция |
– |
|||||
|
черный цвет |
|
|
|
|
|||||
|
|
|
|
|
|
|
||||
|
|
|
Гликоген, |
|
|
|
|
|||
Гликоген, нейтральные |
ШИК-реакция |
|
нейтральные |
|
|
|
|
|||
мукополисахариды |
|
мукополисахариды |
– |
|||||||
|
|
|||||||||
|
|
|
малиново-красный цвет |
|||||||
|
|
|
Гликозаминогликаны |
|||||||
Гликозаминогликаны |
Толуидиновый |
|
– |
сиренево-розовые; |
||||||
синий |
|
остальные |
структуры |
– |
||||||
|
|
|||||||||
|
|
|
голубые |
|
|
|
|
|
||
|
|
|
РНК – красный цвет; |
|||||||
РНК |
Реакция Браше |
|
другие структуры ядра |
|||||||
|
|
|
клетки – зеленый цвет. |
|||||||
ДНК |
Реакция Фёльгена |
|
ДНК |
– |
пурпурно- |
|||||
|
красный цвет |
|
|
|
|
|||||
|
|
|
|
|
|
|
||||

13
Для изготовления гистологических препаратов в рамках срочной (cito) биопсии используют специальный замораживающий микротом.
III) Метод цитологического исследования
Цитологическое исследование проводят по мазкам, сделанным из содержимого полых органов, а так же по препаратам-отпечаткам, пунктатам и аспиратам (аспирационным пунктатам). Мазки нередко изготавливают из материала смывов со стенок органов, что позволяет захватить клетки, находящиеся в процессе естественного или патологического слущивания (десквамация, эксфолиация), например с шейки матки. Нередко препараты изготавливают из мокроты, слизи, тканевых вытяжек и осадков в жидкостях.
Наиболее популярные окраски при исследовании цитологического материала:
азур-II-эозином (тинкториальные свойства близки к гематоксилину и эозину);
бисмарк-брауном по Папаниколау.
IV) Метод иммуногистохимического исследования
При некоторых патологических состояниях, особенно опухолях, бывает трудно и даже невозможно с помощью гистоили цитологических окрасок определить тип ткани или её происхождение (гистогенез), поэтому используют различные дополнительные методы. Одним из них является иммуногистохимический метод.
Иммуногистохимическое исследование – метод микроскопического исследования тканей, обеспечивающий наиболее специфическое выявление в них искомых веществ и основанный на обработке срезов маркированными специфическими антителами к выявляемому веществу, которое в данной ситуации служит антигеном.
Виды иммуногистохимического исследования:
1.По принципу реакции:
прямой иммуногистохимический метод – реакция специфического связывания маркированных антител непосредственно с выявляемым веществом;
непрямой иммуногистохимический метод – немаркированные первичные антитела связываются с искомым антигеном (выявляемым веществом), а далее уже их выявляют при помощи вторичных меченых антител.
2.По способу маркировки антител:
флуоресцентные красители (флуоресцеин);
14
ферменты (щелочная фосфатаза, пероксидаза хрена);
электронно-плотные частицы (коллоидное золото).
3.По виду применяющихся антител:
моноклональные антитела;
поликлональные антитела.
При проведении данного исследования, если искомый антиген есть в изучаемых тканях или клетках, возникающий комплекс антигенантитело в сочетании с маркером точно укажут локализацию и количество последнего. В настоящее время данный метод становится ведущим в точной диагностике опухолей, а его применение – обязательным компонентом лечебно-диагностического процесса.
IV) Молекулярно-биологические методы исследования
Для прижизненной диагностики в ряде случаев применяют методы молекулярной биологии:
1.Проточная цитометрия – для количественного анализа содержания ДНК в клетках опухолей и других патологических субстратов;
2.Техника гибридизации in situ – для идентификации по геному микробов или вирусов, находящихся в тканях или жидкостях; для изучения генома при его врождённых нарушениях; при диагностике опухолей для распознавания вирусных онкогенов:
FISH анализ (от англ.: fluorescence in situ hybridization) –
цитогенетический метод, который применяют для детекции и определения положения специфической последовательности ДНК и/или мРНК in situ;
CISH анализ (от англ.: chromogenic in situ hybridization) –
цитогенетический метод гибридизации in situ с использованием хромогенов, что позволяет оценить результат с использованием обычного светового микроскопа;
DISH анализ (от англ.: dual in situ hybridization) –
цитогенетический метод гибридизации in situ с возможностью одновременного выявления экспрессии двух последовательностей ДНК.
V) Метод электронной микроскопии
В ходе диагностических исследований на материале, взятом при жизни больного, нередко используется электронная микроскопия – трансмиссионная (в проходящем пучке, подобно светооптической микроскопии) или сканирующая (снимающая рельеф поверхности). Первую применяют чаще, особенно для изучения в ультратонких

15
срезах ткани деталей строения клеток, выявления микроорганизмов, вирусов, отложений иммунных и других комплексов.
ФОРМУЛИРОВКА ПАТОЛОГОАНАТОМИЧЕСКОГО ДИАГНОЗА
Патологоанатомическое исследование завершается формулировкой патологоанатомического диагноза и составлением патологоанатомического эпикриза с определением непосредственной причины и механизма смерти, сопоставлением клинического и патологоанатомического диагнозов, установлением характера и причины недостатков в оказании медицинской помощи.
Патологоанатомический диагноз представляет собой медицинское заключение о сущности заболевания, отображающее его нозологию, этиологию, патогенез и морфологически-функциональные проявления, выраженные в терминах, предусмотренных Международной классификацией болезней и причин смерти.
Патологоанатомический диагноз формулируется по нозологическому принципу, с выделением следующих рубрик в патогенетической последовательности:
основное заболевание;
осложнение основного заболевания;
сопутствующие заболевания и их осложнения.
Основное заболевание – нозологическая форма, которая в соответствии с классификацией и номенклатурой заболеваний сама по себе или через свои осложнения привела
ксмерти.
Всоответствии с классификацией диагноз основного заболевания может быть:
монокаузальным – одно заболевание;
бикаузальным – два заболевания (конкурирующие заболевания, сочетанные заболевания, основное и фоновое заболевание) – см. ниже;
мультикаузальным – три и более заболевания.
Конкурирующие заболевания – это нозологические единицы,
каждая из которых сама по себе или через свои осложнения могла привести к смертельному исходу.

16
Сочетанные заболевания – это нозологические единицы, каждая из которых сама по себе не является смертельной для данного больного, но их взаимное негативное влияние на организм пациента столь велико, что является причиной летального исхода.
Фоновые заболевания – это заболевания, имеющие основное значение в возникновении или неблагоприятном течении другого (основного) заболевания, которое явилось причиной смерти.
После указания нозологической формы основного заболевания необходимо перечислить наиболее выраженные его морфологические проявления, форму и стадию развития процесса. В рубрику основного заболевания включаются оперативные вмешательства, производившиеся в связи с ним с обозначением даты их проведения, способа и модификации выполнения.
Осложнение основного заболевания (оперативного вмешательства, медицинской манипуляции) – патологический процесс, синдром, нозологическая единица, которые связаны с ним патогенетически (непосредственно или опосредованно) и усугубили его клиническое течение.
Осложнения указываются в хронологической последовательности с учётом их взаимной патогенетической связи. Если в связи с осложнением производились какие-либо операции или другие сложные врачебные вмешательства, такие как гемодиализ, то они должны быть указаны в рубрике осложнений.
Сопутствующее заболевание – нозологическая форма
(единица), патологический процесс или остаточные явления после ранее перенесенных болезней, этиологически и патогенетически не связанные с основным заболеванием и его осложнениями, не оказавшие на их течение и развитие неблагоприятного влияния и не способствовавшие наступлению смерти
Наконец, указывают непосредственную причину смерти.
Непосредственная причина смерти – патологическая реакция, процесс, синдром, нозологическая единица или совокупность функциональных состояний, которые привели к необратимым изменениям в жизненно важных органах.
17
Непосредственной причиной смерти может быть как основное заболевание, так и его осложнения (кровопотеря, шок, пневмония, перитонит и прочие).
Сопоставление клинического и патологоанатомического диагнозов производится по основному заболеванию, по его осложнениям и по сопутствующему заболеванию.

18
РАЗДЕЛ II
►ПОВРЕЖДЕНИЕ И ГИБЕЛЬ КЛЕТОК И ТКАНЕЙ◄
ДИСТРОФИИ
Дистрофия – патологический процесс, в основе которого лежат нарушения тканевого (клеточного) метаболизма, ведущие к структурным изменениям. В связи с этим дистрофия рассматривается как один из видов повреждения (альтерации).
Классификация дистрофий
1.В зависимости от преобладания морфологических изменений в специализированных клетках или строме и сосудах:
паренхиматозные;
стромально-сосудистые;
смешанные.
2.В зависимости от вида нарушения обмена:
белковые (диспротеинозы);
жировые (липидозы);
углеводные;
минеральные.
3.В зависимости от распространенности процесса:
местные;
системные (общие).
4.В зависимости от происхождения:
приобретенные;
наследственные.
ЭТИОЛОГИЯ
Дистрофии относят к повреждениям или альтеративным процессам – это изменение структуры клеток, межклеточного вещества, тканей и органов, которое сопровождается нарушением их жизнедеятельности. Эти изменения, как филогенетически наиболее древний вид реактивных процессов, встречается на самых ранних этапах развития живого организма.
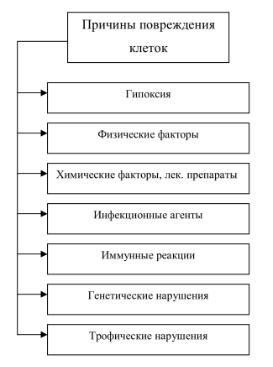
Повреждения способны вызвать самые разнообразные причины (рис. 1). Они воздействуют на клеточные и тканевые структуры непосредственно или через гуморальные и рефлекторные влияния. Характер и степень повреждения зависят от силы и природы патогенного фактора, строения и функции органа, а также от реактивности организма. В одних случаях возникают поверхностные и
19
обратимые изменения, касающиеся ультраструктур, а в других – глубокие и необратимые, которые могут завершиться гибелью не только клеток и тканей, но и целого органа.
Непосредственной причиной развития дистрофий могут служить нарушения как клеточных, так и внеклеточных механизмов, обеспечивающих трофику:
расстройство ауторегуляции клетки (токсин, радиация,
отсутствие ферментов) приводят к дефициту энергии и нарушению ферментативных процессов в клетке;
нарушение работ транспортных систем, обеспечивающих метаболизм и структуру клеток, вызывает гипоксию, которая является ведущей причиной в патогенезе дистрофии;
расстройство эндокринной регуляции трофики или нарушение нервной регуляции трофики ведут к эндокринной или нервной дистрофии.
Рис. 1. Причины повреждения клеток
ПАТОГЕНЕЗ
Есть четыре основных патогенетических механизма развития дистрофий (рис. 2):

20
Инфильтрация – избыточное проникновение продуктов обмена из крови и лимфы в клетки и межклеточное вещество. Существует два типа инфильтрации: в первом случае клетка получает избыточное количество какого-либо вещества
1. и через некоторое время клетка не может ассимилировать этот избыток; во втором случае
характерно понижение уровня жизнедеятельности клетки, в результате чего она не справляется даже с нормальным количеством поступающего вещества.
Декомпозиция (фанероз) – распад ультраструктур клеток и межклеточного вещества, ведущий к нарушению тканевого (клеточного) метаболизма и накоплению продуктов нарушенного обмена в тканях
2. (клетке). Главным образом, происходит распад белково-
липидных комплексов, которые входят в состав мембран органелл. Свободные белки гидролизуются с участием ферментов лизосом или подвергаются денатурации.
Извращенный синтез – синтез в клетке веществ, не встречающихся в ней в норме. Примеры: синтез патологического
3.белка амилоида, алкогольного гиалина, гликогена в эпителии почек, кератина в эпителии
слезной железы, патологических пигментов и др.

21
Трансформация – образование продуктов одного вида обмена из общих исходных продуктов, которые идут на построение белков, жиров, углеводов. Процесс характеризуется
4. биохимическим преобразованием соединений в другие, например жиров и углеводов в белки или
белков и углеводов в жиры, повышенный синтез гликогена из глюкозы и т.д., с избыточным накоплением вновь образованных соединений.
Рис. 2. Механизмы развития дистрофий
Проявления дистрофий могут варьировать по степени выраженности и обратимости. Все стрессовые факторы и неблагоприятные агенты проявляют свое действие, в первую очередь, на молекулярном или биохимическом уровне. Существует временной промежуток между воздействием повреждающего фактора и морфологическими проявлениями клеточной альтерации или гибели клетки. Продолжительность этого периода может варьировать в зависимости от интенсивности действия повреждающего фактора, адаптационных резервов, а также чувствительности методов, которые используются для оценки изменений. Так, при использовании гистохимических или ультраструктурных методов исследования
