
2 курс / Нормальная физиология / Общий_курс_физиологии_человека_и_животных_Том_2_Ноздрачев_А_Д_,
.pdfбета-МСГ, которые являются полипептидами и весьма близки к АКТГ. Альфа-форма МСГ человека содержит 13 аминокислотных остатков, бета — 22.
Основная функция МСГ заключается в стимуляции биосинтеза кожного пигмента меланина, а также увеличении размеров и количества пигментных клеток. Действие МСГ у рыб, амфибий и пресмыкающихся состоит в увеличении пигментации кожи за счет дисперсии меланина в пигментных клетках (меланофорах или меланоцитах). Изменение окраски кожных покровов имеет существенное защитное значение, так как животное может иметь окраску, близкую к цвету окружающей среды. У млекопитающих МСГ участвует в сезонных изменениях пигментации кожи и меха; этот гормон может влиять и на возбудимость нервной системы. Роль МСГ у млекопитающих пока недостаточно выяснена. Регуляция функции клеток промежуточной доли гипофиза, вырабатывающих МСГ, осуществляется гипоталамическими ингибирующими и рилизинг-факторами (МСГИГ, МСГ-РГ).
6.3. Эндокринные железы, находящиеся под контролем гормонов аденогипофиза
Действие четырех из семи гормонов аденогипофиза (см. разд. 6.2) состоит в основном в регуляции выработки других гормонов эндокринными железами, функция которых тесно связана с деятельностью гипоталамо-гипофизарной системы. Тиреотропный гормон аденогипофиза стимулирует выработку тиреоидных гормонов в щитовидной железе, адренокортикотропный гормон влияет на секрецию глюкокортикоидов корой надпочечника, а гонадотропные гормоны приводят к выработке половых гормонов стероидогенной тканью гонад. В коре надпочечника синтезируются также минералокортикоиды (альдостерон), а в мозговом веществе надпочечника — катехоламины. В пределах расположения щитовидной железы у млекопитающих специальными клетками вырабатывается гормон кальцитонин. Функции этих гормонов будут рассмотрены позже, так как их выработка и выделение частично или полностью независимы от гипоталамо-гипофизарной системы.
6.3.1. Щитовидная железа и ее гормоны — тироксин и трийодтиронин
Щитовидная железа образуется из выпячивания на вентральной стенке глотки между I и II жаберными карманами. Основной особенностью щитовидной железы, имеющейся у всех позвоночных, является способность ее клеток поглощать йод из окружающей среды и
вкомбинации с аминокислотой тирозином синтезировать тиреоидные гормоны.
Умногих представителей беспозвоночных (моллюски, черви и др.) также существуют структуры, способные к синтезу йодопротеинов. У хордовых животных (ланцетник и др.) на вентральной стенке глотки существует желобок, называемый эндостилем. Его клетки наряду с выполнением пищеварительной функции способны поглощать йод и синтезировать тиреоидные гормоны — тироксин и трииодтиронин, которые поступают в кишечник, а затем разносятся кровью по всему организму. Следовательно, эндостиль является железой с экзокринной секрецией.
Унизших позвоночных (миксины, личинки миног) возникает специализация клеток; часть из них выполняет железистую функцию, другие — пищеварительную. У взрослых миног из эндостиля образуются фолликулы щитовидной железы, имеющиеся и у всех других позвоночных животных.
Основной структурной и функциональной единицей щитовидной железы является фолликул (рис. 6.6). Стенка фолликула образована тиреоидным эпителием, в полости фолликула находится так называемый коллоид, в котором содержатся тиреоидные гормоны. Фолликулы окружены соединительной тканью с кровеносными сосудами. Щитовидная железа обильно снабжается кровью; по капиллярам поступают компоненты,
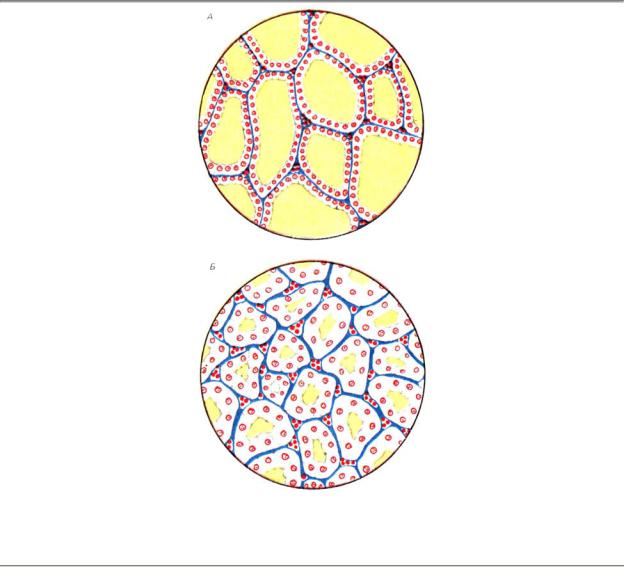
необходимые для образования гормонов, и выводятся синтезированные гормоны.
Рис. 6.6. Фолликулы щитовидной железы крысы при неактивном (А) и активном (Б) состояниях железы:
А — эпителий плоский, фолликулы содержат много коллоида; Б — тиреоидный эпителий высокий, в полости фолликулов мало коллоида
У ряда низших позвоночных (круглоротые, костистые рыбы) группы фолликулов лежат разрознено, и щитовидная железа носит диффузный характер. В ходе дальнейшей эволюции у других групп рыб и у наземных позвоночных щитовидная железа становится более компактной. У млекопитающих она состоит обычно из двух долей, соединенных перешейком, и локализована в области трахеи. Кроме фолликулов в щитовидной железе млекопитающих обнаружены так называемые парафолликулярные, светлые или С-клетки, вырабатывающие кальцитонин (или тиреокальцитонин). Эти клетки по эмбриональному происхождению отличаются от тиреоидных и у других позвоночных входят в состав ультимобранхиальных желез; в связи с этим функции кальцитонина будут рассмотрены отдельно.
Основная особенность клеток щитовидной железы. Этой особенностью является способность щитовидной железы активно извлекать йод из плазмы крови против химического и электрического градиентов, накапливать его и преобразовывать в органически связанный йод и физиологически активные тиреоидные гормоны. Пути биосинтеза тиреоидных гормонов у всех позвоночных сходны. В щитовидной железе под действием тиреотропного гормона вырабатываются два гормона: тетраиодтиронин (тироксин, T4) и трийодтиронин (Т3). Трийодтиронин вырабатывается в меньших количествах, чем тетрайодтиронин, но значительно превосходит его по активности.
Отличительной особенностью тиреоидных гормонов является содержание йода. Йод поступает в основном с пищей и водой. Т4 содержит четыре атома йода, связанных с
тирониновым ядром, Т3 — три атома. Компоненты образования тиреоидных гормонов соединяются с гликопротеином — тиреоглобулином — и поступают в коллоид в полости фолликула. При поступлении в кровь путем протеолиза Т3 и Т4 отщепляются от тиреоглобулина, но в плазме они вновь соединяются с тироксинсвязывающим глобулином и лишь небольшая часть Т3 и Т4 остается в крови в активном состоянии. Степень стимулирующего эффекта тироксина зависит, как правило, от уровня свободного тироксина. Основные данные о синтезе тиреоидных гормонов и их функциях получены в
работах с использованием радиоактивного изотопа 131 I в качестве метки.
Действие гормонов щитовидной железы. Трийодтиронин и тетрайодтиронин обладают примерно одинаковым действием, но активность Т3 почти в пять раз выше, чем Т4. Эффекты Т4 развиваются через более длительный латентный период; он может превращаться в организме в Т3 путем деиодирования. В связи с этим предполагают, что Т4 может являться прогормоном.
Тиреоидные гормоны имеют широкий спектр действия. Их основные эффекты состоят во влиянии на различные обменные процессы, рост и развитие, они участвуют также в адаптивных реакциях.
Наиболее выражено влияние Т3 и Т4 на энергетический обмен. В отсутствие тиреоидных гормонов скорость обменных процессов снижается; при их избытке основной обмен в покое может повышаться почти вдвое по сравнению с нормой. Калоригенный эффект наиболее четко выражен у высших позвоночных и проявляется на всех клетках растущего организма, но особенно на клетках нервной системы.
Гормоны действуют путем индукции ферментов и активации митохондриальных ферментов, что увеличивает синтез белка и окислительный распад жиров и углеводов. Таким образом, тиреоидные гормоны действуют на разные стороны обмена веществ. У различных животных четко доказана их роль в регуляции минерального обмена. Так, тироксин способствует сохранению градиента электролитов между вне- и внутриклеточной средой. Показана роль тиреоидных гормонов в обмене кальция и магния.
Действие Т3 и Т4 состоит также в повышении чувствительности тканей к катехоламинам; они усиливают гликогенолитическое и гипергликемическое действие катехоламинов. На ряд процессов тиреоидиные гормоны оказывают сенсибилизирующее или пермиссивное действие. Т3 и Т4 участвуют в регуляции выделения глюкокортикоидов надпочечниками, гормона роста аденогипофизом.
Тетрайодтиронин стимулирует общий рост тела, поэтому его недостаток может привести к карликовости. Роль тиреоидных гормонов наиболее четко прослеживается у молодых животных. Недостаток этих гормонов сопровождается нарушением состояния нервной системы, задержкой роста и развития. При гипотиреозе в молодом возрасте нарушается умственное развитие; при недостатке гормонов в эмбриональный период наблюдается тяжелая умственная отсталость.
Тиреоидные гормоны оказывают стимулирующее влияние на процессы метаморфоза, что наиболее четко показано на амфибиях. При помещении головастиков лягушки в воду, не содержащую йода, не осуществляется метаморфоз; добавление йода или тиреоидных гормонов приводило к осуществлению метаморфоза и развитию во взрослые формы.
Тиреоидэктомия сопровождается задержкой развития половых желез, что свидетельствует о необходимости тиреоидных гормонов для нормальной половой функции. Они имеют большое значение при сезонных адаптациях у различных животных. При осуществлении приспособительных изменений в организме тиреоидные гормоны действуют совместно с другими гормонами, прежде всего с глюкокортикоидами.
Регуляция концентрации тиреоидных гормонов. Уровень Т4 и Т3 в крови в нормальных условиях варьирует в очень узких пределах. В ситуациях, которые требуют повышенной концентрации тиреоидных гормонов, их секреция соответственно возрастает.

Секреция тиреоидных гормонов регулируется тиреотропным гормоном (ТТГ), уровень которого, в свою очередь, зависит в значительной степени от стимуляции ТРГ. Тиреотропин действует на мембраны эпителиальных клеток щитовидной железы, вызывая увеличение синтеза гормонов и их секреции путем стимуляции аденилатциклазы. ТТГ стимулирует все фазы метаболизма йода, иодизацию тирозина и синтез тироксина, а также протеолитическую деградацию тиреоглобулина и отдачу тиреоидных гормонов.
Функция щитовидной железы, как и других эндокринных желез, находящихся под влиянием гипоталамо-гипофизарной системы, регулируется по принципу отрицательной обратной связи. При снижении секреции Т3 и Т4 содержание ТТГ в плазме повышается; напротив, концентрацию ТТГ можно снизить введением Т3 и Т4. В систему регуляции входит также гипофизотропная зона гипоталамуса, где вырабатывается ТРГ, стимулирующий выработку ТТГ гипофизом (рис. 6.7). Тироксин тормозит секрецию как ТТГ, так, очевидно, и ТРГ. Возможно, что накапливающиеся в щитовидной железе тиреоидные гормоны могут подавлять свое собственное образование и выведение Т4 в кровь. Это может быть одним из факторов, регулирующих дальнейший синтез гормона. На секрецию Т3 и Т4 оказывают влияние факторы, действующие через внутренние и наружные терморецепторы.
Рис. 6.7. Регуляция уровня тиреоидных гормонов с включением механизмов влияния через терморецепторы и стресс-факторы:
Т3 — трийодтиронин, Т4 — тироксин, ТРГ — тиреотропин-рилизинг-гормон, ТТГ — тиреотропный гормон; красными стрелками обозначено прямое, стимулирующее влияние различных факторов, синими — торможение по типу обратной связи
Патофизиология. Тиреоидные гормоны играют важную роль в регуляции жизненно важных функций организма, изменение уровня их содержания приводит к тяжелым патологическим состояниям. Давно известный синдром диффузного токсического зоба (базедова болезнь, болезнь Гревса) возникает из-за образования (очевидно, в вилочковой железе) длительно действующего стимулятора щитовидной железы, который обладает свойствами ТТГ. Его выделение не тормозится механизмом отрицательной обратной связи, и поэтому он неограниченно стимулирует образование тиреоидных гормонов. Этот стимулятор нарушает иммунологические процессы в организме, в связи, с чем базедову болезнь рассматривают как аутоиммунное заболевание.
Предполагают, что стимулятор представляет собой антитело к рецептору ТТГ в
аденогипофизе. Избыточная продукция тиреоидных гормонов приводит к активации катаболизма белков, в результате чего и может наступить отрицательный азотистый баланс. При этом происходят также нарушение углеводного обмена, торможение перехода углеводов в жиры, усиление мобилизации жира, нарушение водного и минерального обмена, нарушаются процессы окислительного фосфорилирования. Заболевание сопровождается похуданием, тахикардией, повышенной нервной возбудимостью, часто наблюдается пучеглазие (экзофтальм).
Среди других заболеваний, связанных с увеличением продукции тиреоидных гормонов,
часто встречается узловой токсический зоб (токсическая аденома). В этом случае в щитовидной железе образуется узел (аденома), автономно продуцирующий повышенные количества тиреоидных гормонов. Теоретически возможен также гипертиреоз, связанный с повышением секреции ТТГ; однако такое заболевание наблюдается крайне редко.
Гипотиреоидное состояние связано с пониженной продукцией тиреоидных гормонов. Как правило, оно возникает в результате разрастания ткани щитовидной железы. Это происходит потому, что Т3 и Т4 не включаются в необходимой степени (из-за их малого количества) в цепь регуляции обратной связи. В результате продолжается выработка ТТГ, который и приводит к дальнейшему увеличению щитовидной железы. Нарушение секреции тиреоидных гормонов часто связано с недостаточным количеством иода в пище (эндемический зоб). Развитие этой формы зоба наблюдается в различных районах земного шара, в частности в Альпах. В этих случаях введение йода с пищей предотвращает развитие заболевания.
Другие формы гипотиреоза возникают в связи с генетическими нарушениями синтеза тиреоидных гормонов или вследствие аутоиммунного разрушения железы. Гипотиреоз может наблюдаться также при нарушении секреции ТТГ гипофизом и ТРГ гипоталамусом. При отсутствии тиреоидных гормонов в период эмбрионального развития наблюдается умственная отсталость. Синдром полного отсутствия у детей тиреоидных гормонов называют кретинизмом. Снижение окислительных процессов и понижение синтеза белка приводят к задержке роста у детей. У взрослых недостаточность функции щитовидной железы вызывает умственную и физическую отсталость. При этом происходит нарушение белкового (понижение синтеза и распада белка), углеводного (гипогликемия), водного и минерального обмена, наблюдается брадикардия. Этот синдром называют микседемой; он сопровождается тестовидным утолщением кожи, связанным с увеличением объема соединительной ткани и задержкой в ней воды и мукопротеинов.
Многие результаты по действию тиреоидных гормонов получены на основе данных по удалению щитовидной железы с замещающей терапией тиреоидными гормонами или ТТГ. Определенное значение в изучении физиологии щитовидной железы имело применение различных антитиреоидных веществ, ингибирующих ее функцию. Важную роль здесь играют также особенности цитоморфологии щитовидной железы, выявляемые на основании гистологического и электронно-микроскопического анализа. Однако в настоящее время наибольшее значение имеют методы радиоиммунологического анализа концентраций Т3, Т4 и ТТГ в плазме. Плодотворным методом является введение
радиоактивного изотопа 131 I (или 123 I) и регистрация его поглощения щитовидной железой с получением «карты» распределения его излучения. Так, в частности, возможно определение функции щитовидной железы при различных состояниях организма. Скорость падения радиоактивности в этом случае служит мерой выделения тиреоидных гормонов.
6.3.2. Кора надпочечника и кортикостероиды
Надпочечник — это парный орган, лежащий над почкой и состоящий из двух частей, которые различаются по своему происхождению, морфологии и функции — коры и
мозгового вещества. Кора развивается из складки целомического эпителия, из которого образуются и гонады. Клеточные элементы из брюшных симпатических ганглиев мигрируют в область расположения коркового вещества и в дальнейшем образуют клетки мозгового вещества надпочечников, вырабатывающие катехоламины. Такое происхождение объясняет близость гормонов, выделяющихся в коре надпочечника и в железистой ткани гонад: и те, и другие являются стероидами. Понятна также синэргичность симпатической нервной системы и гормонов мозгового вещества надпочечника.
У низших позвоночных гомологом коры надпочечника является интерреналовая железа — островки железистой ткани, вырабатывающей кортикостероиды. Они разбросаны в ткани головной и отчасти туловищной почки. Хромаффинная ткань, являющаяся гомологом мозгового вещества надпочечника, разобщена с интерреналовой и находится вблизи крупных кровеносных сосудов.
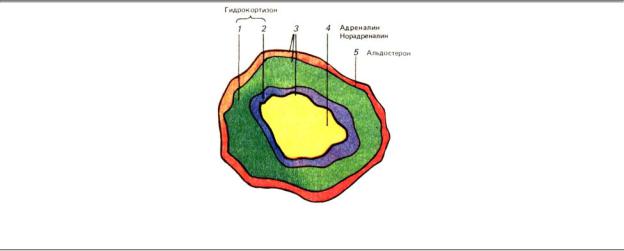
В ходе эволюции позвоночных происходила постепенная концентрация структур интерреналовой и хромаффинной ткани и их объединение в одну железу — надпочечник. Уже у рептилий образуется единый парный орган, характерный также и для более высокоорганизованных позвоночных и человека (рис. 6.8). По-видимому, гормоны коры надпочечника повышают способность мозгового слоя к синтезу гормонов, и поэтому объединение коры и мозгового вещества в один орган дает определенное преимущество.
Рис. 6.8. Надпочечник и его гормоны: 1 —- пучковая зона, 2 — сетчатая зона, 3 — кора надпочечника, 4 — мозговое вещество, .5 — клубочковая зона
Кора надпочечника. Кора надпочечника у млекопитающих состоит из трех слоев: клубочковой зоны, лежащей снаружи, пучковой зоны и сетчатой, прилежащей к мозговому веществу. Надпочечник имеет обильное кровоснабжение.
Из коры надпочечника выделено около 50 различных стероидов. Большинство из них являются промежуточными продуктами синтеза активных гормонов. Основным субстратом для синтеза стероидных гормонов является холестерин, поступающий в клетки с кровью. В клетках он хранится в виде эфиров или других соединений в липидных каплях или липосомах, представляющих собою депо холестерина. В процессе синтеза стероидов большую роль играют митохондрии, эндоплазматический ретикулум, комплекс Гольджи. Ряд этапов синтеза стероидов осуществляется в митохондриях, в связи с этим в стероидогенных тканях эти органоиды имеют везикулярные кристы.
В коре надпочечника вырабатываются гормоны, называемые кортикостероидами или кортикоидами. Они разделяются на две основные группы: глюкокортикоиды, выделяемые пучковой и сетчатой зонами, и минералокортикоиды, образующиеся в наружной клубочковой зоне. Кроме того, в коре надпочечника, главным образом в сетчатой зоне, секретируются небольшие количества половых стероидов, главным образом андрогенов.
Состав секретируемых кортикостероидов различается у разных животных; у человека только три кортикоида секретируются в виде гормонов: кортизол (гидрокортизон), альдостерон и в меньшей степени кортикостерон. В крови гормоны находятся в
связанном состоянии с белком-носителем — транскортином.
Действие кортикоидов. Кортикоиды обладают широким спектром действия. Удаление обоих надпочечников приводит к смерти животного. Основным действием глюкокортикоидов является влияние на углеводный обмен; минералокортикоиды (альдостерон) связаны с балансом электролитов. Такое разделение действия кортикостероидов характерно для высших позвоночных.
У млекопитающих требуется введение очень высоких доз глюкокортикоидов, чтобы выявить их минералокортикоидный эффект, а глюкокортикоидное действие альдостерона выражено столь слабо, что практически равно нулю. Однако у низших позвоночных такого четкого разделения влияний кортикостероидов нет. У большинства рыб в интерреналовой железе вообще не вырабатываются минералокортикоиды; в этом случае глюкокортикоиды обладают более широким спектром действия и кроме влияний на углеводный обмен оказывают минералокортикоидное действие. Лишь с выходом позвоночных на сушу у амфибий начинает в больших количествах вырабатываться альдостерон и в дальнейшем ходе эволюции развиваются специфические эффекты двух групп кортикостероидов.
Эффекты глюкокортикоидов. Влияние глюкортикоидов весьма разнообразно и выявляется весьма четко у животных после удаления надпочечников (адреналэктомии) и введения альдостерона. Так, синтез глюкозы из аминокислот — глюконеогенез — находится под регулирующим влиянием кортизола. У этого гормона несколько путей влияния, но преимущественно его воздействие осуществляется за счет увеличения активности ряда ферментов, необходимых для глюконеогенеза. Глюкоза, вырабатываемая
врезультате введения кортизола, восполняет запасы гликогена в печени, истощенные после удаления коры надпочечника. Таким образом, кортизол увеличивает образование и отложение гликогена в печени и мышцах и повышает уровень глюкозы в крови.
Глюкокортикоиды обладают катаболическим действием. Они тормозят синтез белков
впериферических тканях и усиливают их катаболизм. Аминокислоты, поступающие в печень в результате катаболизма белков, служат субстратом для глюконеогенеза. Избыток кортизола приводит к атрофии мышц. В отсутствие глюкокортикоидов нарушаются мобилизация и выделение жирных кислот из жировой ткани, т. е. липолиз. Благодаря повышению кровотока в клубочках и усилению клубочковой фильтрации кортизол обеспечивает экскрецию воды. Он обладает также специфическим влиянием на экскрецию мочи — снижает проницаемость для воды дистального отдела канальцев. При недостаточности коры надпочечника наблюдается мышечная слабость, проявления которой снижаются при введении кортизола.
Вголовном мозгу обнаружены многочисленные рецепторы глюкокортикоидов, благодаря чему эти гормоны оказывают разнообразное действие на функцию ЦНС и органов чувств. При недостаточности коры надпочечников нарушается способность различать оттенки вкусовых, обонятельных и звуковых ощущений; введение глюкокортикоидов способствует нормализации функции. Глюкокортикоиды, видимо, влияют на процессы обработки информации в центрах мозга, регулируя интеграцию сенсорных импульсов, хотя механизм их влияния пока не ясен.
Глюкокортикоиды оказывают значительное влияние на клеточный и гуморальный иммунитет. При снижении активности коры надпочечников происходит увеличение тимуса и лимфатических узлов. Введение глюкокортикоидов нормализует функцию этих органов. Кортизол обладает четким противовоспалительным действием, в связи, с чем его применяют при лечении ревматических заболеваний.
Концентрация глюкокортикоидов поддерживается в течение более или менее длительных периодов времени на постоянном уровне за счет специальных регуляторных механизмов, хотя существуют циркадные колебания. Например, у человека продукция кортизола максимальна в утренние часы и снижена ночью. 90 % глюкокортикоидов связано с белками крови.

Регуляция секреции глюкокортикоидов. Схема регуляции секреции глюкокортикоидов такова. Рилизинг-гормон КРГ, образованный в гипофизотропной зоне гипоталамуса (см. разд. 6.2), поступает в гипофиз и вызывает выделение АКТГ. Последний доставляется кровью к коре надпочечника, где он стимулирует синтез и секрецию глюкокортикоидов (рис. 6.9).
Рис. 6.9. Регуляция секреции глюкокортикоидов в коре надпочечника: КРГ — кортикотропин-рилизинг-
гормон; красными стрелками обозначено стимулирующее влияние различных факторов, синими — торможение по типу отрицательной обратной связи, пунктиром — «короткая отрицательная обратная связь»
Введение АКТГ крысе уже через 2 мин приводит к увеличению уровня глюкокортикоидов. Образование КРГ в гипофизотропной зоне гипоталамуса находится под контролем высших отделов ЦНС, которые получают и перерабатывают сигналы, поступающие с периферии организма. На секреторной активности коры надпочечников отражаются эмоциональное состояние и поведение.
Введение глюкокортикоидов в гипофизотропную зону вызывает снижение секреции АКТГ. Секреция АКТГ изменяется также при их инъекции в аденогипофиз. Очевидно, что в гипофизотропной зоне и в гипофизе располагаются рецепторы глюкокортикоидов. Возможно, АКТГ способен и непосредственно ингибировать свою собственную выработку через так называемую короткую цепь обратной связи. При этом этот гормон влияет на функцию нейросекреторных клеток, вырабатывающих КРГ.
Изменения концентрации глюкокортикоидов особенно отчетливо выступают при предъявлении к организму особых требований — стресс. Автор теории стресса Г. Селье выделяет три его фазы: тревоги, резистентности и истощения. Стресс-реакция может пройти бесследно, если воздействие не очень сильное; при его повторении возможна адаптация к этому стимулу. В некоторых случаях реакция на стресс-фактор может оказаться столь интенсивной, что произойдут опустошение всех запасов глюкокортикоидов в коре надпочечников и ее разрушение. В этом случае введение глюкокортикоидов облегчает ситуацию.
Патофизиология. Из анализа эффектов глюкокортикоидов следует, что как гиперфункция, так и снижение выработки этих гормонов приводят к серьезным нарушениям функций организма. В результате повышенного содержания кортизола
наблюдаются ожирение, гипергликемия, усиленный распад белков (катаболическое действие), задержка воды и хлорида натрия в организме (отеки), гипертензия, пониженная резистентность. При недостаточности функции коры надпочечников, снижении выработки кортикостероидов развивается тяжелое состояние — бронзовая, или аддисонова, болезнь. Она характеризуется бронзовой окраской кожи, ослаблением сердечной мышцы, повышенной утомляемостью, восприимчивостью к инфекциям.
6.3.3.Гонады и половые гормоны
Вгонадах происходит развитие и созревание половых клеток, а также выработка половых гормонов.
Процессы развития, созревания половых клеток и размножения значительно различаются у разных позвоночных, в связи, с чем наблюдаются особенности и в механизмах их гормональной регуляции. У рыб, амфибий, рептилий и птиц в яйцах накапливается желток, необходимый для развития эмбриона, которое протекает в большинстве случаев вне тела самки. Большой сложности достигает репродуктивная система млекопитающих (см. гл. 13), у которых развитие эмбриона происходит в теле самки. У большинства видов млекопитающих образуется плацента — специальный орган, обеспечивающий развитие плода и вырабатывающий собственные гормоны.
Восуществлении функции размножения принимает участие ряд гормонов, однако основное значение имеют половые гормоны, которые относятся к стероидам. Их можно разделить на три основные группы: эстрогены, гестагены и андрогены. Гормоны первых двух групп называют также женскими половыми гормонами, важнейшими из них являются эстрадиол, эстрон и прогестерон. Третья группа — мужские половые гормоны.
Из них наиболее важным является тестостерон.
Локализация выработки половых гормонов. Этот процесс осуществляется стероидогенной тканью гонад, развивающейся, так же как и кора надпочечника, из целомического эпителия. Синтез стероидов в этих образованиях происходит сходным путем; в гонадах из прогестерона (центральное звено синтеза) образуются андрогены и эстрогены. Пути синтеза и обеспечивающая их система ферментов обнаружены у всех позвоночных и некоторых групп беспозвоночных животных. Это указывает на значительную древность, стабильность и универсальность половых стероидов, играющих важную роль в обеспечении репродукции и, следовательно, в сохранении вида.
Эстрогены и гестагены образуются в женской гонаде и плаценте (у плацентарных млекопитающих), а андрогены — в так называемых клетках Лейдига (или интерстициальных) в мужской гонаде. В яичнике половые гормоны образуются в оболочках фолликула. У млекопитающих, в яичниках которых в ходе цикла на месте лопнувшего фолликула образуется желтое тело (см. разд. 13.9), в этом образовании синтезируются прогестины. Небольшие количества андрогенов вырабатываются у особей женского пола; они образуются в яичнике и в коре надпочечника (см. разд. 6.3.2). В семенниках также вырабатываются небольшие количества эстрогенов и гестагенов.
Действие половых гормонов. Гормоны, образующиеся в гонадах, способствуют эмбриональной дифференцировке (у млекопитающих) и последующему развитию половых органов. В дальнейшем они определяют половое созревание и развитие разнообразных вторичных половых признаков. Половые гормоны регулируют процессы, связанные с синтезом желтка в ооцитах и овуляцией, а у млекопитающих индуцируют изменения в эндометрии матки, предшествующие имплантации яйцеклетки и обеспечивающие нормальное протекание беременности (прогестерон). Совместно с другими гормонами половые стероиды вызывают изменения молочных желез, необходимые для секреции молока.
Они обладают также рядом эффектов вне половой сферы, так называемых экстрагенитальных. Половые гормоны оказывают значительное влияние на ЦНС и
половое поведение; они являются важным звеном в механизме саморегуляции гипоталамо- гипофизарно-гонадной системы. Органами-мишенями стероидных гормонов являются клетки семенных канальцев, простата, семенные пузырьки, матка, печень, гипоталамус и др. В крови половые гормоны находятся в основном в связанном со специфическими белками состоянии.
Половая дифференцировка у эмбриона. На ранних этапах эмбриогенеза млекопитающих (у человека в конце 3-го месяца) мужские гонады приобретают гормональную активность и начинают синтезировать андрогены (тестостерон). Образующиеся андрогены обеспечивают половую дифференцировку гипоталамуса и формирование органов половой системы, характерных для мужского пола. В опытах на крысах показано, что если на ранних этапах эмбриогенеза блокировать секрецию тестостерона, у плода-самца развиваются гениталии самки. Если на этих стадиях развития плоду-самке ввести тестостерон, происходит частичное развитие гениталий самца. Путем воздействия половыми стероидами на развивающихся эмбрионов ряда рыб получают фенотипических самок из генотипических самцов и наоборот. В результате соответствующих воздействий формируются популяции, состоящие только из самок или из стерильных особей. У эмбрионов женского пола в период внутриутробного развития яичники не обладают гормональной активностью. Выработка половых стероидов начинается в связи с половым созреванием.
Половое созревание. Половые стероиды оказывают значительное влияние на развитие и созревание половых клеток. Эстрогены стимулируют синтез белка вителлогенина в
печени, который включается в ооцит и образует желток, необходимый для роста и развития эмбриона. В опытах на лягушках, в ооцитах которых еще не началось накопление желтка, показано, что введение эстрадиола уже через 12—24 ч приводило к синтезу вителлогенина.
Половыми стероидами контролируется развитие весьма разнообразных вторичных половых признаков, обеспечивающих процесс размножения. Так, брачный наряд рыб и других животных, развитие рогов и других образований определяются половыми стероидами. После удаления яичников или семенников, являющихся источниками половых гормонов у различных животных (от рыб до млекопитающих), наблюдается обратное развитие вторичных половых признаков самцов (и наоборот). Эти эффекты были четко показаны на птицах в опытах М. М. Завадовского (рис. 6.10).
