
- •2. Ускорение при плоском криволинейном движении. Нормальное и тангенсальное ускорения.
- •3. Кинематика вращения твёрдого тела вокруг закреплённой оси. Угол поворота. Угловая скорость. Угловое ускорение. Связь между линейной и угловой скоростью. Равноускоренное движение.
- •4. Законы Ньютона. Принцип относительности Галилея.
- •5. Упругие силы. Силы трения.
- •6. Закон всемирного тяготения. Сила тяжести. Вес тела. Состояние невесомости.
- •7. Импульс. Импульс силы. Закон сохранения импульса. Центр масс.
- •8. Механическая работа. Мощность. Энергия. Кинетическая энергия.
- •9. Поле сил. Консервативные силы. Потенциальная энергия. Связь между потенциальной энергией и силой.
- •10. Закон сохранения полной механической энергии частицы.
- •11. Закон сохранения энергии для системы невзаимодействующих частиц.
- •12. Взаимная потенциальная энергия частиц. Закон сохранения энергии системы частиц.
- •13. Энергия упругой деформации. Условия равновесия механической системы.
- •14. Момент импульса. Момент силы. Потенциальная энергия. Связь между потенциальной энергией и силой.
- •15. Вращение твёрдого тела вокруг закреплённой оси. Основное уравнение динамики вращательного движения твёрдого тела.
- •16. Момент инерции. Вычисление моментов инерции ноторых тел относительно оси симметрии (тонкий стержень, обруч, диск). Теорема Штейнера.
- •17. Момент инерции однородного тела вращения. Моменты инерции конуса, шара.
- •18. Кинетическая энергия вращающегося твёрдого тела вокруг закреплённой оси. Кинетическая энергия твёрдого тела при плоском движении.
- •19. Уравнения динамики твёрдого тела. Центр тяжести. Условия равновесия твёрдого тела.
- •20. Колебательное движение. Кинематика и динамика гармонических колебаний.
- •21. Кинетическая и потенциальная энергия гармонического колебания. Полная энергия гармонического колебания. Средние за период значения кинетической и потенциальной энергии.
- •22. Математический и физический маятники. Приведённая длина физического маятника. Центр качаний.
- •23. Сложение гармонических колебаний одного направления. Сложение взаимно перпендикулярных колебаний.
- •24. Затухающие колебания. Логарифмический декремент затухания. Добротность колебательной системы.
- •25. Вынужденные колебания. Явление резонанса. Резонансные кривые.
- •26. Основные понятия и исходные положения положения термодинамики. Обратимые и необратимые процессы. Круговые процессы (циклы).
- •27. Внутренняя энергия. Работа и теплота. Первое начало термодинамики.
- •28. Теплоёмкость. Молярная и удельная теплоёмкости. Связь между ними. Формула Майера.
- •29. Уравнение состояния идеального газа. Изотермический, изохорический и изобарический процессы и их уравнения. Графики этих процессов.
- •30. Адиабатический процесс. Уравнение Пуассона. Показатель адиабаты.
- •31. Политропические процессы. Уравнение политропы идеального газа. Показатель политропы.
- •32. Тепловые двигатели. К.П.Д. Теплового двигателя. Холодильный коэффицент. Различные формулировки второго начала термодинамики.
- •33. Цикл Карно. Первая теорема Карно. Вторая теорема Карно.
- •34. Рабочий цикл четырёхтактного двигателя внутреннего сгорания. К.П.Д. Цикла.
- •35. Рабочий цикл четырёхтактного двигателя внутреннего сгорания Дизеля. К.П.Д. Цикла.
- •36. Неравенство Клаузиуса. Равенство Клаузиуса. Энтропия. Изэнтропический процесс. Теорема Нернста(третье начало термодинамики).
- •37. Закон возрастания энтропии. Основное уравнение термодинамики.
- •38. Число степеней свободы механической системы. Поступательные, вращательные и колебательные степени свободы молекулы. Теорема о равнораспределении энергии по степеням свободы.
- •39. Классическая теория теплоёмкости идеальных газов.
- •40. Классическая теория теплоёмкости твёрдых тел (кристаллов). Закон Дюлонга и Пти.
- •41. Пространство скоростей. Функция распределения молекул по скоростям. Распределение Максвелла.
- •42. Распределение молекул по абсолютным значениям скоростей. Характерные скорости (наиболее вероятная, средняя, среднеквадратичная) в распределении Максвелла.
- •43. Барометрическая формула. Распределение Больцмана. Распределение Максвелла - Больцмана.
- •44. Энтропия и вероятность. Формула Больцмана. Макро- и микросостояния. Термодинамическая вероятность макросостояния (статистический вес).
35. Рабочий цикл четырёхтактного двигателя внутреннего сгорания Дизеля. К.П.Д. Цикла.
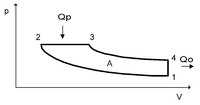
Цикл Дизеля — термодинамический цикл, описывающий рабочий процесс двигателя внутреннего сгорания с воспламенением впрыскиваемого топлива от разогретого рабочего тела, цикл дизельного двигателя. Идеальный цикл Дизеля состоит из четырёх процессов:
![]()
p-V диаграмма цикла Дизеля
1—2 адиабатное сжатие рабочего тела;
2—3 изобарный подвод теплоты к рабочему телу;
3—4 адиабатное расширение рабочего тела;
4—1 изохорное охлаждение рабочего тела.
КПД
цикла Дизеля
![]() ,где
,где![]() —
степень сжатия,
—
степень сжатия,
![]() —
коэффициент предварительного расширения,k—
показатель адиабаты.
—
коэффициент предварительного расширения,k—
показатель адиабаты.
Идеальный цикл лишь приблизительно описывает процессы, происходящие в реальном двигателе, но для технических расчётов в большинстве случаев точность такого приближения удовлетворительна.
36. Неравенство Клаузиуса. Равенство Клаузиуса. Энтропия. Изэнтропический процесс. Теорема Нернста(третье начало термодинамики).
Энтропия изолированной системы не может убывать. dS≥0 (Неравенство Клаузиуса)
В
случае, если термодинамический цикл
состоит только из обратимых процессов,
неравенство переходит в Равенство
Клаузиуса:
![]()
Энтропия системы — функция её состояния, определённая с точностью до произвольной постоянной, разность которых в двух равновесных состояниях 1 и 2 по определению равна приведённому количеству теплоты, которое надо сообщить системе, чтобы перевести её из состояния 1 в состояние 2 по любому квазистатическому пути.
![]()
Закон возрастания энтропии. Энтропия адиабатически изолированной системы либо возрастает, либо остаётся постоянной.
Термин широко применяется и в других областях знания: в статистической физике — как мера вероятности осуществления какого-либо макроскопического состояния
Изоэнтропийный процесс - тепловой процесс, происходящий при постоянной энтропии.
Условия,
при которых тепловой процесс будет
изоэнтропийным, можно получить из
равенства Клаузиуса для обратимых
процессов:
![]() ,
,
где dS - приращение (дифференциал) энтропии, а δQ - бесконечно малое полученное количество теплоты. Отсюда следует, что из обратимых процессов изоэнтропийным является только обратимый адиабатный процесс.
Из
неравенства Клаузиуса для необратимых
процессов
![]() ,
,
следует, что необратимый адиабатный процесс не может быть изоэнтропийным.
Но вообще и при необратимом процессе энтропия системы может сохранять постоянное значение, если вся производимая энтропия сразу удаляется с помощью теплообмена.
Линию на любой термодинамической диаграмме, изображающую изоэнтропийный процесс, можно называть изоэнтропой. Но обычно её называют адиабатой, так как необратимый процесс (в том числее необратимый адиабатный) нельзя корректно изобразить линией на диаграмме.
Третье начало термодинамики (теорема Нернста) — физический принцип, определяющий поведение энтропии при абсолютном нуле температуры. Является одним из постулатов термодинамики.
«Приращение энтропии при абсолютном нуле температуры стремится к конечному пределу, не зависящему от того, в каком равновесном состоянии находится система».
![]() или
или
![]()
где x — любой термодинамический параметр.
третье начало термодинамики относится только к равновесным состояниям.
П![]() оскольку
на основе второго начала термодинамики
энтропию можно определить только с
точностью до произвольной аддитивной
постоянной (то есть, определяется не
сама энтропия, а только её изменение):
третье начало термодинамики может быть
использовано для точного определения
энтропии. При этом энтропию равновесной
системы приабсолютном
нуле температуры
считают равной нулю.
оскольку
на основе второго начала термодинамики
энтропию можно определить только с
точностью до произвольной аддитивной
постоянной (то есть, определяется не
сама энтропия, а только её изменение):
третье начало термодинамики может быть
использовано для точного определения
энтропии. При этом энтропию равновесной
системы приабсолютном
нуле температуры
считают равной нулю.
