
- •1 Параметры состояния рабочего тела
- •Примеры
- •2 Законы и уравнения состояния идеальных газов
- •Примеры
- •3 Газовые смеси
- •Примеры
- •4 Теплоемкость газов
- •Примеры
- •5 Первый закон термодинамики
- •Примеры
- •6 Процессы изменения состояния идеальных газов
- •Примеры
- •7 Второй закон термодинамики
- •Примеры
- •8 Водяной пар
- •Примеры
- •9 Истечение и дросселирование газов и паров
- •Примеры
- •10 Циклы двигателей внутреннего сгорания
- •Примеры
- •11 Циклы паросиловых установок
- •Примеры
- •12 Циклы холодильных установок
- •Примеры
- •13 Компрессоры
- •Примеры
- •14 Влажный воздух
- •Примеры
Примеры
П-5.1
При испытании двигателей для определения мощности необходимо их тормозить (рис. 3). При этом работа, произведенная двигателем, расходуется на преодоление сил трения и превращается в теплоту, часть которой (примерно 20%) рассеивается в окружающей среде, а остальная часть отводится охлаждающей тормоз водой.
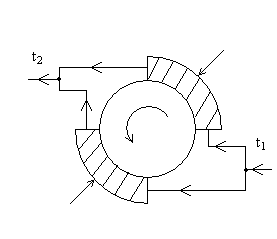
Рис. 3
Сколько
воды необходимо подводить к тормозу за
1 ч, если крутящий момент на валу Мкр=2000
Дж, частота
вращения
n=1500
об/мин, а допустимое повышение температуры
воды
![]() К. Теплоемкость
воды ср
принять равной 4,1868 кДж/(кг·К).
К. Теплоемкость
воды ср
принять равной 4,1868 кДж/(кг·К).
Решение.
Мощность двигателя целиком переходит в теплоту трения, выделяемую в единицу времени, а 80 % этой теплоты поглощается водой. Поэтому энергетический баланс можно записать так:
0,80N = mв cр t,
где mв- расход воды, кг/с;
cр – теплоемкость воды, кДж/(кг·К);
N
= 2![]() -
мощность
двигателя, Вт.
-
мощность
двигателя, Вт.
Тогда,
![]() =1,714
кг/с=6170 кг/ч.
=1,714
кг/с=6170 кг/ч.
П-5.2
Найти изменение внутренней энергии 1 кг воздуха при переходе его от начального состояния t1 = 300 ºС до конечного при t2 = 50 ºС. Зависимость теплоемкости от температуры принять линейной. Ответ дать в кДж.
Решение.
Изменение внутренней энергии найдем по формуле:
u=cvm(t2-t1).
Пользуясь приложением К, получим для воздуха
![]() кДж/(кг·К);
кДж/(кг·К);
![]() кДж/(кг·К).
кДж/(кг·К).
Следовательно,
u = 0,7411(50-300)= -185,3 кДж/кг.
Задачи
З-5.1
Производится испытание двигателя, во время которого двигатель вместо того, чтобы принимать полезную нагрузку, тормозится.
На сколько градусов нагреется охлаждающая тормоз вода, если крутящий момент двигателя равен 5 кДж, а частота вращения – 1500 об/мин. Известно, что к колодкам тормоза подводится 10 т/ч воды при температуре 15 ºС. Предполагается, что вся работа двигателя превращается в теплоту трения.
Ответ: на 67,6 К.
З-5.2
Свинцовый шар падает с высоты 80 м на твердую поверхность. При этом кинетическая энергия шара переходит в теплоту, 80 % которой им усваивается.
На сколько градусов нагревается при падении шар?
Теплоемкость свинца ср = 0,1256 кДж/(кг·К)
Ответ: на 5 К.
З-5.3
В сосуд, содержащий 5 л воды при температуре 20 ºС, помещен электронагреватель мощностью 800 Вт.
Определить, сколько времени потребуется, чтобы вода нагревалась до температуры кипения 100 ºС. Потерями теплоты сосуда в окружающую среду пренебречь.
Ответ:
![]() =
30 мин.
=
30 мин.
З-5.4
Автомобиль массой 1,5 т останавливается под действием тормозов при скорости 40 км/ч.
Вычислить конечную температуру тормозов t2, если их масса равна 15 кг, начальная температура t1=10 С, а теплоемкость стали, из которой изготовлены тормозные части, равна 0,46 кДж/(кг·К). Потерями теплоты в окружающую среду пренебречь.
Ответ: t2=23,4 ºС.
З-5.5
Найти изменение внутренней энергии 2 м3 воздуха, если температура его понижается от t1 = 250 ºС до t2 = 70 ºС. Зависимость теплоемкости от температуры принять линейной. Начальное давление воздуха p1 = 0,6 МПа.
Ответ: U = -1063кДж.
6 Процессы изменения состояния идеальных газов
Основными термодинамическими процессами являются:
Изохорный процесс – процесс сообщения или отнятия теплоты при постоянном объеме газа (v=const). Зависимость между начальными и конечными параметрами процесса
![]() . (6.1)
. (6.1)
Изменение внутренней энергии
![]() . (6.2)
. (6.2)
Если в процессе участвует М кг или Vн м3 газа, то количество теплоты или изменение внутренней энергии газа
![]() . (6.3)
. (6.3)
Совершаемая в процессе работа
l=0, L=0. (6.4)
Изменение энтропии
![]() . (6.5)
. (6.5)
Изобарный процесс - процесс сообщения или отнятия теплоты при постоянном давлении газа (р=const). Зависимость между начальными и конечными параметрами процесса
![]() . (6.6)
. (6.6)
Изменение внутренней энергии
![]() . (6.7)
. (6.7)
Работа 1 кг газа
![]() . (6.8)
. (6.8)
Для М кг газа
![]() . (6.9)
. (6.9)
Если в процессе участвует М кг или Vн м3 газа, то количество теплоты
![]() . (6.10)
. (6.10)
Изменение энтропии
![]() . (6.11)
. (6.11)
Изотермический процесс - процесс сообщения или отнятия теплоты при постоянной температуре газа (t=const). Зависимость между начальными и конечными параметрами процесса
![]() . (6.12)
. (6.12)
Изменение внутренней энергии
![]() . (6.13)
. (6.13)
Работа 1 кг газа
![]() . (6.14)
. (6.14)
Если в процессе участвует М кг газа, то полученные значения следует увеличить в М раз, также можно удельный объем v заменить на полный объем V
![]() . (6.15)
. (6.15)
Количество теплоты, сообщаемое газу или отнимаемое от него
qt=l. (6.16)
Теплота для М кг газа
Qt=L. (6.17)
Изменение энтропии
![]() . (6.18)
. (6.18)
Адиабатный процесс – процесс без сообщения или отнятия теплоты (dq=0, s = const). Уравнение адиабаты pvk=const при (cv=const), где k – показатель адиабаты (см. формулу (4.2) и таблицу 3).
Зависимость между начальными и конечными параметрами процесса
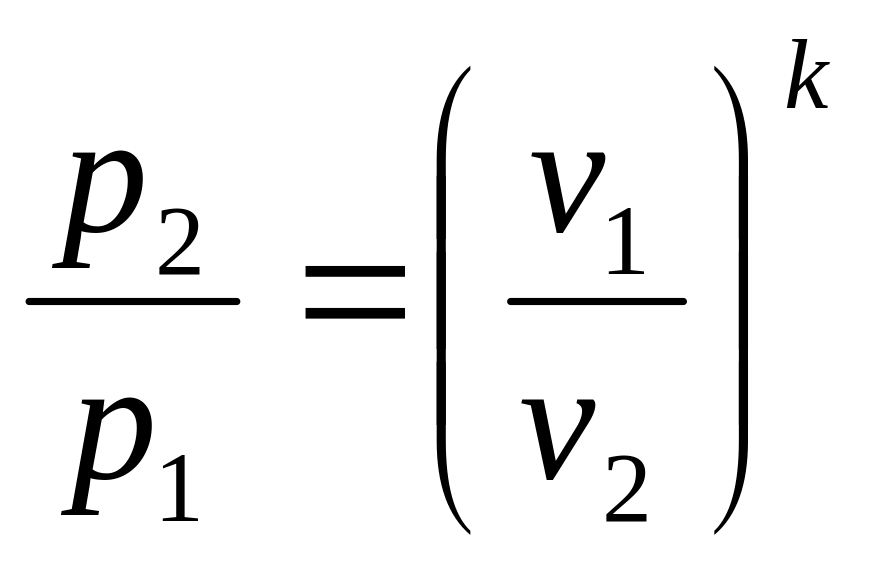 ,
,
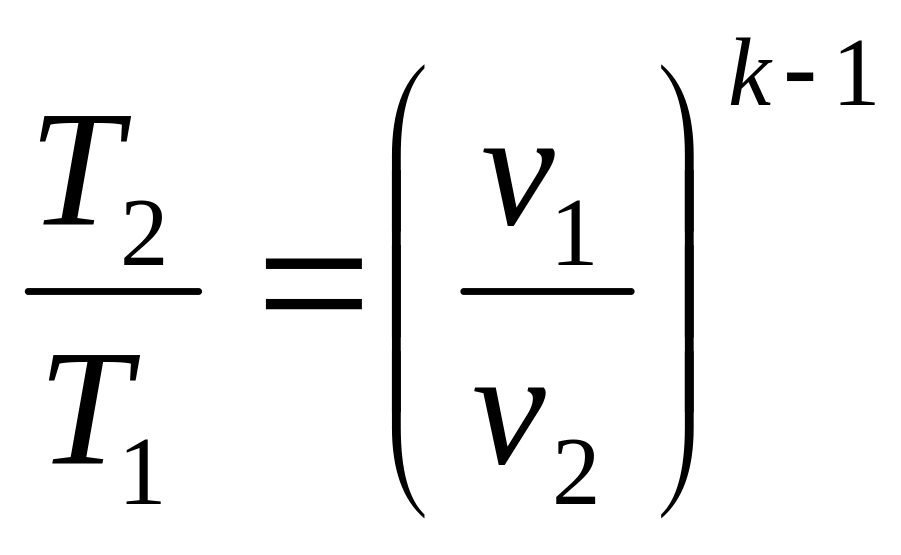 ,
,
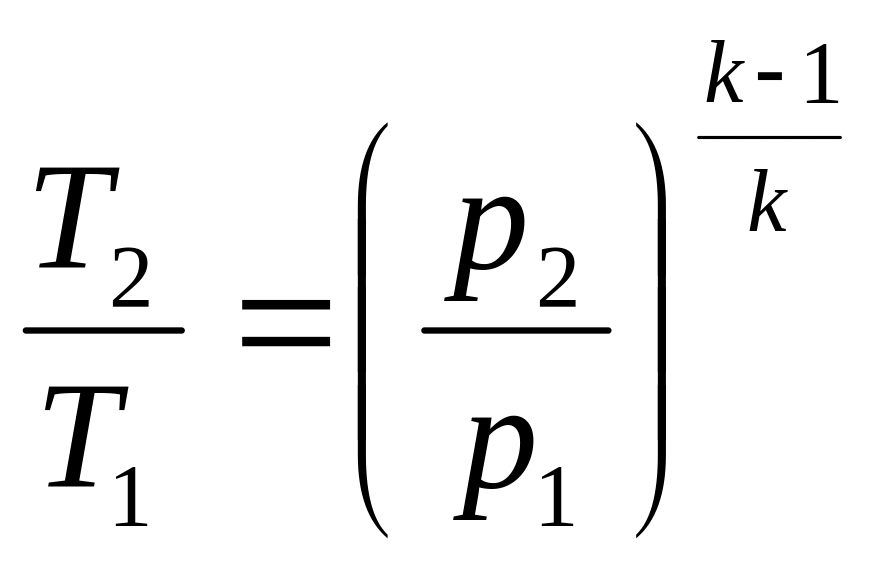 . (6.19)
. (6.19)
Изменение внутренней энергии
![]() . (6.20)
. (6.20)
Уравнение первого закона термодинамики для адиабатного процесса имеет вид
0=du+dl, (6.21)
следовательно
du= - dl, или Δu= - l. (6.22)
Изменение внутренней энергии газа и работа адиабатного процесса равны по величине и противоположны по знаку.
Работа 1 кг газа
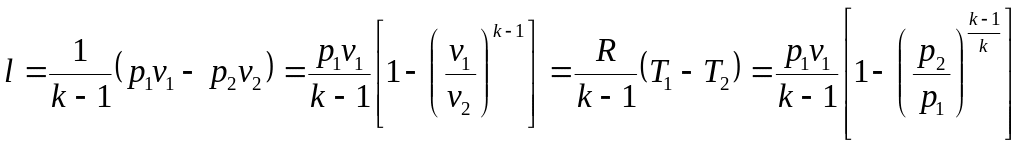 . (6.23)
. (6.23)
Для М кг газа
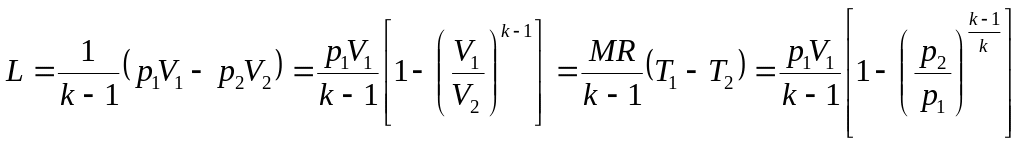 . (6.24)
. (6.24)
Количество теплоты, сообщаемое газу или отнимаемое от него
q=0. (6.25)
Изменение энтропии
Δs = 0. (6.26)
Политропный процесс – процесс, при котором изменение параметров подчиняется уравнению pvn=const, где n – показатель политропы, величина постоянная для данного процесса. Характеристикой политропного процесса является величина φ – коэффициент разветвления теплоты, т.е. доля теплоты, затрачиваемая на изменение внутренней энергии рабочего тела.
![]() . (6.27)
. (6.27)
Показатель политропы определяется из уравнения
![]() . (6.28)
. (6.28)
Если известны значения двух параметров в начальном и конечном состоянии
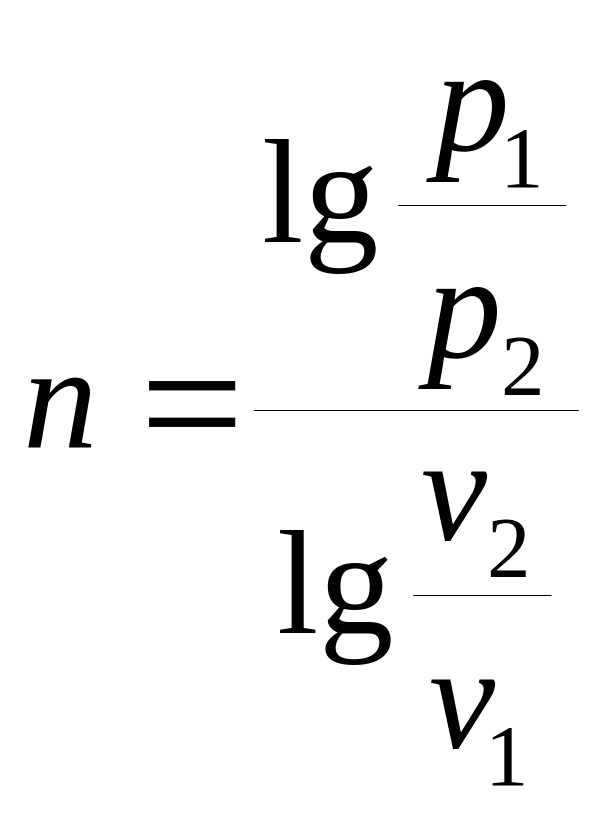 ,
,
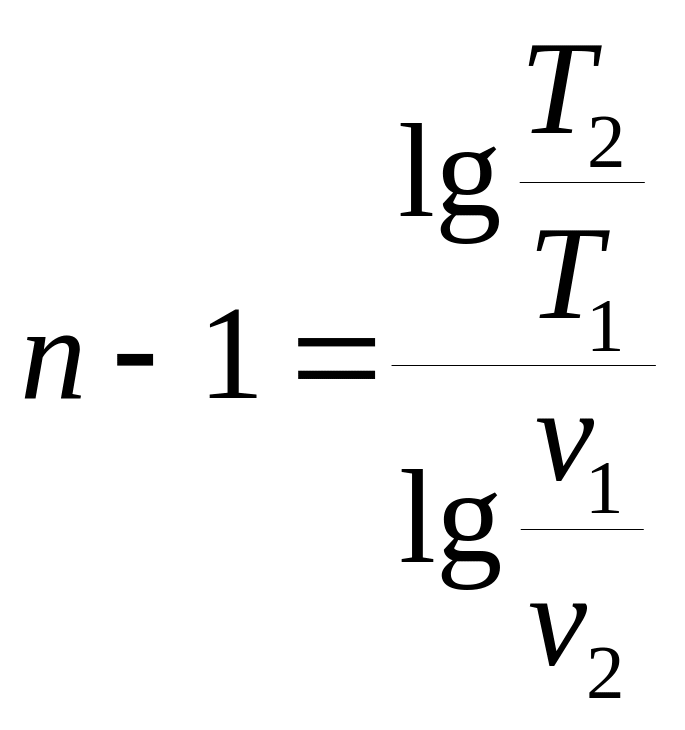 ,
,
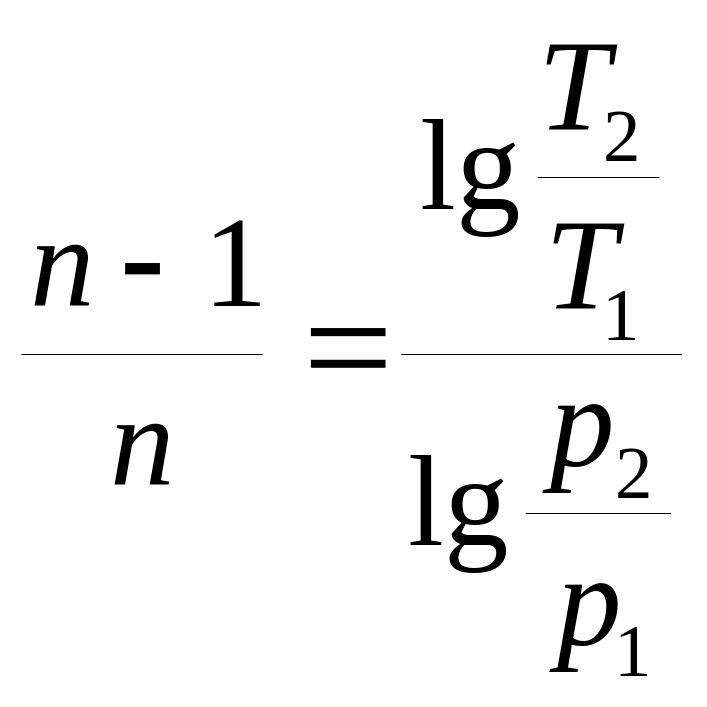 . (6.29)
. (6.29)
Для процессов расширения:
а) n<1 – теплота подводится (q>0), внутренняя энергия газа увеличивается (Δu>0);
б) k>n>1 – теплота подводится (q>0), внутренняя энергия газа уменьшается (Δu<0);
в) n> k – теплота отводится (q<0), внутренняя энергия газа уменьшается (Δu<0).
Для процессов сжатия
а) n<1 – теплота отводится (q<0), внутренняя энергия газа уменьшается (Δu<0);
б) k>n>1 – теплота отводится (q<0), внутренняя энергия газа увеличивается (Δu>0);
в) n> k – теплота подводится (q>0), внутренняя энергия газа увеличивается (Δu>0).
Зависимость между начальными и конечными параметрами процесса
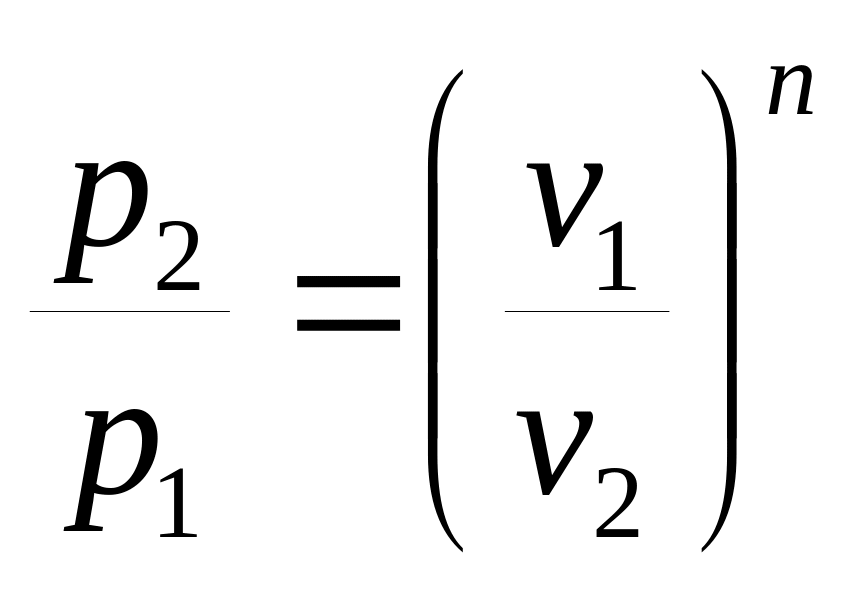 ,
,
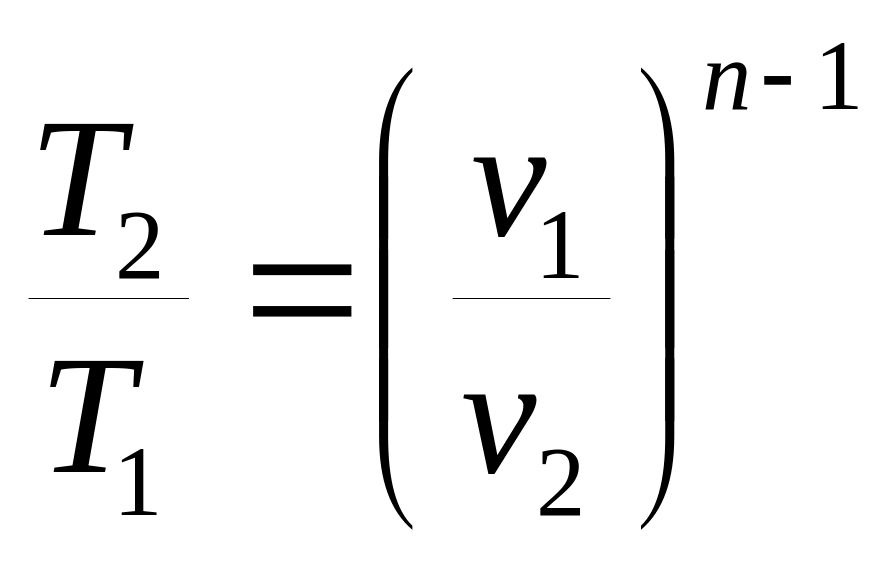 ,
,
 . (6.30)
. (6.30)
Изменение внутренней энергии
![]() . (6.31)
. (6.31)
Работа 1 кг газа
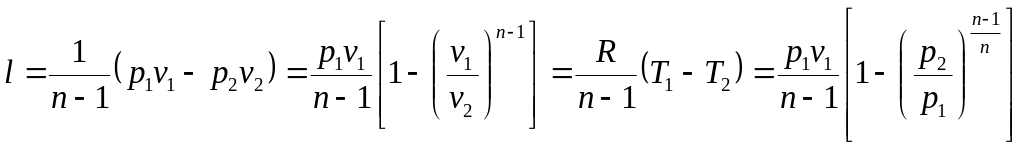 . (6.32)
. (6.32)
Если количество теплоты, участвующее в процессе известно
![]() . (6.33)
. (6.33)
Для М кг газа
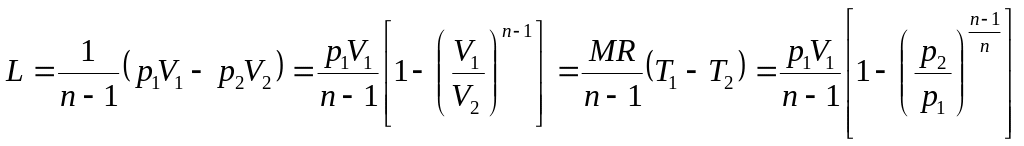 . (6.34)
. (6.34)
Если количество теплоты, участвующее в процессе известно
![]() . (6.35)
. (6.35)
Теплоемкость политропного процесса
![]() . (6.36)
. (6.36)
Количество теплоты, сообщаемой газу или отнимаемой от него
![]() ; (6.37)
; (6.37)
![]() . (6.38)
. (6.38)
Изменение энтропии
![]() . (6.39)
. (6.39)
