
- •Содержание
- •1. Тепловые эффекты
- •Примеры решения задач
- •Задачи и упражнения для самостоятельной работы
- •2. Тепловые свойства. Зависимость теплового
- •Примеры решения задач
- •Задачи и упражнения для самостоятельной работы
- •3. Энергия Гиббса – критерий термодинамической
- •Примеры решения задач
- •Задачи и упражнения для самостоятельной работы
- •4. Константа равновесия
- •Примеры решения задач
- •Задачи и упражнения
- •5. Основы химической кинетики и катализа
- •Задачи и упражнения для самостоятельной работы
- •6. Прочность связей в молекулах углеводородов
- •Задачи и упражнения для самостоятельной работы
- •7. Реакции радикалов при термическом
- •Задачи и упражнения для самостоятельной работы
- •8. Химизм и механизм термических превращений
- •Задачи и упражнения для самостоятельной работы
- •9. Соотношение скоростей реакций радикалов
- •Задачи и упражнения для самостоятельной работы
- •10. Процессы переработки нефтяного сырья, протекающие
- •Задачи и упражнения для самостоятельной работы
Примеры решения задач
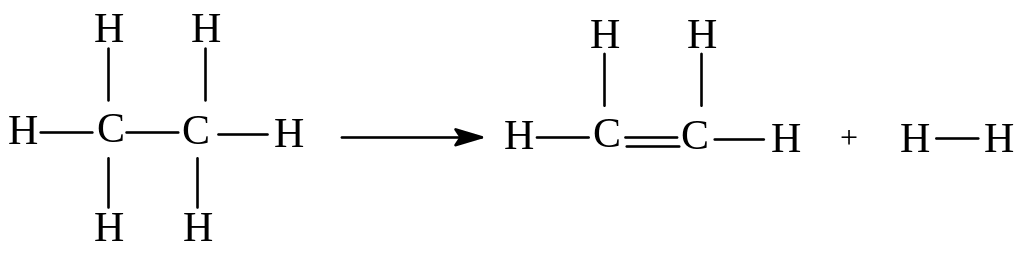
Задача 1. Определить тепловой эффект реакции
C2H6 ↔ C2H4 + Н2 + Qр
в стандартных условиях разными методами, если известны:
|
Теплота образования, кДж/моль |
Теплота сгорания, кДж/моль |
Энергия связи, кДж/моль |
Н2 C2H4 C2H6 |
0 -52,36 +84,79 |
+286,25 +1413,01 +1562,11 |
С−С 258,02 С=С 419,00 С−Н 365,69 Н−Н 433,25 |
Решение:
1)
![]()
2
3)![]()
![]()
Задача 2. В процессе каталитического риформинга при температуре 800К из метилциклогексана образовалось 920 кг толуола, причем 80% его образовалось по реакции:
ц-С6Н11СН3 ↔ С6Н5СН3 + ЗН2 (1)
а 20% - по реакции:
н-С7Н16 ↔ С6Н5СН3 + 4Н2 (2)
Найдите тепловой эффект этого процесса, если при температуре 800 оК:
∆Нц-гексан = -182,09 кДж/моль
∆Нтолуол = +33,23 кДж/моль
∆Нн-гептан = -217,13 кДж/моль
Решение:
Q=NiQ(l) + NiQ(2),
где: Ni – число молей образовавшихся по реакции веществ.
По реакции (1) образовалось (920/92)∙0,8 = 8 кмоль толуола;
По реакции (2) образовалось (920/92)∙0,2 = 2 кмоль толуола.
Q = 8 (33,23+182,09) + 2∙(33,23+217,13) = 2223280 Дж
Задача 3. Определите количество тепла, выделяющегося при гидрировании 1000 кг ацетилена, в стандартных условиях, если конечная смесь содержит 80% этилена, 2% этана и 18% ацетилена (% масс.).
Решение:
Из справочных данных (см.приложение, табл.1) находим теплоты образования веществ, участвующих в химической реакции:
Ацетилен - 227,073 кДж/моль
Этилен - 52,358 кДж/моль
Этан - -88,881 кДж/моль
Водород - 0 кДж/моль
В процессе гидрирования протекает две реакции:
СН≡СН + Н2 ↔ СН2=СН2 (1)
СН≡СН + 2Н2 ↔ СН3−СН3 (2)
На 100 кг конечной смеси расходуется ацетилена по реакции (1):
СН≡СН + Н2 ↔ СН2=СН2
26 2 28
2 6
- 28
6
- 28
х 1
- 80
1
- 80
![]()
по реакции (2):
СН≡СН + 2Н2 ↔ СН3−СН3
26 4 30
2 6 - 30
х
2
- 2
![]()
Остается непрореагировавшего ацетилена: 18%, т.е. 18 кг.
Всего на 100 кг конечной смеси: 74,28 + 1,73 + 18 = 94,01 кг ацетилена.
По условию задачи было взято для гидрирования 1000 кг С2Н2, следовательно, образуется конечной смеси:
9 4,01 - 100
1
000
- х3
![]() ,
,
в том числе: этилена - 1063,8∙0,8 = 851,04 кг
этана - 1063,8∙0,02 = 21,28 кг
ацетилена - 1063,8∙0,18 = 191,48 кг
Тепловой эффект реакции (1): Q1 = 52,358 - 227,073 = -174,71 кДж/моль.
Тепловой эффект реакции (2): Q2 = -88,881 - 227,073 = -315,95 кДж/моль.
Тогда, общий тепловой эффект процесса гидрирования ацетилена равен:
Qоб. = Q1∙851,04/28 + Q2∙21,28/30 = - 5,5∙103 кДж/моль.
