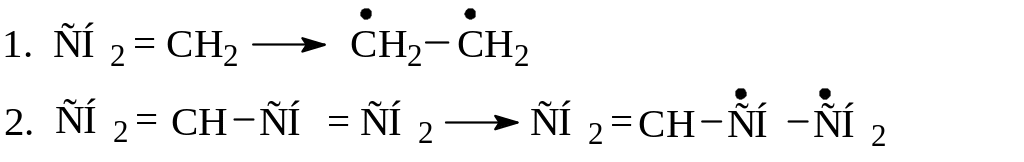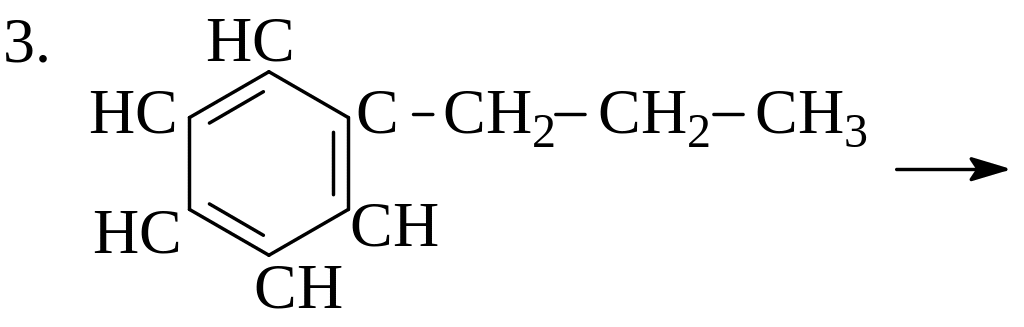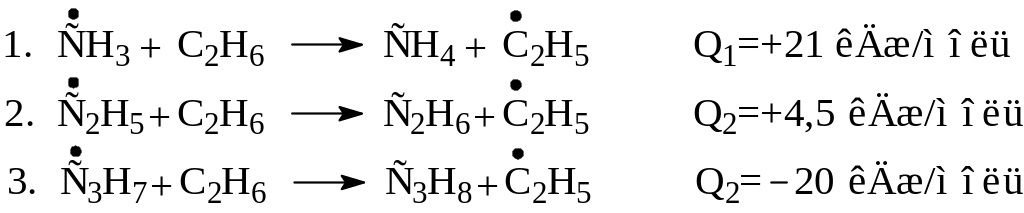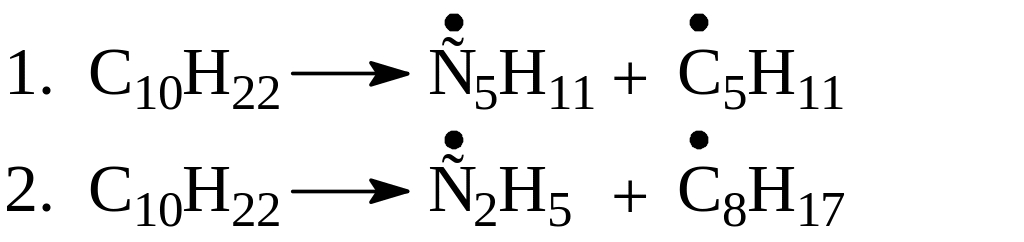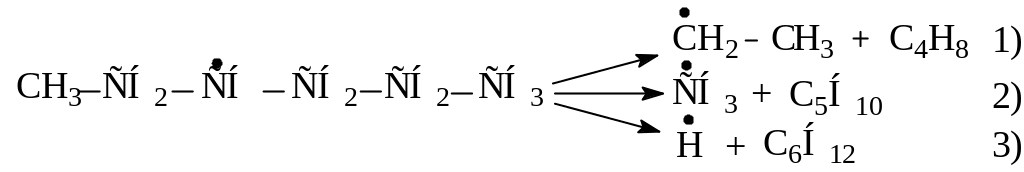- •Содержание
- •1. Тепловые эффекты
- •Примеры решения задач
- •Задачи и упражнения для самостоятельной работы
- •2. Тепловые свойства. Зависимость теплового
- •Примеры решения задач
- •Задачи и упражнения для самостоятельной работы
- •3. Энергия Гиббса – критерий термодинамической
- •Примеры решения задач
- •Задачи и упражнения для самостоятельной работы
- •4. Константа равновесия
- •Примеры решения задач
- •Задачи и упражнения
- •5. Основы химической кинетики и катализа
- •Задачи и упражнения для самостоятельной работы
- •6. Прочность связей в молекулах углеводородов
- •Задачи и упражнения для самостоятельной работы
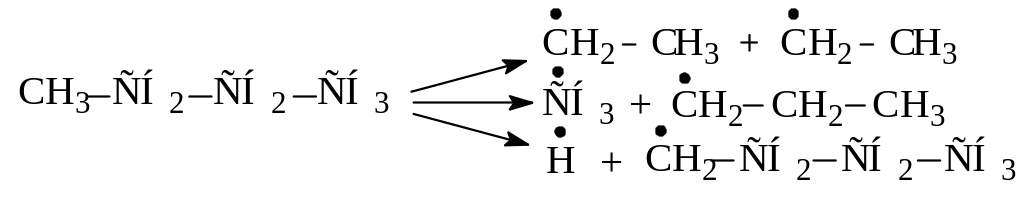
- •7. Реакции радикалов при термическом
- •Задачи и упражнения для самостоятельной работы
- •8. Химизм и механизм термических превращений
- •Задачи и упражнения для самостоятельной работы
- •9. Соотношение скоростей реакций радикалов
- •Задачи и упражнения для самостоятельной работы
- •10. Процессы переработки нефтяного сырья, протекающие
- •Задачи и упражнения для самостоятельной работы
Задачи и упражнения для самостоятельной работы
№ п/п Задачи |
Условие задачи |
1. |
Рассчитайте, во сколько раз быстрее протекает распад этана по связи С–С по сравнению с распадом его по связи С–Н при температуре 627оС. (Энергии разрыва связей см.в Прилож.5). |
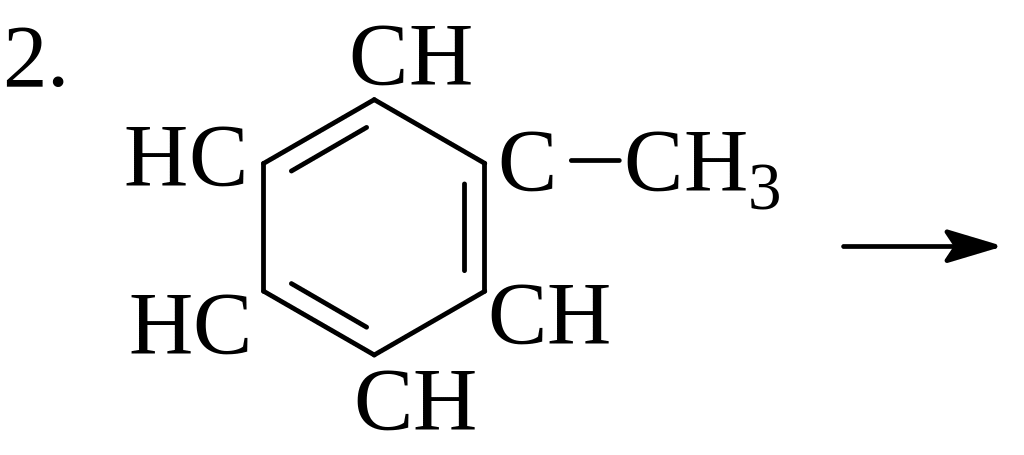
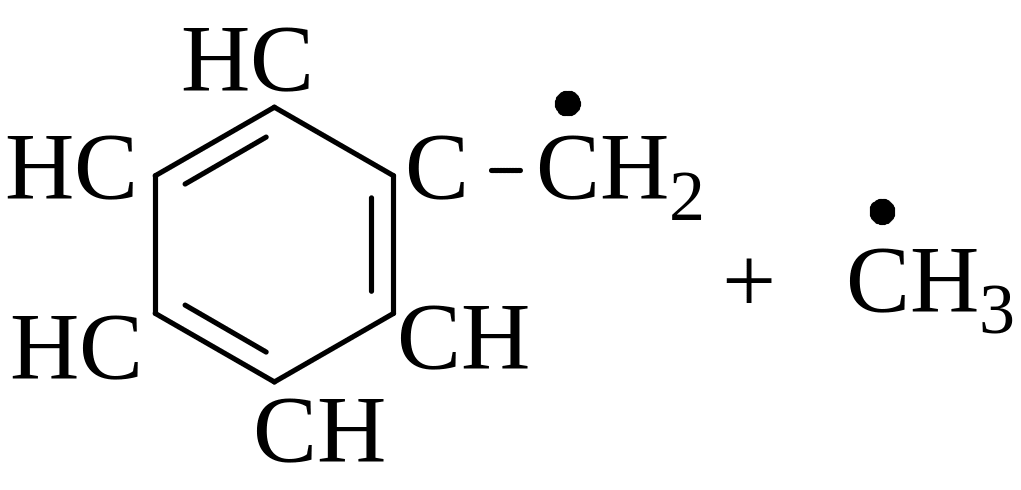
2. |
Какая из реакций пойдет быстрее при температуре 550оС, и во сколько раз?
Энергии разрыва связей см.в Прилож.5 |
3. |
Рассчитайте, во сколько раз быстрее протекает распад н-декана по реакции (1), по сравнению с распадом по реакции (2) при температуре 523оС:
|
4. |
Энергия разрыва π-связи в алкене равна 249 кДж/моль, а в алкадиене – 192 кДж/моль. Рассчитайте, какая из реакций пойдет с большей скоростью при температуре 1000оС, и во сколько раз?
|
5. |
Рассчитайте константы скорости реакций при температуре 550оС и сделайте соответствующие выводы о термической устойчивости исходных молекул углеводородов:
|
№ п/п Задачи |
Условие задачи |
6. |
Рассчитайте величину энергии активации и соотношение скоростей реакций:
|
7. |
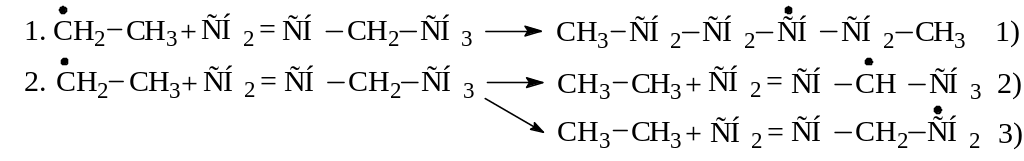
Найдите соотношение скоростей реакций распада:
при температуре 527оС, если энергии активации этих реакций соответственно равны: Е1 = 310 кДж/моль; Е2 = 335 кДж/моль |
8. |
Найдите значения энергий активации и соотношение скоростей реакций распада радикала:
при температуре 700оС, если тепловые эффекты этих реакций соответственно равны: Q1 = + 126 кДж/моль; Q2 = + 138 кДж/моль; Q3 = + 188 кДж/моль |
9. |
Найдите значения энергий активации и соотношение скоростей экзотермических реакций замещения и присоединения радикалов:
при температуре 427оС, если тепловые эффекты этих реакций соответственно равны: Q1 = + 75 кДж/моль; Q2 = + 71 кДж/моль; Q3 = + 13 кДж/моль |
10. Процессы переработки нефтяного сырья, протекающие
в присутствии катализаторов кислотного характера
Катализ жидкими и твердыми кислотами широко распространен в нефтепереработке и нефтехимии. Каталитическое действие кислот обусловлено образованием при их взаимодействии с углеводородами положительно заряженных ионов, называемых карбкатионами или карбоний-ионами. Карбкатионы обладают высокой химической активностью и реагируют как мономолекулярно, так и с молекулами углеводородов с очень большой скоростью.
Образование карбкатионов
Протонные кислоты (кислоты Бренстеда) отдают протон молекуле ненасыщенного углерода:
![]() (10.1)
(10.1)
Апротонные кислоты (кислоты Льюиса) при взаимодействии с протонодонорными веществами часто образуют сильные протонные кислоты:
![]() (10.2)
(10.2)
Углеводороды являются слабыми основаниями, основность которых изменяется в очень широких пределах. Наибольшей основностью характеризуются алкены, меньшей - арены, причем полициклические арены являются значительно более сильными основаниями, чем моноциклические. У бензола с ростом замещения кольца основность метилбензолов резко возрастает.
Свойства карбкатионов
Карбкатионы - высокоактивные частицы, по некоторым свойствам сходные с радикалами. Карбкатионы, как и радикалы подвергаются мономолекулярному распаду и бимолекулярным реакциям присоединения и замещения. Существенное различие в химических свойствах карбкатионов и радикалов − способность первых изомеризоваться.
Изомеризация карбкатионов
Изомеризация может происходить в результате переноса гидрид иона:
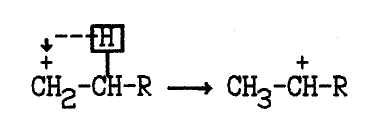
т.е. происходит 1,2-изомеризация.
Перенос метил-аниона приводит к изомеризации углеродного скелета молекулы алкана:
----------------
+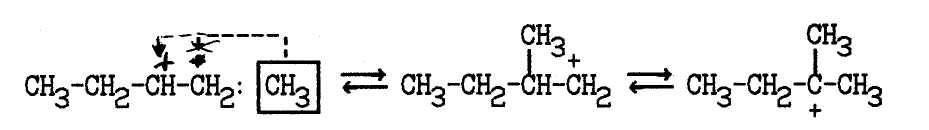


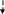
Изомеризация первичного катиона во вторичный экзотермична, вторичного в третичный также экзотермична. Структура третичного карбкатиона наиболее устойчива. Изомеризация углеродной цепи в результате переноса метил-аниона связана с переходом вторичного карбкатиона в первичный, и поэтому эндотермична, в связи с чем изомеризация углеродного скелета происходит медленнее, чем изомеризация с переносом гидрид-иона.
Распад карбкатионов
Распад протекает по β-связи относительно заряженного атома углерода. Распад первичных карбкатионов с неразветвленной цепью идет тем легче, чем большее число атомов углерода содержит образующийся карбкатион.
Труднее всего происходит отщепление метильного иона:
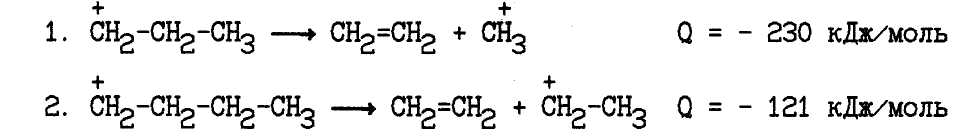
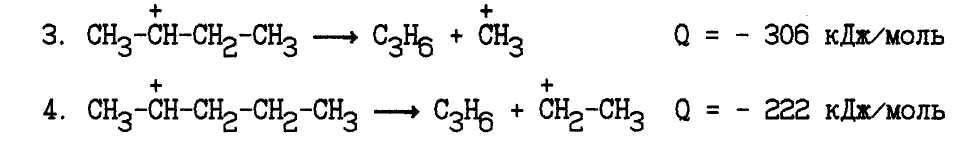
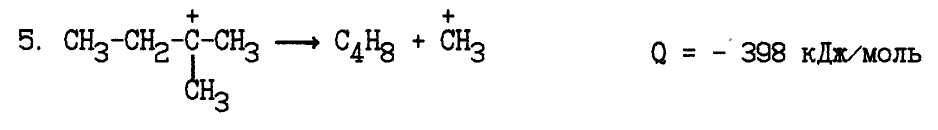
Легко протекает распад первичных карбкатионов, если при этом образуется вторичный и, особенно, третичный карбкатион:

Распад вторичных карбкатионов с образованием тех же ионов несколько труднее.
Энергетика распада и изомеризации показывает, что в большинстве случаев изомеризация должна предшествовать распаду. Устойчивость относительно распада третичных карбкатионов и их преимущественное образование при распаде больших карбкатионов должны приводить к образованию, в основном, изоструктур при распаде н-алкильных карбкатионов с большим числом атомов углерода.
Реакции присоединения карбкатионов к олефинам обратны реакциям распада, и поэтому характер закономерностей также противоположен характеру закономерностей распада:
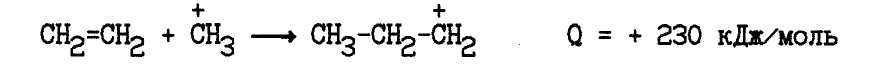
При присоединении данного иона к молекуле олефина реакция протекает более легко в ряду:
![]()
Реакции передачи протона могут происходить при взаимодействии карбкатионов с молекулой алкена:
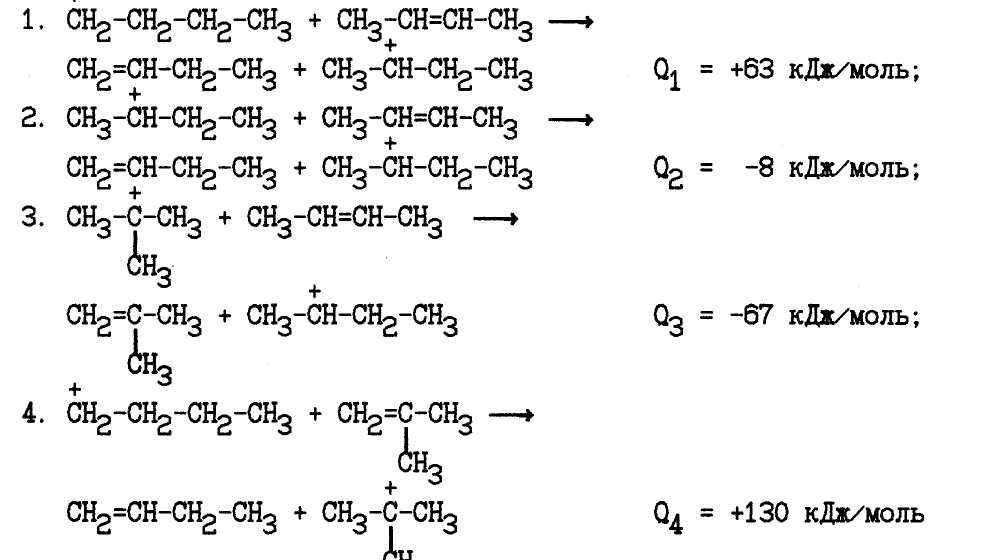
Сравнение энергетики этих реакций показывает, что наиболее легко протекает взаимодействие первичных карбкатионов с алкенами, если образуются вторичные и, особенно, третичные карбкатионы. Наибольшие затраты энергии требуются при передаче протона молекуле олефина третичным карбкатионом.
Реакции отрыва гидрид-иона
При взаимодействии с молекулой углеводорода карбкатион может отрывать электрон у первого гидрид-иона и превращаться в молекулу:
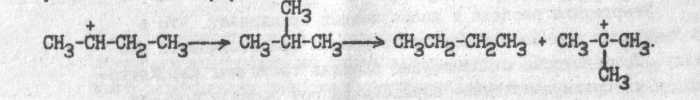
Стабилизация карбкатиона в соответствующий углеводород при отрыве гидрид-иона происходит легко, когда донором гидрид-иона является третичный атом углерода или атом углерода, сопряженный с π-связью или ароматическим кольцом. Активность карбкатионов также снижается в ряду
![]()
Наиболее энергетически выгодна реакция, когда образующийся ион третичный. Например:

По карбкатионному механизму протекают процессы, в которых катализаторы являются кислоты. Это каталитический крекинг, каталитическое алкилирование низкомолекулярных изоалканов и аренов алкенами, каталитическая изомеризация нормальных алканов и полимеризация алкенов.
Каталитический крекинг – один из наиболее распространенных в нефтепереработке каталитических процессов, цель которого – получение высокооктановых компонентов моторных топлив (бензинов) из нефтяных фракций, имеющих температурный предел кипения 240-500оС.
Каталитическое алкилирование низкомолекулярных изоалканов и аренов алкенами – процесс алкилирования изобутана бутиленом с целью получения высокооктанового компонента бензинов – технического изооктана.
Каталитическая изомеризация нормальных алканов – процесс, предназначенный для получения изоалканов, улучшающих антидетонационные свойства автомобильных бензинов и обеспечивающих легкость запуска двигателя в холодное время года.
Полимеризация алкенов – процесс для получения полимербензина, а также сырья для производства поверхностно-активных веществ. Полимербензин представляет собой смесь ди-, три- и тетрамеров пропилена, ди- и триммеров бутенов или смесь сополимеров пропилена и бутилена.