
- •Основные стехиометрические законы.
- •Закон химических эквивалентов. Молярные массы эквивалентов сложных веществ.
- •Волновые свойства электрона. Квантовые числа состояния электрона. Электронные орбитали.
- •Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
- •Связь периодического закона со строением электронных оболочек атомов. Правило Клечковского Энергетические ячейки. Правило Хунда.
- •Периодический закон д.И.Менделеева и периодическая система элементов: ряды, периоды, группы, подгруппы, порядковый номер элемента.
- •Периодическое изменение свойств химических элементов. Радиус атомов, сродство к электрону, энергия ионизации, электроотрицательность.
- •Образование химической связи. Энергия и длина связи.
- •Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов. Валентность.
- •Направленность ковалентной связи. Π – связи. Гибридизация атомных орбиталей.
- •Ионная (электронная) связь.
- •Представление о методе электронных орбиталей.
- •Полярность связи. Полярность молекул и дипольный момент.
- •Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
- •Межмолекулярное взаимодействие. Водородная связь.
- •Система. Фаза. Компонент. Параметры. Функция состояния: внутренняя энергия и энтальпия. Стандартные условия.
- •Первое начало термодинамики. Закон Гесса как следствие первого начала термодинамики. Термохимические расчеты.
- •Стандартная энтальпия образования. Следствие из закона Гесса.
- •Зависимость теплового эффекта химической реакции от температуры (закон Кирхгоффа).
- •Второе начало термодинамики. Понятие об энтропии. Расчет энтропии.
- •Постулат Планка. Стандартная энтропия веществ.
- •Объединенная формула первого и второго начал термодинамики. Свободная энергия Гиббса и Гельмгольца.
- •Зависимость f и g от температуры (уравнения Гиббса-Гельмгольца).
- •Условия самопроизвольного протекания химических реакций.
- •Изотерма химической реакции. Стандартное изменение свободной энергии.
- •Константа химического равновесия. Различные способы выражения констант равновесия . Соотношения между константами.
- •Зависимость константы химического равновесия от температуры (изобара и изохора химической реакции).
- •Принцип Ле-Шателье.
- •Скорость химической реакции. Закон действующих масс. Константа скорости.
- •Молекулярность и порядок реакции.
- •Кинетическая классификация по степени сложности. Обратимые и необратимые реакции.
- •Зависимость скорости химической реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса.
- •Энергия активации химической реакции. Аналитический и графический метод расчета.
- •Скорость гетерогенной химической реакции. Особенности ее протекания.
- •Инициирование химических реакций. Катализ. Сущность гомогенного и гетерогенного катализа.
- •Дисперсные системы. Коллоидные растворы.
- •Растворы (разбавленные, концентрированные, насыщенные, пересыщенные). Растворимость. Способы выражения концентраций растворов.
- •Физические и химические процессы при растворении. Растворимость твердых тел и жидкостей в жидкостях.
- •Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •Закон Рауля. Криоскопия и эбуллиоскопия.
- •Электролитическая диссоциация. Закон разведения Оствальда.
- •Сильные электролиты. Понятие активности и коэффициента активности.
- •Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель. Понятие об индикаторах.
- •Гидролиз солей. Константа и степень гидролиза.
- •Произведение растворимости. Условие выпадения осадка.
- •Овр. Ионно-электронный метод подбора коэффициентов в овр.
- •Возникновение скачка потенциала на границе раздела «металл-раствор». Равновесный электродный потенциал.
- •Медно-цинковый гальванический элемент Якоби-Даниэля. Процессы на электродах. Понятие эдс.
- •Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
- •Стандартный водородный электрод. Формула Нернста. Стандартный потенциал. Ряд напряжений. Расчет эдс гальванического элемента.
- •Типы электродов и цепей. Окислительно-восстановительные электроды и цепи.
- •Электролиз. Последовательность разряда ионов на катоде и аноде.
- •Законы Фарадея. Выход по току. Понятие химической и концентрационной поляризации при электролизе. Перенапряжение.
- •Классификация химических источников тока.
- •Коррозия металлов. Химическая и электрохимическая коррозия.
- •Основные методы борьбы с коррозией.
- •Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •Составные части системы и компоненты. Правило фаз. Диаграмма состояния однокомпонентной системы (на примере воды). ???? диаграмма
- •Сущность термографического анализа. Кривые нагревания и охлаждения. Принцип построения диаграммы плавкости бинарной системы.
- •Эвтектическая диаграмма плавкости (без образования твердых растворов).
- •Поверхностные явления. Понятие поверхностного натяжения.
- •Адсорбция и абсорбция. Изотермы адсорбции.
Коррозия металлов. Химическая и электрохимическая коррозия.
 Коррозия
– самопроизвольно протекающий процесс
поверхностного окисления металла в
результате его химического или
электрохимического взаимодействия с
окружающей средой.В результате коррозии
металл из свободного состояния переходит
в связанное. Потери от коррозии велики:
десятки миллиардов долларов в
индустриально-развитых странах.Химическая
коррозия (газовая и жидкостная).Газовая
– разрушение происходит в атмосфере
сухого газа – окислителя (кислород,
галогены).
Коррозия
– самопроизвольно протекающий процесс
поверхностного окисления металла в
результате его химического или
электрохимического взаимодействия с
окружающей средой.В результате коррозии
металл из свободного состояния переходит
в связанное. Потери от коррозии велики:
десятки миллиардов долларов в
индустриально-развитых странах.Химическая
коррозия (газовая и жидкостная).Газовая
– разрушение происходит в атмосфере
сухого газа – окислителя (кислород,
галогены).![]() На поверхности металла образуется
твердая пленка оксида.Скорость окисления
зависит от прочности пленки (наличия
или отсутствия трещин). Если пленка
растягивается, трещины образуются
легко. Если сжимается – гораздо
труднее.Это зависит от отношения мольных
объемов окислителя и металла.
На поверхности металла образуется
твердая пленка оксида.Скорость окисления
зависит от прочности пленки (наличия
или отсутствия трещин). Если пленка
растягивается, трещины образуются
легко. Если сжимается – гораздо
труднее.Это зависит от отношения мольных
объемов окислителя и металла.
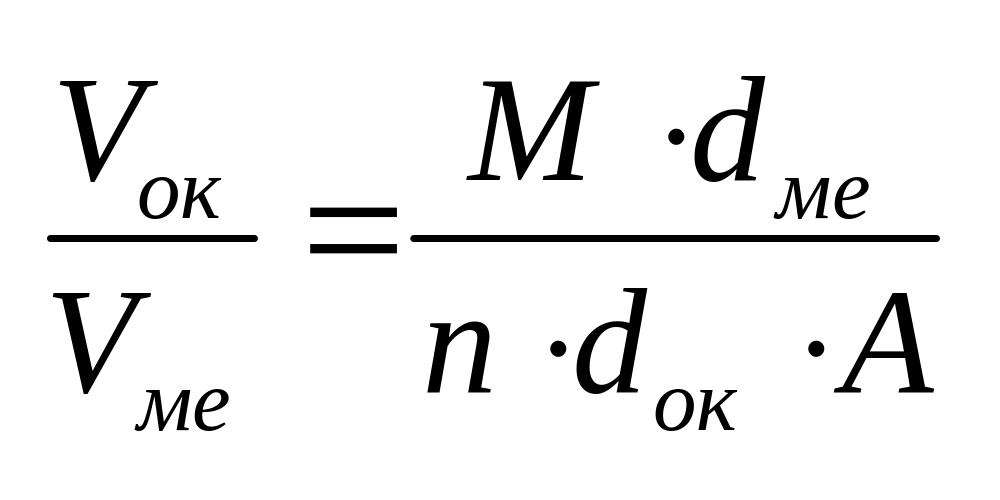 М – молекулярная масса оксида, d
– плотность, n – число
атомов в молекуле оксида, А – атомная
масса металла.Если отношение <1 =>
пленка растягивается, если >1 =>
сжимается.Некоторые металлы (железо,
алюминий, хром, нержавеющая сталь) могут
подвергаться пассивации (образование
на поверхности под действием реагентов
слоев, препятствующих коррозии).Пример.
М – молекулярная масса оксида, d
– плотность, n – число
атомов в молекуле оксида, А – атомная
масса металла.Если отношение <1 =>
пленка растягивается, если >1 =>
сжимается.Некоторые металлы (железо,
алюминий, хром, нержавеющая сталь) могут
подвергаться пассивации (образование
на поверхности под действием реагентов
слоев, препятствующих коррозии).Пример.
![]() Активными
газами, вызывающими газовую коррозию
являются – хлор, фтор, кислород,
сероводород.Жидкостная коррозия –
разрушение металла в жидкой непроводящей
среде (нефть, бензин, керосин, смазочные
масла). Скорость невелика.Электрохимическая
коррозия (гальванокоррозия и
электрокоррозия).Гальванокоррозия. При
протекании процесса разрушающийся
металл является отрицательным
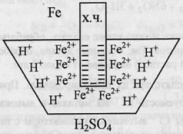
электродом.Рассмотрим пример.На
границе «металл-жидкость» образуется
слой ионов железа, удерживаемых
отрицательно заряженным металлом у
своей поверхности. Ионы железа удерживают
на расстоянии ионы водорода, не давая
им восстановиться за счет электронов
железа. Отсюда, коррозионная стойкость
химически чистого железа.В случае
технического железа (содержит примеси)
происходит восстановление ионов водорода
(пример примесей – углерод).Электрокоррозия.Идет
процесс электролиза под действием тока
от внешнего источника.Рассмотрим
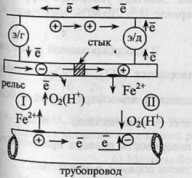
пример.Коррозия стального трубопровода
в почве под действием электрических
токов. Возникают 2 участка: 1. где рельс
(источник тока) играет роль катода (-), а
участок провода под ним – роль анода
(+).2. справа от стыка. рельс – анод, провод
– катод.Слева от стыка разрушается
трубопровод, справа – рельс.Разрушение
происходит локально – на ограниченном
участке.
Активными
газами, вызывающими газовую коррозию
являются – хлор, фтор, кислород,
сероводород.Жидкостная коррозия –
разрушение металла в жидкой непроводящей
среде (нефть, бензин, керосин, смазочные
масла). Скорость невелика.Электрохимическая
коррозия (гальванокоррозия и
электрокоррозия).Гальванокоррозия. При
протекании процесса разрушающийся
металл является отрицательным
электродом.Рассмотрим пример.На
границе «металл-жидкость» образуется
слой ионов железа, удерживаемых
отрицательно заряженным металлом у
своей поверхности. Ионы железа удерживают
на расстоянии ионы водорода, не давая
им восстановиться за счет электронов
железа. Отсюда, коррозионная стойкость
химически чистого железа.В случае
технического железа (содержит примеси)
происходит восстановление ионов водорода
(пример примесей – углерод).Электрокоррозия.Идет
процесс электролиза под действием тока
от внешнего источника.Рассмотрим
пример.Коррозия стального трубопровода
в почве под действием электрических
токов. Возникают 2 участка: 1. где рельс
(источник тока) играет роль катода (-), а
участок провода под ним – роль анода
(+).2. справа от стыка. рельс – анод, провод
– катод.Слева от стыка разрушается
трубопровод, справа – рельс.Разрушение
происходит локально – на ограниченном
участке.
Основные методы борьбы с коррозией.
Коррозия – самопроизвольно протекающий процесс поверхностного окисления металла в результате его химического или электрохимического взаимодействия с окружающей средой. В результате коррозии металл из свободного состояния переходит в связанное. Потери от коррозии велики: десятки миллиардов долларов в индустриально-развитых странах.Методы борьбы различны:
-антикоррозийное легирование металла
– введение в металл добавок, чтобы
повысить стойкость основного
металла.защитные покрытия
(металлические и неметаллические).металлические
наносятся под давлением сжатого воздуха.
характерно покрытие листового материала
тонким слоем другого материала.неметаллические
– лаки ,краски, битум, солидол.-ингибиторы
коррозии.вещества, замедляющие процесс
разрушения металла.Пример.
![]() -электрозащита.защищаемый
металл приводят в контакт с менее
благородным металлом (цинк или
магний).
-электрозащита.защищаемый
металл приводят в контакт с менее
благородным металлом (цинк или
магний).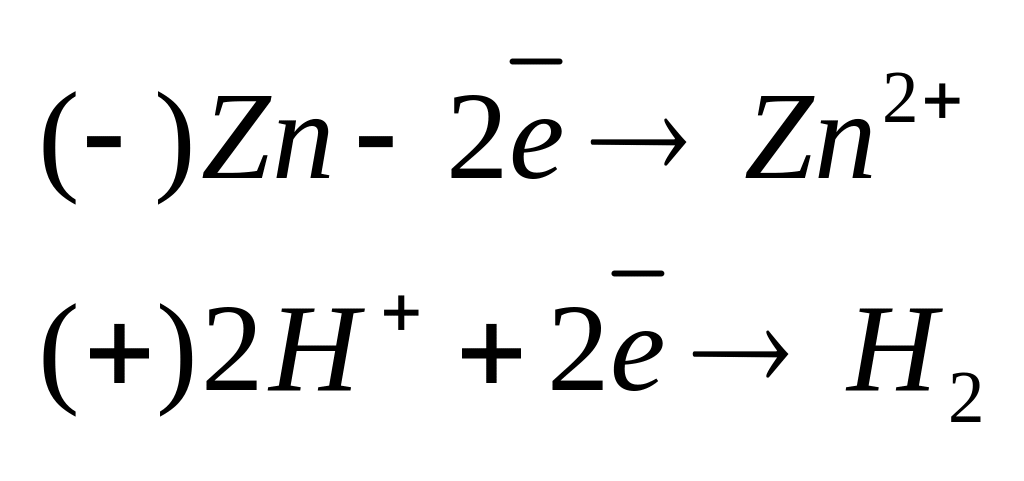 Поток
электронов направляется к защищаемому
металлу. Этот вид защиты используется
для магистральных труб, корпусов кораблей
и т.д.
Поток
электронов направляется к защищаемому
металлу. Этот вид защиты используется
для магистральных труб, корпусов кораблей
и т.д.
