
- •Основные газовые законы. Определение молекулярных масс газообразных веществ.
- •2. Основные стехиометрические законы.
- •3. Понятие о химическом эквиваленте и эквивалентной массе простых и сложных веществ. Закон химических эквивалентов.
- •4. Волновые свойства электрона. Квантовые числа, s-,p-,d-,f-состояния электрона. Электронные орбитали.
- •5. Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
- •6. Связь периодического закона со строением электронных оболочек атомов. Правило Клечковского. Энергетические ячейки. Правило Гунда.
- •7. Периодический закон д.И.Менделеева и периодическая система элементов: ряды, периоды, подгруппы, порядковый номер.
- •8. Периодическое изменение свойств химических элементов. Радиус атомов, сродство к электрону, энергия ионизации, электроотрицательность.
- •9. Образование химической связи. Энергия связи и длина связи.
- •10. Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов. Валентность.
- •11. Направленность ковалентной связи. Сигма и п-связи. Гибридизация атомных орбиталей.
- •12. Ионная (электронная) связь.
- •13. Полярная связь. Полярность молекул и их дипольный момент.
- •14. Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
- •15. Межмолекулярное взаимодействие. Водородная связь.
- •16. Система. Фаза. Компонент. Параметры. Функции состояния: внутренняя энергия и энтальпия. Стандартные условия.
- •17. Первое начало термодинамики. Закон Гесса как следствие 1-го начала термодинамики.
- •17. Первое начало термодинамики. Закон Гесса как следствие 1-го начала термодинамики.
- •18. Стандартная энтальпия образования. Следствие из закона Гесса. Термохимические расчеты.
- •19. Зависимость теплового эффекта реакции от температуры.
- •20. Второе начало термодинамики. Понятие об энтропии. Расчет энтропии.
- •21. Объединенная формула 1 и 2 начала термодинамики. Свободная энергия Гиббса и Гельмгольца.
- •22. Условия самопроизвольного протекания химических реакций.
- •23. Константа химического равновесия. Расчет Кр и Кс. Изотерма химической реакции.
- •24. Принцип подвижного равновесия (принцип Ле-Шателье).
- •25. Скорость химической реакции. Закон действующих масс. Константа скорости.
- •26. Молекулярность и порядок реакции.
- •28. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса.
- •29. Энергия активации химической реакции. Аналитический и графический метод расчета.
- •30. Скорость гетерогенной химической реакции.
- •31. Катализ. Сущность гомогенного и гетерогенного катализа.
- •32. Растворы (разбавленные, концентрированные, насыщенные, перенасыщенные).
- •33. Физические и химические процессы при растворении. Растворимость твердых тел и жидкостей в жидкостях.
- •34. Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •35. Законы Рауля.
- •36. Электролитическая диссоциация. Степень диссоциации. Слабые электролиты.
- •37. Константы диссоциации. Закон разведения.
- •38. Сильные электролиты. Понятие активности и коэффициента активности.
- •39. Электролитическая диссоциация воды. Ионные произведения воды. Водородный показатель. Понятие об индикаторах.
- •40. Гидролиз солей.
- •41. Окислительно-восстановительные реакции. Ионно-электронный метод подбора коэффициентов в окислительно-восстановительных реакциях.
- •42. Возникновение скачка потенциала на границе раздела «металл-раствор». Равновесный электродный потенциал.
- •43. Медно-цинковый гальванический элемент. Процессы на электродах. Эдс.
- •44. Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
- •45. Стандартный водородный электрод. Формула Нернста. Стандартный потенциал. Ряд напряжения.
- •46. Типы электродов и цепей. Окислительно-восстановительные электроды и цепи.
- •47. Электролиз. Последовательность разряда ионов на катоде и аноде.
- •48. Законы Фарадея. Выход по току.
- •49. Химическая и концентрационная поляризация при электролизе. Перенапряжение.
- •50. Классификация химических источников тока.
- •51. Коррозия металлов. Химическая и электрохимическая коррозия.
- •52. Основные методы борьбы с коррозией.
- •53. Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •54. Сущность физико-химического анализа. Правило фаз. Диаграмма состояния воды.
- •55. Основные принципы построения диаграммы плавкости бинарных систем. Термографический анализ.
- •60. Произведение растворимости. Условия выпадения осадка.
44. Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
1. Зависимость от природы.
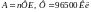
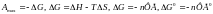
2. Зависимость от концентрации.

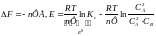
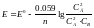
3. Зависимость от температуры.

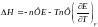

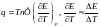
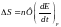
45. Стандартный водородный электрод. Формула Нернста. Стандартный потенциал. Ряд напряжения.
В наст. время невозможно рассчитать или экспериментально определить абсолютное значение скачка потенциала на отдельно взятом электроде. Поэтому значение потенциала на электроде всегда определяется по отношению к эталонному электроду, потенциал к-го условно принимается =0.В электрохимии таким электродом является нормальный водородный элемент (н.в.э.).Потенциал н.в.э. при опред-х условиях =0. В стеклянный сосуд сложной формы залит раствор серной кислоты такой концентрации, что [H+]»»1 г-ион/л.Платиновая чернь (губчатая пластина) – платиновый электрод.Р=1атм.Водород омывает платину, растворяется в ней. Насыщенная водородом платина начинает вести себя как водородный электрод, т.е.
H++к «« 1/2H2
2H+½ЅH2
jjH=0
Т.о. за величину электродного потенциала данного электрода принимается ЭДС гальванического элемента, составленного из исследуемого электрода и н.в.э. Электродному потенциалу присваевается знак, одинаковый со знаком заряда данного электрода в паре с н.в.э.
Например Zn в паре с н.в.э. заряжается отрицательно, а это значит, что потенциал Zn-го электрода равен ЭДС Zn-го водородного элемента с обратным знаком.
jjZn=jj0Zn+RT/nФ*ln aZn2+ jjMe=jj0Me+RT/nФ*ln[Men+] jj0-стандартное значение потенциала.Т=298К(250С). jjМе=jj0Ме+0.059/n*lg[Men+]
Если все металлы выстроить в ряд повелечинам их jj0, то мы получим т.н. ряд напряжений. В ряду напряжений помещен и jjН=0. Все металлы, расположенные в ряду напряжений выше Н имеют jj0<0, ниже - jj0>0В водородном электроде протекает реакция: H++к «« H – n=1 jjH= jj0H+0.059/1*lg[H+], jj0H =0 по условию. jjH =0.059lg[H+], pH=-lg[H+], jjH=-0.059pH. потенциала более положительного электрода вычесть потенциал менее положительного. Cu – Zn: E=jjCu-jjZn=jj0Cu-jj0Zn+RT/nФ*ln([Cu2+]-[Zn2+])=E0 E0-RT/nФ*ln[Zn2+]/[Cu2+] n=2; E0=jj0Cu-jj0Zn=0.34-(-0.763)=1.103B;E0экспериментальное=1.087В, DDE=0.016B-диффузионный скачок потенциалов на границе 2 растворов.
46. Типы электродов и цепей. Окислительно-восстановительные электроды и цепи.
1. Электроды 1 рода. Металлические, обратимые относительно катиона.
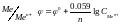
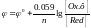

2. Металлические электроды, обратимые относительно аниона.
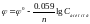
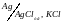
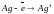
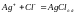
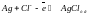
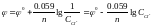
3. Газовые электроды, обратимые как относительно катионов, так и анионов.
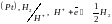

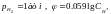
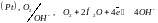

4. Окислительно-восстановительные электроды.
Металлическая пластина не принимает участия, она токоотвод.
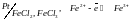
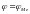
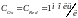

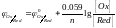

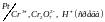

Типы цепей
1. Химические цепи – 2 разных металлических электрода (Al-Zn).
2. Окислительно-восстановительные цепи (2 ОВ-электрода)
ОВР течет самопроизвольно в сторону превращения сильного окислителя в слабый сопряженный окислитель, сильного восстановителя в слабый сопряженный восстановитель.
3. Концентрационные цепи.

Разные концентрации электролитов.
