- •Опорні лекції розділу Динамічна біохімія
- •Лекція №1. Загальні уявлення про обмін речовин і енергії
- •Суттєві ознаки обміну речовин у живих організмах:
- •Типи метаболічних реакцій
- •Шляхи використання енергії організмом:
- •Перетворення адф на атф
- •Проміжний метаболізм
- •Проміжний метаболізм
- •Лекція 2. Ферменти Основні питання:
- •Будова активного центру ферментів
- •Ферментативний аналіз
- •Лекція №3. Механізми перетворення поживних речовин у травному тракті
- •Основні перетравлювальні процеси
- •Сік підшлункової залози (підшлунковий або панкреатичний сік);
- •Сік, що виробляється клітинами печінки (жовч);
- •Сік, що виробляється слизовою оболонкою самої кишки (кишковий сік).
- •Білковий обмін
- •Білковий обмін: загальні відомості
- •Етапи розщеплення білків:
- •Процеси перетворення амінокислот і білків у товстій кишці
- •Гниття білків
- •Отруйні речовини
- •Шляхи розщеплення білків:
- •Біогенні аміни та реакції декарбоксилювання
- •Шляхи перетворення амінокислот в печінці
- •Лекція 5. Обмін вуглеводів
- •Розкладання вуглеводів у тканинах організму людини
- •Біосинтез вуглеводів в організмі
- •Лекція 6. Обмін ліпідів. Взаємозв’язок між різними процесами обміну речовин
- •Метаболізм жирів
- •Обмін нуклеїнових кислот
- •Взаємозв’язок між обміном вуглеводів і ліпідів:
- •Взаємозв’язок між обміном вуглеводів і білків:
- •Взаємозв’язок між обміном білків і ліпідів:
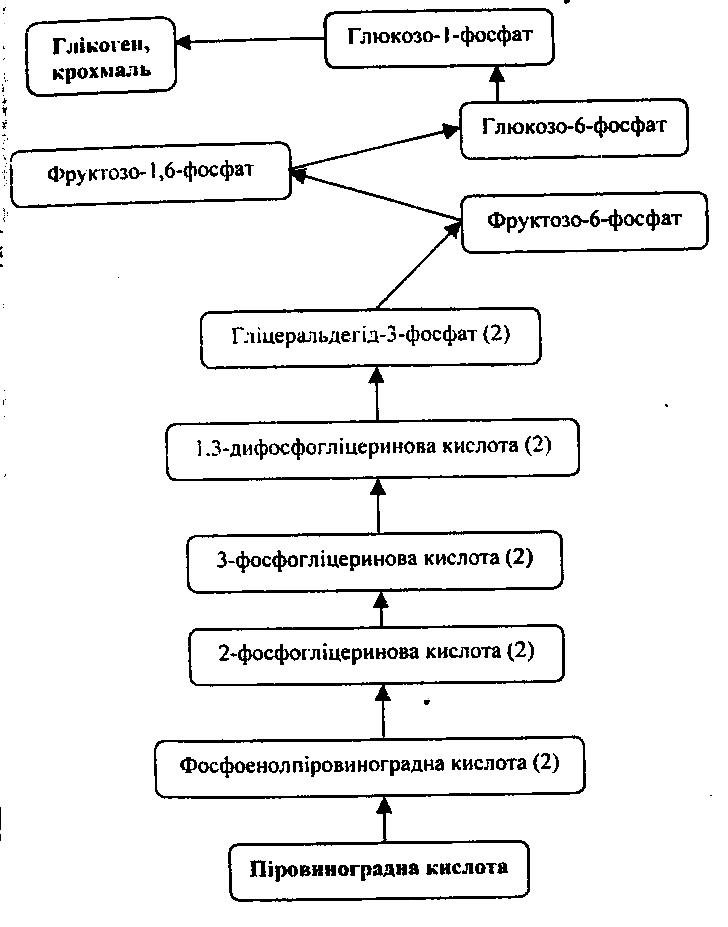
Біосинтез вуглеводів в організмі
Процес біосинтезу полісахаридів з вихідних речовин відбувається в тваринних клітинах по шляху, оборотному до процесу гліколізу.
Біосинтез вуглеводів в організмі відбувається:
синтез глікогену (з глюкози в печінці);
глюконеогенез: синтез вуглеводів із продуктів їх розкладу і сполук не вуглеводної природи (молочна та піровиноградна кислоти, гліцерин, амінокислоти, ацетил-КоА).
Лекція 6. Обмін ліпідів. Взаємозв’язок між різними процесами обміну речовин
Основні питання:
Перетравлювання та всмоктування ліпідів.
Транспортні форми ліпідів.
Метаболізм ліпідів.
Обмін нуклеїнових кислот.
Взаємозв’язок між різними процесами обміну речовин.
Етапи перетравлювання ліпідів
Відділ травної системи |
Процеси перетравлювання ліпідів |
|
|||
Шлунок (початок перетравлювання) |
Розщеплюється незначна кількість ліпідів із-за відсутності необхідних умов: ліпаза малоактивна при рН 1,5 – 2 (оптимум дії при рН = 5,5 – 7,5), здатна розщеплювати лише емульговані жири. Частковому гідролізу піддаються лише емульговані жири молока. У немовлят рН шлункового соку становить близько 5, що сприяє перетравлюванню емульгованих жирів молока ліпазою, що міститься в їх шлунку. |
|
|||
Тонка кишка (верхні відділи) – основні процеси перетравлювання ліпідів
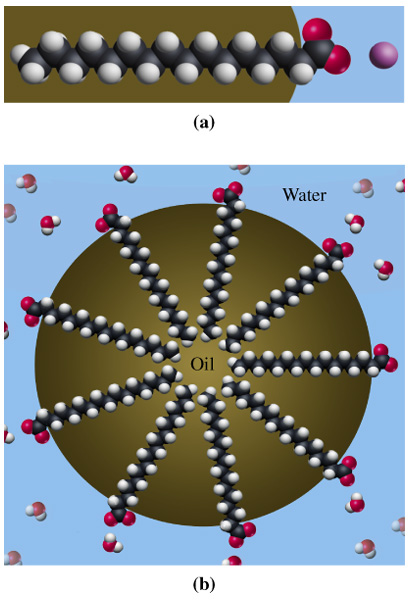
Схема утворення емульсії: а – молекула ПАР; b – орієнтація ПАР на межі поділу фаз олія – вода (гідрофобна частина ПАР спрямована до масла, а гідрофільна частина молекули спрямована до води)
|
Умови:
Після надходження хімусу з шлунку у дванадцятипалу кишку під впливом вугільної кислоти (виділяється внаслідок нейтралізації соляної кислоти, що потрапила з шлунку гідрокарбонатами панкреатичного соку) відбувається активне перемішування харчової маси і часткове емульгування жирів. Цьому сприяють солі жовчних кислот (мила), а також жовчні кислоти, які разом із жовчю виділяються у дванадцятипалу кишку. Жовчні кислоти синтезуються у печінці з холестерину, є похідними холанової кислоти, виділяються з жовчю в кишки у сполуках з гліцином і таурином. Парні жовчні кислоти (складаються з двох компонентів є сполуками жовчних кислот з таурином і гліцином. Зальна кількість жовчних кислот – 3-5г, синтезується цілодобово 0,5 – 0,8г. Роль жовчних кислот у забезпеченні процесу травлення:
Ферментативний гідроліз тригліцеридів проходить за участю ферментів панкреатичної ліпази та кишкової ліпази. Активність кишкової ліпази значно менша, ніж панкреатичної. Тригліцерид гліцерин + жирні кислоти (схема гідролізу жирів) |
|
|||
|
Розщеплення фосфоліпідів відбувається за участю ферментів фосфоліпаз, які виділяються у складі панкреатичного соку. Фосфоліпази А1; А2; С; Д, кожна з яких гідролізує певний складноефірний зв’язок у молекулах гліцерофосфоліпідів. Гідроліз фосфатидихоліну (лецитину): 1 стадія (від молекули лецетину відщеплюється молекула жирної кислоти, утворюється лізолецитин), каталізатор – фосфоліпаза А2: Лецитин Лізолецитин (дуже токсична сполука) 2 стадія ( відщеплення другої молекули жирної кислоти від молекули лізолецитину і утворення α-гліцерофосфохоліну), каталізатор – фосфоліпаза А1: Лізолецитин α-гліцерофосфохолін 3 стадія (відщеплення молекули холіну від молекули α-гліцерофосфохоліну і утворення α-гліцерофосфату), каталізатор – фосфоліпаза Д: α-гліцерофосфохолін α-гліцерофосфат + Холін 4 стадія (відщеплення молекули фосфорної кислоти від молекули α-гліцерофосфату і утворення гліцерину), каталізатор – фосфоліпазаС: α-гліцерофосфат Гліцерин + Фосфорна кислота Кінцевими продуктами розщеплення лецитину є гліцерин, жирні кислоти, холін і фосфорна кислота. |
|
|||
|
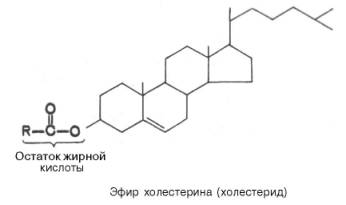
Розщеплення стеридів (ефіри холестерину): Фермент панкреатичної і кишкового соку – холестеринестераза Ефір холестерину Холестерин + Жирна кислота
|
|
|||
Тонка кишка (проксимальна частина) – всмоктування продуктів розщеплення жирів і ре синтез їх у стінках кишок |
Міцели: у гідрофобному ядрі – жирні кислоти, гліцериди, холестерин і деякі інші ліпіди, а зовнішня гідрофільна оболонка – жовчні кислоти і фосфоліпіди. Міцели майже в 100 разів менші, ніж краплі емульгованого жиру. Жовчні кислоти циркулюють між печінкою і кишками, щодобово вони здійснюють 5-6 циклів. Фосфорна кислота всмоктується стінками кишок в основному у вигляді солей калію або натрію. Азотисті основи гліцерофосфоліпідів – холін, етаноламін та інші всмоктуються в тонкій кишці у своїх активних формах. В епітеліальних клітинах з продуктів всмоктування синтезуються ліпіди, специфічні для даного організму. Процес синтезу жирів обмежений (частина чужорідних жирів відкладається в жировому депо в незмінному вигляді. |
||||
Ресинтезовані ліпіди, які всмокталися з порожнини кишок, і деякі продукти розщеплення жирів (жирні кислоти), які не були використані в ресинтезі, здатні сполучатися з білком крові і утворювати транспортні форми ліпідів.

Жири (триацилгліцерини) — найбільш важливий резерв енергії в організмі тварин. Вони зберігаються в основному в клітинах жирової тканини. Там же вони беруть участь в процесах утворення та деградації.
Жирні кислоти, які необхідні для синтезу жирів (ліпогенеза), у складі триацилглицеринів переносяться з печініки та кишечнику у вигляді ліпопротеїнових комплексів (ЛОНП та хіломікрони). Ліпопротеїн-ліпаза, що знаходиться на поверхні клітин кровоносних капілярів, відщеплює від цих ліпопротеїдів жирні кислоти.
В адипоцитах деградація жирів (ліполіз) каталізується гормонозалежною ліпазою. Рівень вільних жирних кислот, що надходять з жирової тканини, залежить від активності цієї ліпази — фермент регулює рівень жирних кислот у плазмі.
Жирні кислоти з жирової тканини транспортуються в плазму крові в неетерифікованій формі. При цьому розчинними є тільки жирні кислоти з малою кількістю атомів карбону, а жирні кислоти з більш довгими ланцюгами, менш розчинні у воді, переносяться в комплексі з альбуміном.
|
Транспорт ліпідів Утворення комплексів білків з ліпідами – ліпопротеїдів – сприяє розчинності і стабілізації ліпідів та забезпечує їх транспорт до різних органів і тканин організму. Зв’язок між білковою та ліпідною частинами в молекулах ліпопротеїдів залежить від наявності або відсутності в молекулі ліпідів іонізованих груп атомів. Якщо до складу простетичної групи ліпопротеїдів входять полярні ліпіди – фосфатиди, то між білком і ліпідним компонентом утворюються лабільні не ковалентні зв’язки. |
Деградація жирних кислот в печінці (на схемі зліва)
Жирні кислоти надходять з плазми крові до тканин; де з них синтезуються жири або за рахунок окислення надходить енергія. Особливо інтенсивно відбувається метаболізм жирних кислот в клітинах печінки (гепатоцитах).
Найбільш важним процесом деградації жирних кислот є β-окислення в мітохондріях. При цьому жирні кислоти спочатку активуються в цитоплазмі, приєднуючись до коферменту А. Потім вони за допомогою транспортної системи попадають в мітохондріальний матрикс, де руйнуються в результаті β-окислення до ацетил-КоА. Утворені ацетильні залишки повністю окислюються до СО2 в цитратному циклі з вивільненням енергії у вигляді АТФ (АТР). Якщо кількість утвореного ацетил-КоА перевищує енергетичну потребу гепатоцитів, що спостерігається при високому вмісту жирних кислот в плазмі крові (типові випадки — голодування та цукровий діабет), то в гепатоцитах синтезуються кетонові тіла, що забезпечують енергією вже інші тканини.
Синтез жирних кислот в печінці (на схемі праворуч)
Біосинтез жирних кислот відбувається в цитоплазмі, в основному в печінці, жировій тканині, нирках, легенях і молочних залозах. Головним джерелом атомів карбону є глюкоза, проте можливі інші попередники ацетил-КоА, наприклад, амінокислоти.
Перша стадія — карбоксилювання ацетил-КоА з утворенням малоніл-СоА — каталізується ацетил-КоА-карбоксилазою, ключевим ферментом біосинтезу жирних кислот. Утворення довголанцюгових жирних кислот здійснюється синтазою жирних кислот. Виходячи з молекули ацетил-КоА під дією цього поліфункціонального ферменту, ланцюг подовжується (процес включає сім реакцій) шляхом додавання малонільних груп і відщеплення СО2 (в кожній реакції) з утворенням пальмітату. Отже, в результаті кожної реакції молекула збільшується на два вуглецевих атоми. Як відновник використовується НАДФН + Н+, утворений в гексозомонофосфатному шляху або в реакціях, що каталізуються ізоцитратдегідрогеназою і «малатферментом».
Подовження ланцюга жирної кислоти при синтезі жирних кислот закінчується на C16, тобто на пальмітиновій кислоті. В наступних реакціях пальмітат використовується в якості попередника для одержання ненасичених або більш довголанцюгових жирних кислот.
Подальший біосинтез жирів відбувається за участю активованих жирних кислот (ацил-КоА) і 3-глицерофосфату. Для забезпечення інших тканин жири в гепацитах упаковуються у ліпопротеїнові комплекси типу ЛОНП (VLDL) і надходять в кров.
Біосинтез ліпідів
Біосинтез тригліцеридів проходить у різних органах і тканинах організму при наявності двох вихідних сполук – активного гліцерину (гліцеро-3-фосфату) та активних жирних кислот (ацетил КоА).
Біосинтез гліцерину відбувається з відновленням діоксиацетонфосфоату – проміжного продукту обміну вуглеводів.
В біосинтезі жирних кислот важливу роль відіграють ацетил-КоА, малоніл-КоА, НАДФ·Н + Н+, іони натрію, магнію, гідрокарбонат-іони, а також складний полі ферментний комплекс синтетаза жирних кислот.
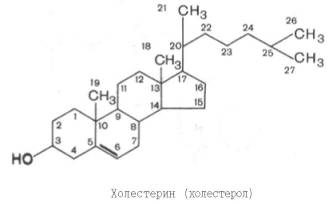
Холестерин синтезується з ацетил КоА, джерелом якого є оцтова кислота, ацетон, оцтовий альдегід, ацето-оцтова кислота та інші сполуки, які утворюються під час метаболічних реакцій.