- •Опорні лекції розділу Динамічна біохімія
- •Лекція №1. Загальні уявлення про обмін речовин і енергії
- •Суттєві ознаки обміну речовин у живих організмах:
- •Типи метаболічних реакцій
- •Шляхи використання енергії організмом:
- •Перетворення адф на атф
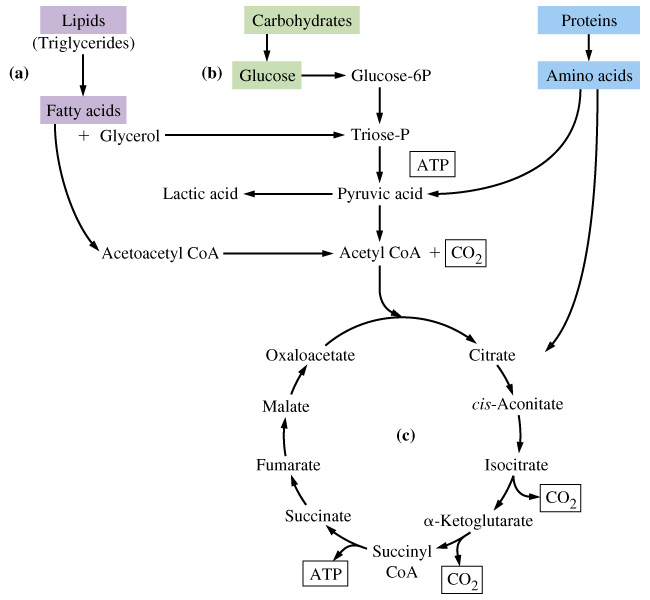
- •Проміжний метаболізм
- •Проміжний метаболізм
- •Лекція 2. Ферменти Основні питання:
- •Будова активного центру ферментів
- •Ферментативний аналіз
- •Лекція №3. Механізми перетворення поживних речовин у травному тракті
- •Основні перетравлювальні процеси
- •Сік підшлункової залози (підшлунковий або панкреатичний сік);
- •Сік, що виробляється клітинами печінки (жовч);
- •Сік, що виробляється слизовою оболонкою самої кишки (кишковий сік).
- •Білковий обмін
- •Білковий обмін: загальні відомості
- •Етапи розщеплення білків:
- •Процеси перетворення амінокислот і білків у товстій кишці
- •Гниття білків
- •Отруйні речовини
- •Шляхи розщеплення білків:
- •Біогенні аміни та реакції декарбоксилювання
- •Шляхи перетворення амінокислот в печінці
- •Лекція 5. Обмін вуглеводів
- •Розкладання вуглеводів у тканинах організму людини
- •Біосинтез вуглеводів в організмі
- •Лекція 6. Обмін ліпідів. Взаємозв’язок між різними процесами обміну речовин
- •Метаболізм жирів
- •Обмін нуклеїнових кислот
- •Взаємозв’язок між обміном вуглеводів і ліпідів:
- •Взаємозв’язок між обміном вуглеводів і білків:
- •Взаємозв’язок між обміном білків і ліпідів:
Біогенні аміни та реакції декарбоксилювання
R─CH─COOH R─CH2─NH2 + СО2
│
NH2 амін (реакція декарбоксилювання), каталізатор – ферменти декарбоксилази
Моноаміни, що утворюються в процесі декарбоксилювання, виявляють високу біологічну активність – біогенні аміни. Деякі з цих сполук є складовими частинами інших біомолекул. Так у складі фосфоліпідів крім амінокислоти серину може входит відповідний біогенний амін етаноламін. Цистеамін і β-аланін є структурними елементами коферменту А та пантетеїну. Утворений з треоніну амінопропанол є структурним елементом вітаміну B12. Деякі біогенні аміни діють як сигнальні речовини. Важливим нейромедіатором є утворена з глутамату γ-аміномасляна кислота [ГАМК (GABA)]. Інші нейромедіатори утворюються шляхом декарбоксилювання небілкових амінокислот. Так, з 3,4-дигідроксифенілаланіну (дофа) утворюється медіатор дофамін. Дофамін одночасно є попередником катехоламінів адреналіну та норадреналіну. Порушення метаболізму дофаміну є причиною хвороби Паркінсона. З триптофану через проміжний 5-гідрокситриптофан утворюється серотонін, сполука з широким спектром дії. Багато моноамінів і катехоламінів інактивуються аміноксидазою (моноаміноксидаза, "МАО") шляхом дезамінування з одночасним окисленням в альдегіди. |
|
Під час декарбоксилювання глутамінової кислоти утворюється γ-аміномасляна кислота, яка відіграє важливу роль у функціональній діяльності центральної нервової системи.
НООС─СН2─СН2─СН─СООН НООС─СН2─СН2─СН2─ NH2
│
NH2
Серотонін впливає на функції нервової, серцево-судинної та м’язової систем. Бере участь у регуляції тиску крові, в роботі органів дихання, в роботі травного каналу. Гістамін спричиняє секрецію соляної кислоти в шлунку, виявляє специфічну дію на нервові закінчення судин, зумовлюючи їх розширення і зниження тиску крові.
Аміни виявляють фізіологічну дію. При досить малих концентраціях. Нагромадження їх в організмі може викликати порушення ряду біохімічних процесів. Для запобігання цьому в тканинах є активна оксидаза, яка каталізує процеси окислення амінів до альдегідів і кислот, частина яких виводиться з організму з сечею, а інша частина піддається перетворенням:
R─ СН2─СН2─ NH2 + О2 R─ СН2─СН=NH + Н2О2
R─ СН2─СН=NH + НОН R─ СН2─СОН + NH3
R─ СН2─СОН + О R─ СН2─СООН
Висновок:
В результаті перетворень амінокислот утворюються аміак, оксид вуглецю (ІV), карбонові кислоти, кетокислоти, аміни та інші сполуки.
Якщо ці сполуки не використовуються в процесах синтезу, то вони піддаються подальшим перетворенням (крім аміаку та оксиду вуглецю): Аміни перетворюються на карбонові кислоти (окислювальне дезамінування), карбонові кислоти і кетокислоти – до води і вуглекислого газу.
Кінцеві продукти розщеплення амінокислот є аміак, вода і оксид вуглецю (ІV).
Синтез сечовини – ферментативний процес, що відбувається із затратою енергії АТФ. Більшість ферментів, які забезпечують синтез сечовини, знаходяться в мітохондріях клітин печінки, де інтенсивно відбуваються окислювально-відновні реакції. Сечовина виділяється з клітин печінки в кров, переноситься в нирки і виділяється з організму з сечею. Утворення сечовини в організмах людини і тварин є основним методом знешкодження аміаку |
|
.
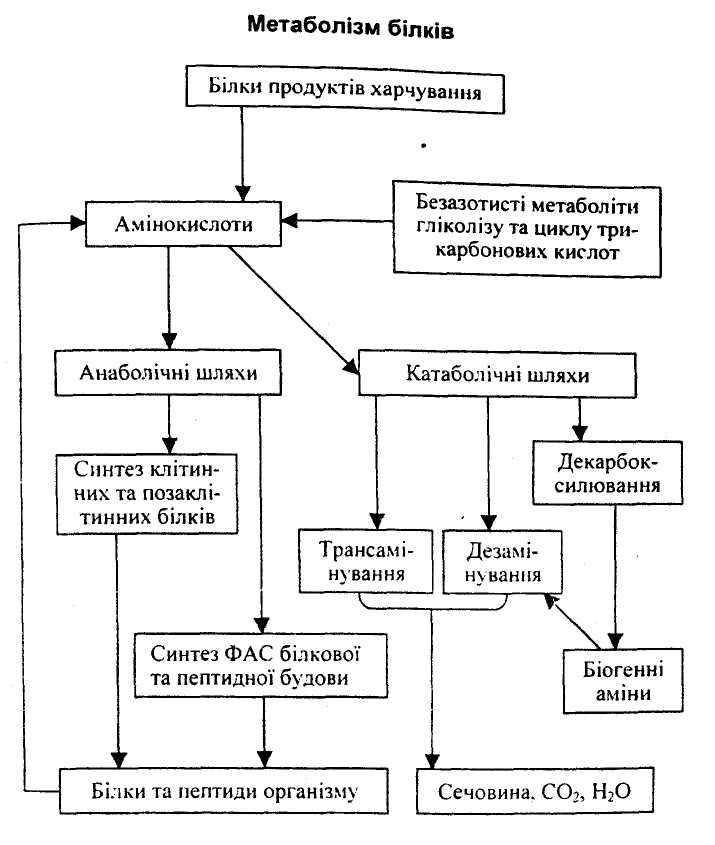
Схема загальних шляхів перетворення амінокислот