
- •Часть I
- •1. Введение
- •1.1. Углерод
- •1.2. Органические соединения
- •1.3.Значение органической химии
- •Иллюстрация
- •1.4. Контрольные вопросы
- •2. Основы теории строения
- •2.1. Основные положения теории химического строения а.М.Бутлерова
- •2.1.1. Формулы строения
- •2.1.2. Понятие о изомерии
- •2.1.2.1. Структурные изомеры
- •2.1.2.2. Стереоизомеры
- •2.2. Электронные представления в органической химии
- •2.2.1. Свойства электрона
- •2.2.2. Атомные орбитали
- •2.2.3. Форма и энергия атомных орбиталей
- •2.2.4. Заполнение атомных орбиталей электронами
- •2.3. Контрольные вопросы
- •1. Какое из положений теории а.М. Бутлерова объясняет различие в реакциях соединений одинакового состава:
- •2. Изомерами называются . . .
- •3.1. Электроотрицательность элементов
- •3.2. Основные типы химических связей
- •3.2.1. Ионная связь
- •3.2.2. Ковалентная связь
- •3.2.2.1. Свойства ковалентной связи
- •3.2.2.2. Характеристики ковалентной связи
- •3.2.2.3. Неполярная ковалентная связь
- •3.2.2.4. Полярная ковалентная связь
- •3.3. Контрольные вопросы
- •2. Как изменяется электроотрицательность элементов в Периодической системе?
- •4. Природа кoвалентной связи
- •4.1. Как взаимодействуют атомные орбитали при образовании молекул?
- •4.2. Молекулярные орбитали
- •4.2.1. Энергия молекулярных орбиталей
- •Влияние несвязывающих молекулярных орбиталей (нсмо) на форму молекул
- •4.2.2.Форма молекулярных орбиталей. - и -мо
- •4.3. Гибридизация атомных орбиталей
- •Vrml-модель (109 822 байт).
- •Vrml-модель (2 камеры, 109 300 байт).
- •Vrml-модель (108 646 байт).
- •4.3.4. Энергия гибридных атомных орбиталей
- •4.4. Моделирование атомных и молекулярных орбиталей с использованием прикладных программ
- •4.5. Механизмы образования ковалентной связи
- •4.6. Донорно-акцепторные связи
- •4.7. Кратные связи
- •4.8. Электронные формулы молекул
- •4.9. Атомно-орбитальные модели
- •4.10. Делокализованные -связи. Сопряжение
- •4.11. Водородные связи (н-связи)
- •Почему связи типа водородных не образуют атомы других элементов?
- •4.11.2. Влияние водородных связей на свойства веществ
- •4.12. Контрольные вопросы
- •9. Укажите тип гибридизации атомов углерода в молекуле:
- •5.1. Классификация соединений по строению углеродной цепи
- •5.2. Классификация соединений по функциональным группам
- •5.3. Контрольные вопросы
- •6. Типы органических реакций
- •6.1. Основные понятия. Химическая реакция
- •6.1.1. Скорость реакции
- •6.1.2. Энергия активации
- •6.1.3. Тепловой эффект реакции
- •6.1.4. Химическое равновесие
- •6.1.5. Катализ
- •6.2. Отличительные особенности органических реакций
- •6.3. Понятие о механизме химической реакции
- •6.4. Классификация органических реакций
- •6.4.1. Классификация реакций по конечному результату
- •6.4.2. Классификация реакций по числу частиц, участвующих в элементарной стадии
- •6.4.3. Классификация реакций по механизму разрыва связей
- •Примеры нуклеофильных реакций
- •Является . . .
- •Панели управления Cosmo Player Панель 1 Панель 2
2.2.3. Форма и энергия атомных орбиталей
Атомные орбитали (АО) разных типов отличаются друг от друга формой и энергией и обозначаются символами: s, p, d, f и т.д.
Органические вещества состоят в основном из элементов 2-го и 3-го периодов, валентные электроны которых находятся на s- и р-АО. Атомные орбитали s-типа имеют форму сферы:

Объем сферы увеличивается с ростом энергетического уровня:
1s < 2s < 3s и т.д.
р-АО имеют форму объемной восьмерки (гантели), направленной по оси x, y или z.
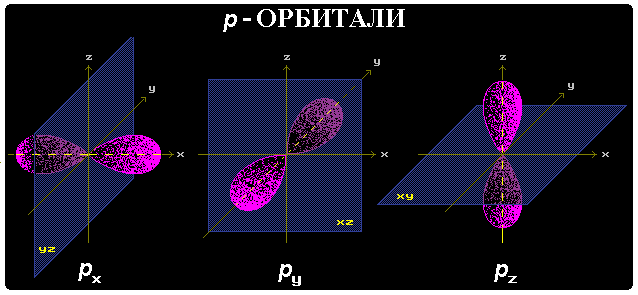
Размеры p-АО также увеличиваются с повышением энергетического уровня:
2p < 3p < 4p и т.д.
Энергия орбитали возрастает по мере удаления электрона от ядра атома (т.е. с увеличением номера электронного уровня).
Так, энергия s-АО увеличивается в ряду: 1s < 2s < 3s и т.д. Аналогично изменяется энергия р-АО: 2p < 3p < 4p и т.д. Внутри одного энергетического уровня энергия АО возрастает от s-АО к р-АО:
2s < 2p; 3s < 3p.
2.2.4. Заполнение атомных орбиталей электронами
При заполнении атомных орбиталей электронами соблюдаются три основные правила.
Принцип устойчивости. АО заполняются электронами в порядке повышения их энергетических уровней:
1s < 2s < 2p < 3s < 3p < 4s < 3d ...
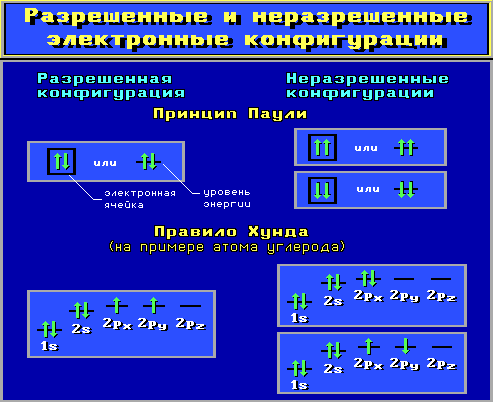
Принцип Паули. На одной АО могут находиться не более двух электронов с противоположными спинами.
Правило Хунда. На АО с одинаковой энергией, так называемых вырожденных орбиталях, электроны стремятся расположиться по одному с параллельными спинами.
 Электронные
конфигурации
Электронные
конфигурации
В химических превращениях принимают участие электроны внешнего электронного уровня - валентные электроны.
Наиболее распространенные в органических соединениях элементы (элементы-органогены) относятся в основном ко 2-му (C, N, O) и 3-му (P, S, Cl) периодам Периодической системы. Валентными электронами этих элементов являются 2s-, 2р- и 3s-, 3р-электроны, соответственно.
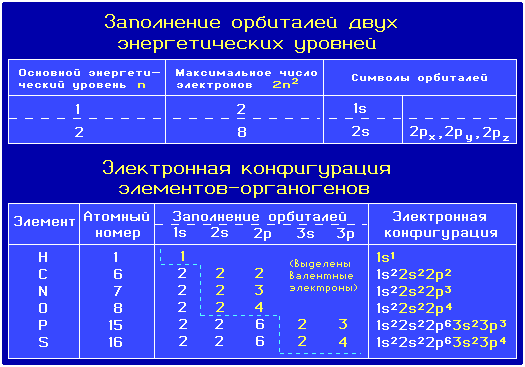 Валентные
электроны элементов-органогенов
Валентные
электроны элементов-органогенов
2.3. Контрольные вопросы
1. Какое из положений теории а.М. Бутлерова объясняет различие в реакциях соединений одинакового состава:
2 CH3-CH2-O-H + 2 Na 2 CH3-CH2-O-Na + H2 CH3-O-CH3 + Na реакция не идет
Ответ 1 : Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентности. Ответ 2 : Химическое строение можно устанавливать химическими методами. Ответ 3 : По свойствам данного вещества можно определить строение его молекул, а по строению молекул - предсказать свойства. Ответ 4 : Атомы и группы атомов в молекуле оказывают друг на друга взаимное влияние.
2. Изомерами называются . . .
Ответ 1 : вещества, имеющие сходное строение и сходные химические свойства, но разный количественный состав Ответ 2 : вещества, имеющие одинаковый качественный состав, но различные свойства Ответ 3 : вещества, имеющие одинаковый качественный и количественный состав, но различное строение молекул Ответ 4 : вещества, молекулы которых содержат одинаковое количество атомов углерода, но разное количество атомов других элементов
3.
Какие из представленных на рисунке
соединений являются изомерами?
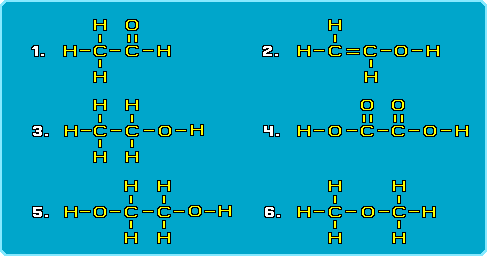
Ответ 1 : 1, 2 и 1, 5 Ответ 2 : 1, 2 и 3, 6 Ответ 3 : 3, 6 и 1, 5 Ответ 4 : 2, 3 и 1, 5
4. Что такое атомная орбиталь?
Ответ 1 : Орбита, по которой движется электрон в поле ядра атома. Ответ 2 : Часть пространства, в котором вероятность нахождения электрона минимальна. Ответ 3 : Область наиболее вероятного пребывания электрона в поле ядер атомов, составляющих молекулу. Ответ 4 : Область наиболее вероятного пребывания электрона в электрическом поле ядра атома.
5.
Укажите типы орбиталей “А” и “Г”:
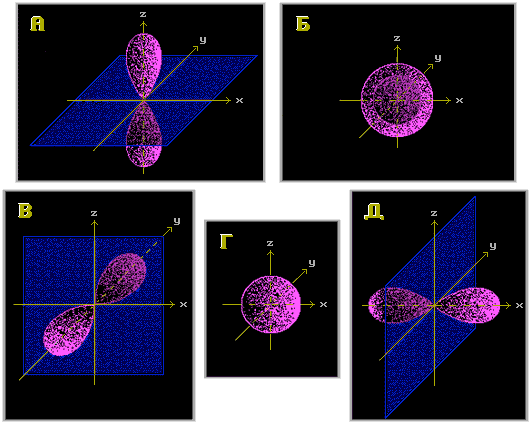
Ответ 1 :“А” - pz; “Г” - s Ответ 2 : “А” - s; “Г” - p Ответ 3 : “А” - pz; “Г” - px Ответ 4 : “А” - py; “Г” - s
6.
Неправильное заполнение атомных
орбиталей электронами
выражено
схемой . . .
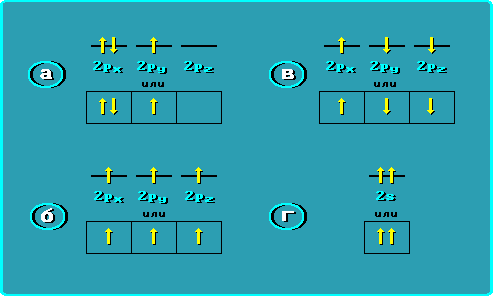
Ответ 1 : а, в, г Ответ 2 : в, г Ответ 3 : а, г Ответ 4 : г
3. ХИМИЧЕСКАЯ СВЯЗЬ
Связь между атомами химических элементов (химическая связь) имеет электростатическую природу и осуществляется взаимодействием внешних (валентных) электронов, в большей или меньшей степени удерживаемых положительно заряженными ядрами связываемых атомов.
Тип и свойства химической связи определяются электpоотрицательностью элементов, участвующих в ее образовании.
Представление о строении и особенностях химических связей между различными атомами необходимо для понимания того, как построены химические соединения и какие свойства (химические, физические) они проявляют
