- •Часть I
- •1. Введение
- •1.1. Углерод
- •1.2. Органические соединения
- •1.3.Значение органической химии
- •Иллюстрация
- •1.4. Контрольные вопросы
- •2. Основы теории строения
- •2.1. Основные положения теории химического строения а.М.Бутлерова
- •2.1.1. Формулы строения
- •2.1.2. Понятие о изомерии
- •2.1.2.1. Структурные изомеры
- •2.1.2.2. Стереоизомеры
- •2.2. Электронные представления в органической химии
- •2.2.1. Свойства электрона
- •2.2.2. Атомные орбитали
- •2.2.3. Форма и энергия атомных орбиталей
- •2.2.4. Заполнение атомных орбиталей электронами
- •2.3. Контрольные вопросы
- •1. Какое из положений теории а.М. Бутлерова объясняет различие в реакциях соединений одинакового состава:
- •2. Изомерами называются . . .
- •3.1. Электроотрицательность элементов
- •3.2. Основные типы химических связей
- •3.2.1. Ионная связь
- •3.2.2. Ковалентная связь
- •3.2.2.1. Свойства ковалентной связи
- •3.2.2.2. Характеристики ковалентной связи
- •3.2.2.3. Неполярная ковалентная связь
- •3.2.2.4. Полярная ковалентная связь
- •3.3. Контрольные вопросы
- •2. Как изменяется электроотрицательность элементов в Периодической системе?
- •4. Природа кoвалентной связи
- •4.1. Как взаимодействуют атомные орбитали при образовании молекул?
- •4.2. Молекулярные орбитали
- •4.2.1. Энергия молекулярных орбиталей
- •Влияние несвязывающих молекулярных орбиталей (нсмо) на форму молекул
- •4.2.2.Форма молекулярных орбиталей. - и -мо
- •4.3. Гибридизация атомных орбиталей
- •Vrml-модель (109 822 байт).
- •Vrml-модель (2 камеры, 109 300 байт).
- •Vrml-модель (108 646 байт).
- •4.3.4. Энергия гибридных атомных орбиталей
- •4.4. Моделирование атомных и молекулярных орбиталей с использованием прикладных программ
- •4.5. Механизмы образования ковалентной связи
- •4.6. Донорно-акцепторные связи
- •4.7. Кратные связи
- •4.8. Электронные формулы молекул
- •4.9. Атомно-орбитальные модели
- •4.10. Делокализованные -связи. Сопряжение
- •4.11. Водородные связи (н-связи)
- •Почему связи типа водородных не образуют атомы других элементов?
- •4.11.2. Влияние водородных связей на свойства веществ
- •4.12. Контрольные вопросы
- •9. Укажите тип гибридизации атомов углерода в молекуле:
- •5.1. Классификация соединений по строению углеродной цепи
- •5.2. Классификация соединений по функциональным группам
- •5.3. Контрольные вопросы
- •6. Типы органических реакций
- •6.1. Основные понятия. Химическая реакция
- •6.1.1. Скорость реакции
- •6.1.2. Энергия активации
- •6.1.3. Тепловой эффект реакции
- •6.1.4. Химическое равновесие
- •6.1.5. Катализ
- •6.2. Отличительные особенности органических реакций
- •6.3. Понятие о механизме химической реакции
- •6.4. Классификация органических реакций
- •6.4.1. Классификация реакций по конечному результату
- •6.4.2. Классификация реакций по числу частиц, участвующих в элементарной стадии
- •6.4.3. Классификация реакций по механизму разрыва связей
- •Примеры нуклеофильных реакций
- •Является . . .
- •Панели управления Cosmo Player Панель 1 Панель 2
9. Укажите тип гибридизации атомов углерода в молекуле:
1 |
2 |
3 |
4 |
CН3 |
СН = |
СН |
СН2 ОН |
Ответ 1 : 1 - sp2, 2 - sp, 3 - sp, 4 - sp2 Ответ 2 : 1 - sp3, 2 - sp2, 3 - sp, 4 - sp3 Ответ 3 : 1 - sp3, 2 - sp2, 3 - sp2, 4 - sp3 Ответ 4 : 1 - sp2d, 2 - sp2, 3 - sp2, 4 - негибридизованный
10. В каких случаях ковалентная связь образуется: а) по донорно-акцепторному механизму; б) по обменному механизму?
I. H + H H2 II. CH3NH2 + HCl [CH3NH3]+ Cl III. CH3OH + H+ CH3O+H2 IV. C + 2H2 CH4
Ответ 1 : а) II, III; б) I, IV Ответ 2 : а) I, IV; б) II, III Ответ 3 : а) II, III, IV; б) I Ответ 4 : а) II; б) I, III, IV
11. Какие электронные формулы соответствуют соединениям с кратными связями?

Ответ 1 : А, Г Ответ 2 : А, Б Ответ 3 : Б, В, Г, Д Ответ 4 : Б, В, Д
12. В каких молекулах имеются делокализованные -связи?
а) CH2=CHCH2CH=CH2
б) CH2=CHCH=CH2
в) CH2=CH2
Ответ 1 : а, б Ответ 2 : б, в Ответ 3 : б Ответ 4 : а
13. Укажите соединения, в которых есть атомы водорода, способные к образованию водородной связи:
а) CH3OCH3
б) CH3NH2
в) CH3CH3
г) CH3OH
Ответ 1 : а, г Ответ 2 : б, г Ответ 3 : а, б, г Ответ 4 : б, в, г
5. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Органические соединения отличаются своей многочисленностью и разнообразием. Поэтому необходима их систематизация. Органические соединения классифицируют, учитывая два основных структурных признака:
- строение углеродной цепи (углеродного скелета);
- наличие и строение функциональных групп.
Углеродный скелет (углеродная цепь) - последовательность химически связанных между собой атомов углерода.
Функциональная группа - атом или группа атомов, определяющие принадлежность соединения к определенному классу и ответственные за его химические свойства.
5.1. Классификация соединений по строению углеродной цепи
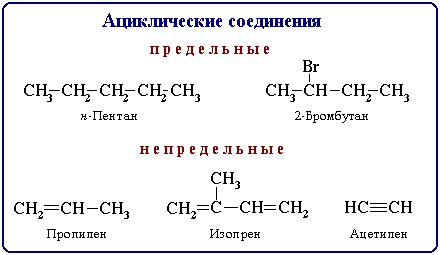
В зависимости от строения углеродной цепи органические соединения делят на ациклические и циклические.

Ациклические соединения - соединения с открытой (незамкнутой) углеродной цепью. Эти соединения называются также алифатическими.
Среди
ациклических соединений различают
предельные
(насыщенные),
содержащие в скелете только одинарные
связи C-C и непредельные
(ненасыщенные), включающие кратные связи
C=C и C![]() C.
C.
Ациклические соединения подразделяют также на соединения с неразветвленной и разветвленной цепью. В этом случае учитывается число связей атома углерода с другими углеродными атомами.
Неразветвленные и разветвленные углеродные цепи
Атом углерода, связанный в цепи только с одним другим атомом углерода, называют первичным, с двумя - вторичным, с тремя - третичным, с четырьмя - четвертичным.
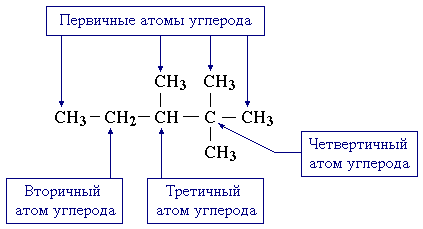
Цепь, содержащая только первичные и вторичные атомы углерода, называется неразветвленной или нормальной (обозначается буквой "н-" перед названием соединения).
Цепь, в которую входят третичные или четвертичные атомы углерода, является разветвленной (в названии часто обозначается приставкой "изо").
Например:

Атомы углерода: C - первичный; C - вторичный; C - третичный.
Циклические соединения - соединения с замкнутой углеродной цепью.
В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения. Карбоциклические соединения содержат в цикле только атомы углерода. Они делятся на две существенно различающихся по химическим свойствам группы: алифатические циклические - сокращенно алициклические - и ароматические соединения.
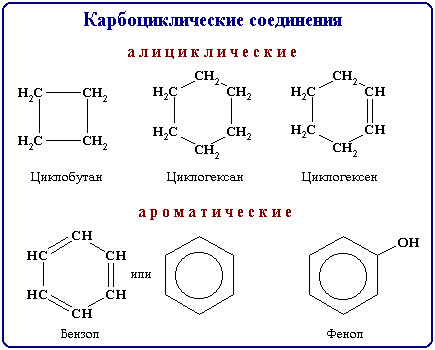
Гетероциклические соединения содержат в цикле, кроме атомов углерода, один или несколько атомов других элементов - гетероатомов (от греч. heteros - другой, иной) - кислород, азот, серу и др.