
- •Часть 1
- •Москва - 2004
- •Рекомендовано Институтом информатизации образования рао
- •Содержание
- •Введение ……………………………………………………………………….. 4
- •Введение
- •1. Углеводы
- •1.1Моносахариды (монозы)
- •1.1.1.Методы получения моносахаридов
- •1.1.2.Отдельные представители моносахаридов
- •1.1.2.1.Пентозы
- •1.1.2.2.Гексозы
- •1.1.3.Продукты превращений моноз
- •Тест по теме «Моносахариды»
- •Ответы на тестовые задания по теме «Моносахариды»
- •1..2.Олигосахариды
- •1.2.1.Отдельные представители дисахаридов
- •1.2.1.1.Невосстанавливающие дисахариды
- •1.2.1.2. Восстанавливающие дисахариды
- •1.2. 2.Отдельные представители трисахаридов
- •Тест по теме «Олигосахариды»
- •Вопросы для самоконтроля по теме «Олигосахариды»
- •Ответы на тестовые задания по теме «Олигосахариды»
- •1.3.Полисахариды
- •1.3.1.Отдельные представители полисахаридов
- •1.3.2.Производные полисахаридов
- •Тест по теме «Полисахариды»
- •Вопросы для самоконтроля по теме «Полисахариды»
- •Ответы на тестовые задания по теме «Полисахариды»
- •Тест по теме «Углеводы»
- •Вопросы для самоконтроля по теме «Углеводы»
- •Ответы на тестовые задания по теме «Углеводы»
- •2. Липиды
- •2.1.Простые липиды
- •Основные спирты липидов
- •Триольные липиды
- •Диольные липиды
- •Гликолипиды
- •2.1.1.Основные превращения простых липидов
- •2.1.2. Пищевая ценность жиров и масел.
- •2.2. Понятие о сложных липидах
- •Тест по теме «Липиды»
- •Б) кислотный гидролиз
- •Вопросы для самоконтроля по теме «Липиды»
- •Ответы на тестовые задания по теме «Липиды»
- •Список рекомендуемой литературы
- •Словарь основных понятий по теме «Углеводы»
- •Простые углеводы – углеводы, которые не способны гидролизоваться с образованием более простых углеводов.
- •Словарь основных понятий по теме «Липиды»
- •Для заметок
- •Органическая химия в пищевых биотехнологиях
- •Часть 1
1.1.3.Продукты превращений моноз
Восстановлением моносахаридов можно получать спирты. В качестве восстановителей применяют амальгаму натрия, каталитически возбужденный водород (катализаторы никель, хромит меди, в последнее время водный раствор натрийборгидрида -NaBH4). Практический интерес представляет восстановление ксилозы и глюкозы соответственно в ксилит и сорбит.
Ксилит - пятиатомный спирт получают восстановлением альдопентозы ксилозы.
COH CH2OH
H-C-OH H-C-OH
H2 / Ni
HO-C-H ----------------- HO-C-H
H-C-OH H-C-OH
CH2OH CH2OH
Д-ксилоза Д-ксилит
Ксилит (т.пл.61OС) хорошо растворяется в воде, в два раза слаще сахара, нетоксичен, используется при диетическом питании, при диабете и ожирении. Кроме того, ксилит применяют в качестве пластификатора в производстве целлофана, в парфюмерии, бумажной промышленности и др.
Сорбит - шестиатомный спирт получают восстановлением альдогексозы глюкозы.
COH CH2OH
H-C-OH H-C-OH
H2 / Ni
HO-C-H или NaBH4 HO-C-H
-----------------
H-C-OH H-C-OH
H-C-OH H-C-OH
CH2OH CH2OH
Д-глюкоза Д-сорбит
Сорбит (т.пл.110OС) широко распространен в природе в растениях. Он вдвое менее сладок, чем сахар, используется как заменитель сахара для больных диабетом и для производства аскорбиновой кислоты.
Аскорбиновая кислота - известна под названием витамина С (противоцинготный витамин) и по структуре химическа близка к моносахаридам.
Химическое название аскорбиновой кислоты -лактон-2,3-дегидро-L-гулоновая кислота.
Аскорбиновая кислота (т.пл. 190OС) хорошо растворяется в воде, имеет кисловатый вкус, оптически активна (имеет два асимметрических атома углерода), малоустойчива к окислителям, разрушается при нагревании.
Она широко распространена в растительном мире (в плодах, овощах, иглах хвойных деревьев и др.). Впервые аскорбиновую кислоту выделил Сент-Дьерди - венгерский химик-органик - в 1928 г. Ее структура может быть выражена формулой А и Б (см.далее). Аскорбиновая кислота играет важную роль в обмене веществ. Суточная потребность человека в витамине С около 100 мг.
Синтетически ее получают из глюкозы рядом превращений, которые можно изобразить следующими схемами:
COH
CH2OH
CH2OH
H-C-OH
H-C-OH
H-C-OH
HO-C-H
H2 / Ni HO-C-H [O]
HO-C-H [O]
-----------
---------
------------- H-C-OH
H-C-OH энзима-
H-C-OH после защиты
тическое
OH-группы H-C-OH
H-C-OH
C=O
CH2OH
CH2OH
CH2OH
Сорбит L-Сорбоза
CH2OH
CH2OH CH2OH
H-C-OH
H-C-OH H-C-OH
OH-C-H
H + C-H
C-H ---
----
H-C-OH
-H2O H-C-OH
C-OH
C=O
O C=O O C-OH
COOH
C=O C=O
(А)
(Б)
L-аскорбиновая
кислота (витамин С)











Она широко распространена в растительном мире (в плодах, овощах, иглах хвойных деревьев и др.). Впервые аскорбиновую кислоту выделил Сент-Дьерди - венгерский химик-органик - в 1928 г. Ее структура может быть выражена формулой А и Б. Аскорбиновая кислота играет важную роль в обмене веществ. Суточная потребность человека в витамине С около 100 мг. Аскорбиновая кислота (т.пл. 190OС) хорошо растворяется в воде, имеет кисловатый вкус, оптически активна (имеет два асимметрических атома углерода), малоустойчива к окислителям, разрушается при нагревании.
Брожение сахаров
Многие оксиальдегиды и оксикетоны способны под действием микроорганизмов претерпевать химические превращения, известные под названием брожений. Брожением называется процесс глубокого распада углеводов на более простые вещества под действием ферментов-микроорганизмов. Процессы брожения были известны давно. В 1857 году французский ученый Луи Пастер показал, что дрожжевые грибки, вызывающие брожение могут попадать из воздуха. Эти дрожжевые грибки были названы ферментами. Наиболее легко брожению подвергаются вещества с числом атомов углерода в молекуле кратным трем. Пентозы брожению не подвергаются.
Спиртовое брожение
Виноградный сахар - глюкоза в присутствии микроорганизмов - дрожжевых грибков превращается в спирт и углекислоту по реакции:
С6H12O6 --------------------------- 2CO2 + 2C2H5OH + 28ккал (1 ккал = 4,19 кДж)
(микроорганизмы)
Процесс брожения глюкозы сложный биохимический процесс, в результате которого образуются различные фосфорнокислые эфиры сахаров и глицерина. Источником фосфорной кислоты, принимающей участие в реакциях брожения, являются микроорганизмы, содержащие аденозинфосфорные кислоты, как например, аденозинтрифосфорная кислота, которая состоит из 6- аминопурина, связанного с пентозой - Д-рибозой, соединенной, в свою очередь, с тремя остатками фосфорной кислоты:
N==C---NH2
/
Сокращенно ее называют АТФ / CH
C---NH
CH H H H H
O O O
N----C---N--------C---C---C---C---CH2---O---P---O---
P--O---P---OH
HO OH
OH OH OH
-------O------




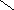
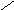














В качестве промежуточных и побочных продуктов брожения наряду с фосфорилированными сахарами и глицерином образуются янтарная, пировиноградная и уксусная кислота, уксусный альдегид и т.д. К вторичным продуктам, образующимся при спиртовом брожении, относятся сивушные масла, состоящие из смеси пропилового, изобутилового и изоамиловых спиртов.
Встречающиеся в природе простые сахара не применяются для промышленного получения спирта. В качестве исходных продуктов для получения этилового спирта используют крахмал и крахмалосодержащие продукты - хлебные злаки и картофель.
Схема производства спирта из картофеля и зерна
Сырье
-----
отделение -----
разваривание -----
разваренная -----
примесей
масса
----
осахаривание ----
солодовое размножение
молоко
дрожжей
Осахаренная м а
с с а зрелые
дрожжи
б р о ж е н и е
зрелая бражка
барда спирт






Картофель предварительно распаривают под давлением в автоклаве /запарнике/, при этом происходит разрыв клеточных оболочек и зерна крахмала превращаются в клейстер. Полученную массу переносят в заторные чаны и прибавляют дробленый солод - проросшие зерна ячменя, содержащее амилолитические ферменты - и - амилазы, под влиянием которых крахмал осахаривается, образуя декстрины и мальтозу.
H2O,
ферменты
(C6H10O5)n ------------ амило-, эритро-, ахродекстрины --- C12H22O11
крахмал мальтоза
Осахаренную жидкость сбраживают, прибавляя для этого к ней чистую культуру винных дрожжей, которые в растворе сахара быстро размножаются. Дрожжевые грибки содержат ферменты, под действием которых мальтоза в процессе брожения превращается в конечном итоге в спирт и углекислый газ.
ферменты, H2O
C12H22O11 --------------------- 2 C6H12O6 (глюкоза)
ферменты
C6H12O6 -------------- 2 СO2 + 2 C2H5OH (этанол)
Дальнейший процесс состоит в фракционной перегонке перебродившей жидкости. Перегнанные фракции многократно конденсируют с помощью ректификационных колонн и дефлегматоров - получают спирт - сырец 90 % концентрации. Остаток, называемый бардой, содержит янтарную кислоту, белки, жиры и глицерин. Барду применяют в качестве корма для скота. Полученный спирт-сырец подвергают дробной перегонке. Первый погон содержит ацетальдегид и ацетали, а главная фракция представляет собою 90-95 % этиловый спирт. В состав последней фракции входят сивушные масла, о которых говорилось выше, немного высших спиртов, жирных кислот и фурфурола. Чистый спирт имеет температуру кипения 78,3OC и содержит 95,5 % спирта.
Из спирта готовят ликеры добавляя воду, эссенции, сахар.
|
Продукты содержащие |
Спиртные напитки |
||
|
сахара |
до перегонки |
после перегонки |
|
|
1. Виноград |
вино |
коньяк |
|
|
2. Фрукты |
фруктовое вино |
- |
|
|
3. Патока |
- |
ром |
|
|
4. Вишни |
вишневая настойка |
вишневая водка |
|
|
5. Сливы |
вино |
сливовая водка |
|
|
Продукты содержащие |
Спиртные напитки |
|
|
крахмал |
до перегонки |
после перегонки |
|
1. Ячмень |
пиво |
виски |
|
2. Пшеница |
пиво, квас |
хлебная водка |
|
3. Рожь |
квас |
хлебная водка |
|
4. Картофель |
- |
водка, спирт |
|
5. Маис |
- |
виски |
|
6. Просо |
буза |
аррак |
Спирт находит широкое применение в химической промышленности для синтеза каучука и других веществ, в пищевой промышленности для изготовления вин, в фармацевтической промышленности, в органических синтезах душистых веществ, лаков, красителей полимеров и т.д.
Кроме спиртового брожения существуют и другие виды брожения: молочнокислое, лимонно-кислое, масляно-кислое и т.д. Эти реакции рассмотрены ниже.
Молочнокислое брожение
Д , L- молочная и левовращающая молочная кислоты образуются из декстрозы, из тростникового сахара и из мальтозы при действии бактерий Bacillus Delbriickii. Этот способ применяется для промышленного получения молочной кислоты. Процесс проводят при 50OC . К бродильной жидкости добавляют мел, так как кислотность отрицательно влияет на рост бактерий. Сахар сладкой сыворотки - молочный сахар превращается в молочную кислоту под действием бактерий.
Молочная кислота содержится в кислой капусте, огурцах, кислом молоке. Дисахариды сперва подвергаются гидролизу:
C12H22O11 + HOH --------- 2 C6H12O6
дисахарид моносахариды
Реакция молочнокислого брожения глюкозы:
C6H12O6 ------- 2 CH3-CH(OH)-COOH + 22,5ккал
глюкоза молочная кислота 1ккал=4,19кДж
Маслянокислое брожение
Масляная кислота получается из крахмала, из сахара, при различных бактериальных процессах брожения, как например, в присутствии бактерий Bacillus factisacidi и др.
Уравнение реакции маслянокислого брожения глюкозы:
C6H12O6 ------ 2 CO2 + 2H2 + CH3-CH2-CH2-COOH + 18 ккал
глюкоза масляная кислота
Лимонокислое брожение
При действии плесневых грибков (цитромицетов) углеводы (глюкоза, мальтоза) превращаются в лимонную кислоту.
цитромицеты OH
31-37OC
C6H12O6 +3 O -------------------- HOOC-CH2-C-CH2-COOH
COOH
Лимонная кислота применяется в пищевой промышленности.
Изучению биохимических процессов и, в частности, процессов брожения посвящены труды советских ученых - биохимиков: А.Н.Баха, А.И.Опарина, В.Н.Шапошникова, С.П.Костычева, В.С.Буткевича и др. Большая заслуга в изучении химии сахаров и глюкозидов принадлежит ученым - П.П.Шорыгину, Б.Н.Степаненко и др.
Замена пищевого сырья непищевым в производстве спирта
С целью экономии пищевого сырья за последние годы для получения спирта пользуются непищевым сырьем. Для этого подвергают гидролизу древесину в присутствии серной кислоты, затем очищают и нейтрализуют гидролизат, сбраживают гидролизную бражку.
Из одной тонны древесины получают 187 литров этанола, наряду с другими продуктами, как-то: фурфуролом, дрожжевыми кормами и т.д. Для получения этилового спирта используют так же отходы производства целлюлозы - сульфитные щелока. В настоящее время для получения спиртов и, в частности, этилового спирта пользуются синтетическими методами, Сырьем служат газы крегинга нефти, содержащие этиленовые углеводороды. В 1872 году А.М.Бутлеров и В.Горяинов впервые получили этиловый спирт из этилена по реакции:
+HOH
H2C=CH2 + HOSO3H ---- CH3-CH2-OSO3H -------- CH3-CH2OH + H2SO4
этилен этилсерная кислота этанол
В дальнейшем вместо серной кислоты применялась смесь последней с диэтилсульфатом, а затем - метод прямой гидратации олефинов при высоком давлении в присутствии катализатора и при повышенной температуре.
p,to
H2C=CH2 + HOH -------- CH3-CH2-OH
этанол
Спирты получают так же по реакции М.Г.Кучерова путем гидратации ацетилена в присутствии ртутных солей:
+2H
HCCH + HOH ----- H2C=CH ------- CH3-COH -------- CH3-CH2-OH
HO
ацетилен виниловый ацетальдегид этанол
спирт
Методы получения спиртов как путем брожения сахаристых веществ, так и синтетические рассматриваются более подробно в разделе о спиртах в органической химии, в курсах биологической химии и в технологии бродильных производств.
