
- •Выписка из учебной программы.
- •Раздел 2: обмен веществ.
- •Тема 2.3. Тканевое дыхание.
- •Практическое занятие № 34 – 4 часа.
- •Карта внутри- и межпредметных связей.
- •Учебно-методическое обеспечение занятия. Оборудование.
- •Учебно-методическое обоснование темы.
- •Цели и результаты обучения по уровням усвоения учебного материала (выписка из рабочей учебной программы)
- •Тестовый контроль.
- •Вариант 2.
- •Вариант 3.
- •Тестовый контроль
- •Комплексы дыхательной цепи.
- •Изучение инструкции.
- •Анализ и решение задач по теме «Тканевое дыхание».
- •Структура занятия.
- •Теоретическая часть:
- •Комплексы дыхательной цепи.
- •2. Указания к занятию:
- •3. Практическая часть.
- •Анализ и решение задач по теме «Тканевое дыхание». Задача 1.
- •Задача 2.
- •Задача 3.
- •Задача 4.
- •Задача 5.
- •4.1. Решение задач фронтально. Обсуждение.
- •Письменный контроль с использованием теоретических знаний по теме.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
- •Вариант 6.
- •Приложение № 6. Домашнее задание.
- •Приложение № 7. Список литературы для преподавателя и для учащихся. Для учащихся:
- •Для преподавателя:
- •9.2. Основные умения учащихся:
- •Приложение № 10. Критерии оценки знаний, умений учащихся.
- •Структура занятия.
- •1. Теоретическая часть:
- •Комплексы дыхательной цепи.
- •2. Указания к занятию:
- •3. Практическая часть.
- •Анализ и решение задач по теме «Тканевое дыхание».
- •Задача 5.
- •4. Закрепление знаний, умений учащихся.
- •4.1. Решение задач фронтально. Обсуждение.
- •5. Контроль знаний, умений учащихся.
- •По теме «тканевое дыхание. Решение ситуационных задач на знание роли нутриентов в работе цепи биологического окисления» Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
- •Вариант 6.
Комплексы дыхательной цепи.
I. НАДН·Н+-убихинон-оксидоредуктаза (около 30 белков, ФМН, 7 FeS-центров). Принимает электроны и протоны от НАДН·Н+; протоны выбрасываются в межмембранное пространство, электроны передаются на KoQ.
II. Сукцинат-убихинон-оксидоредуктаза (ФАД, 3 FeS-центра) принимает электроны и протоны от субстратов в матриксе и передает их на убихинон.
Убихинон – липофильная молекула, хинон, легко перемещается по мембране, принимает электроны и протоны от I и II комплексов дыхательной цепи и передает электроны на III комплекс.
Цитохромы, входящие в состав дыхательной цепи, представляют собой железосодержащие белки, простетическая группа которых представлена гемом. Цитохромы могут переносить только электроны за счет атома железа с переменной валентностью, входящего в состав гема.
Fe3+ + e ↔ Fе2+
III. Убихинол-цитохром-с-оксидоредуктаза (цитохромы в, с1, FeS-белок) переносит электроны с убихинола на цитохром с. Одновременно за счет энергии, выделившейся при переносе, протоны из матрикса перекачиваются в межмембранное пространство.
IV. Цитохром с – оксидаза (13 субъединиц, цитохромы а, а3, 2 атома меди) переносит электроны с цитохрома с непосредственно на кислород. Цитохромы а и а3, помимо атомов железа, содержат атомы меди, поэтому этот комплекс одновременно осуществляет полное (4-х электронное) восстановление молекулы кислорода. Энергия переноса электронов используется на перекачивание в межмембранное пространство протонов.
F1
АТФ
b2 АДФ + ФН
Матрикс
F0
Межмембранное
Н+ пространство
Как указывалось выше, для синтеза АТФ необходимо затратить около 32 кДж/моль энергии. Для этого достаточной является разность потенциалов между окислителем и восстановителем больше или равна 0,26 вольта. Чанс, Скулачев установили, что таких участков в дыхательной цепи три. Они соответствуют I, III и IV комплексам и названы пунктами сопряжения или фосфорилирования.
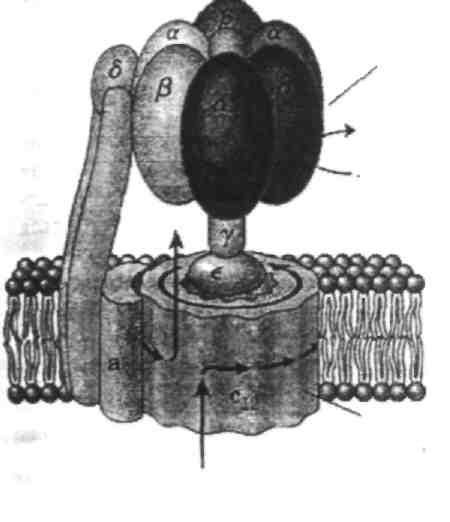
Чтобы понять связь между транспортом электронов по дыхательной цепи с синтезом АТФ, познакомимся с V комплексом внутренней мембраны митохондрий – ферментом, осуществляющим реакцию синтеза АТФ, и называемым протонной АТФ-синтазой. Этот ферментативный комплекс состоит из двух участков: F0 (о – олигомицин), который встроен в мембрану и пронизывает ее насквозь, и F1. Последний по форме напоминает шляпку гриба или дверную ручку и обращен в матрикс митохондрии (см. рис.). В изолированном виде F1 не может синтезировать АТФ, но может проводить ее гидролиз до АДФ и фосфата.
Реакция синтеза АТФ, которую проводит V комплекс, носит название окислительного фосфорилирования и описывается уравнением:
АДФ + Н3РО4 = АТФ + Н2О.
Биохимики долго искали связь – промежуточные макроэргические соединения, которые могли бы служить посредниками между процессом тканевого дыхания и окислительным фосфорилированием. Английский биохимик П. Mитчелл предположил, что синтез АТФ V комплексом ВММ сопряжен с особым состоянием этой мембраны и сформулировал хемиосмотическую теорию окислительного фосфорилирования (Нобелевская премия 1978 г.).
Основные постулаты этой теории:
-
внутренняя митохондриальная мембрана (ВММ) непроницаема для ионов, в частности для Н+ и ОН¯;
-
за счет энергии транспорта электронов через I, III, и IV комплексы дыхательной цепи из матрикса выкачиваются протоны;
-
возникающий на мембране электрохимический потенциал (ЭХП) и есть промежуточная форма запасания энергии;
-
возвращение (транслокация) протонов в матрикс митохондрии через протонный канал V комплекса за счет ЭХП является движущей силой синтеза АТФ.
Дальнейшие исследования (Дж. Уокер, П. Бойер, Нобелевская премия 1997 г.) подтвердили предположения Митчелла. Ими показано, что энергия движения протонов используется на конформационные изменения в активном центре АТФ-синтазы, что сопровождается синтезом АТФ, а затем ее высвобождением. Образовавшаяся АТФ с помощью транслоказы перемещается в цитозоль; взамен в матрикс митохондрии поступают АДФ и фосфат, причем транспорт фосфата сопровождается одновременным переносом в матрикс одного протона. Всего на процесс синтеза, высвобождения и выброса в цитозоль расходуется 4 протона.
При окислении НАД-зависимых субстратов в ММП, выбрасывается 10 протонов (см. сх. комплексов дыхательной цепи). В таком случае, может быть синтезировано 2,5 моль АТФ (10:4), т. е. коэффициент фосфорилирования Р/0 = 2,5. При окислении ФАД-зависимых субстратов в ММП, выбрасывается 6 протонов в III и IV пунктах сопряжения. В таком случае может быть синтезировано 1,5 моль АТФ (6 : 4) т. е. коэффициент фосфорилирования Р/0 = 1,5.
Теперь можно вернуться к пониманию энергетической функции цикла Кребса (см. тему «Цикл Кребса»). В ЦТК происходит 4 реакции дегидрирования, причем 3 ДГ являются НАД-зависимыми и одна – ФАД-зависимой. За счет окисления водорода 3-х молекул НАДН·Н+ в дыхательной цепи синтезируется 7,5 моль АТФ и окисление водорода 1 моль ФАДН2 ведет к синтезу 1,5 моль АТФ. Помимо этого, в ЦТК имеет место одна реакция субстратного фосфорилирования. Таким образом, энергетический выход окисления ацетил-КоА в цикле Кребса ранее 10 моль АТФ (7,5 + 1,5 + 1). Этой цифрой мы будем пользоваться в дальнейших расчетах.
Регулируется скорость работы дыхательной цепи энергетическим зарядом клетки, т. е. соотношением АТФ/АДФ. АДФ является стимулятором дыхательной цепи, АТФ-ингибитором.
Гипоэнергетические состояния возникают в организме вследствие дефицита АТФ в клетках. Причины их следующие:
-
алиментарные (голодание, гиповитаминозы РР, В2);
-
гипоксические (нарушения доставки О2 в клетки);
-
митохондриальные (действие ингибиторов и разобщителей).
Среди последних различают:
а) ингибиторы дыхательной цепи. Это яды, которые блокируют перенос электронов через I, II, III, IV комплексы. Ротенон и барбитураты блокируют I комплекс, малонат – II, антимицин А – III; цианиды, угарный газ блокируют перенос электронов на кислород, осуществляемый IV комплексом дыхательной цепи;
б) ингибиторы окислительного фосфорилирования (олигомицин), закрывающие протонный канал V комплекса;
в) разобщители окислительного фосфорилирования. Это вещества, которые подавляют окислительное фосфорилирование, не влияя при этом на процесс переноса электронов дыхательной цепью. Механизм действия разобщителей сводится к тому, что, являясь липофильными веществами, они обладают способностью связывать протоны и переносить их в матрикс, минуя протонный канал Н+ АТФ-синтазы. Выделяющаяся при переносе электронов энергия рассеивается в виде тепла. Различают:
-
разобщители естественные (продукты перекисного окисления липидов, жирные кислоты с длинной цепью, белки термогенины буровой жировой ткани, большие дозы йодсодержащих гормонов щитовидной железы);
-
разобщители искусственные (динитрофенол, производные витамина К, некоторые антибиотики).
