
Радиобиология с основами радиоэкологии
.pdf8. Действие малых доз ионизирующего излучения на живые организмы |
231 |
|
|
Влияние малых доз радиации на продолжительность жизни животных менее однозначно. С одной стороны, есть данные об ее увеличении под влиянием дозы 0.011 Гр у мышей и морских свинок. Облучение крыс на протяжении всей их жизни по 0.8 Гр в день повышает продолжительность их жизни. При увеличении дозы до 0.25 Гр/сут. продолжительность жизни возра стала с 445 до 650 и 590 сут. С другой стороны, при стимуляции жизнедеятельности возможно ускорение прохождения жизненного цикла – некоторое сокращение сроков жизни.
Итак, несмотря на высокую радиочувствительность млекопитающих, их легкую ранимость радиацией, существует такая область малых доз, несколько превышающих естественный фон, которая стимулирующе воздействует на организм: ускоряет развитие, повышает устойчивость к неблагоприятным условиям, увеличивает численность потомства.
Диапазон стимулирующих доз радиации в растительном мире значительно шире. Многолетняя проверка метода предпосевного γ-облучения семян кукурузы, подсолнечника, ржи, гречихи и других культур показала, что в полевых условиях за несколько лет урожай повышается. Конечно, в каждом годе в зависимости от погоды этот показатель колеблется. Более устойчивые результаты данный прием дает при выращивании овощей в закрытом грунте, где помимо прибавки урожая наблюдается еще и их более раннее созревание.
Сходный эффект при использовании существенно меньших доз, порядка 10–1 Гр, зафиксирован и при облучении вегетирующих растений: увеличивается количество дополнительных побегов за счет пробуждения почек, при облучении черенков усиливается образование корней, повышается масса надземной части растения и плодов.
Известно в практике медицины использование радонотерапии на курортах Цхалтубо, Пятигорска, Белокурихи. Радоновые ванны используют при многих заболеваниях. Оказалось, что облучение радоном тонизирует организм, мобилизует его защитные силы, т.е. активизирует проявление нормально присущих ему свойств, что так характерно для стимулирующего действия малых доз радиации. За курс лечения при приеме радоновых ванн кожа больного получает дозу в 40 раз большую, чем за счет естественного радиационного фона. Кожа, как очень разносторонний рецептор, отвечает на слабый радиационный импульс активацией некоторых физиологических процессов. Экспериментальные работы демонстрируют опосредованное влияние клеток кожи на увеличение фагоцитарной активности лейкоцитов, повышение уровня лизоцима, количества агглютининов, комплемента – факторов, принимающих непосредственное участие в создании иммунитета организма. Это усиление неспецифических иммунных реакций возрастало
232 |
Радиобиология с основами радиоэкологии |
|
|
к окончанию курса лечения и затем стойко держалось в течение нескольких месяцев.
Как же понять существование и механизм стимулирующего действия радиации? По мнению А.М. Кузина и других радиобиологов, радиация стимулирует далеко не все жизненные процессы, а только те, которые поддаются регулированию: это скорость деления клеток, синтез ДНК, РНК и белков, интенсивность дыхания и некоторые другие. Очевидно, радиация воздействует на внутриклеточные механизмы управления данными процессами и в малых дозах их активирует. В качестве таких стимуляторов могут выступать и ничтожно малые дозы радиотоксинов – биологически активных веществ, образую щихся под влиянием радиации в результате окисления фенолов (хиноидных радиотоксинов) и ненасыщенных жирных кислот (липидных радиотоксинов).
А.М. Кузин и некоторые другие исследователи считают, что при переходе в область малых доз и мощностей излучения активация протекающих процессов в живом организме связана, как правило, с возбужденным состоянием молекул и их систем. Именно процессы возбуждения под влиянием ионизирующей радиации занимают ведущее положение среди первичных причин, вызывающих стимуляцию деления клеток, роста и развития. При действии малых доз радиации происходит возбуждение молекул, входящих в построение многочисленных рецепторов биомембран. Рецепторы белковой природы с включенными в них полициклическими остатками аминокислот и взаимодействующие с полиненасыщенными жирными кислотами на основе гидрофобных связей представляют упорядоченную структурную среду, в которой попадание даже одного высокоэнергетического кванта или частицы способно вызвать конформационные изменения в рецепторах и тем самым дать сигнал, сыграть роль триггера в запуске нормальной физиологической реакции на данный сигнал. Если большие дозы радиации поражают структуру генома и его функции, то малые дозы могут влиять на экспрессию генов непосредственно через возбужденные макромолекулы генома или опосредованно воздействуют на рецепторы мембран.
Первое фундаментальное различие в действии больших и малых доз радиации заключается в том, что при высоких дозах ведущее положение в развитии радиобиологического эффекта играет ионизация, в то время как при малых – возбуждение молекул и систем. Возбуждение не любых молекул, а гигантских молекул биополимеров, белков, нуклеиновых кислот, образующих основу живых организмов.
Гормезис, проявляясь в виде соматических реакций, одновременно может способствовать проявлению молекулярных повреждений вследствие развития стохастических эффектов – генетических нарушений и трансформации клеток.
8. Действие малых доз ионизирующего излучения на живые организмы |
233 |
|
|
8.5. Стохастические эффекты малых доз ионизирующего излучения
Под стохастическими эффектами понимают такие по следствия облучения, вероятность появления которых суще ствует при сколь угодно малых дозах ионизирующего излуче ния и возрастает с дозой, тогда как тяжесть проявления об лучения от дозы не зависит и не имеет дозового порога.
В отличие от них нестохастические эффекты проявляются только после накопления дозы выше пороговой и вероятность их появления и тяжесть возрастают с накоплением дозы.
Для нестохастических последствий облучения характерны наличие дозового порога повреждающих эффектов и увеличение тяжести изменений с ростом дозы радиации. Тяжесть этих изменений связана с количеством поврежденных клеток. К не стохастическим эффектам относят лучевую катаракту, нарушение репродуктивной функции, лучевые поражения зародыша и плода, хромосомные аберрации, точковые мутации, трансформацию клеток, склеротические и дистрофические повреждения разных тканей. В настоящее время все больше появляется данных, свидетельствующих о значимости вклада стохастических эффектов в формирование тератогенных последствий облучения и сокращения продолжительности жизни – в той степени, в какой вероятностные процессы участвуют в феномене старения организма. Даже в отношении катаракты хрусталика есть сведения, позволяющие думать об отсутствии порога и, следовательно, о стохастической природе эффекта.
8.5.1. Радиационный канцерогенез при облучении в малых дозах, оценка риска
К стохастическим эффектам относят рак и передаваемые потомству наследственные изменения. Они обнаруживаются лишь при длительном наблюдении за большими группами населения (десятки или сотни тысяч человек). Для получения надежных количественных данных о влиянии на наследственность облучения в малых дозах необходим анализ еще более многочисленных популяций, включающих не одно поколение потомков облученных организмов. Всякий отрицательный в этом отношении факт, даже один на тысячу положительных, особенно если идет речь о здоровье человека, заставляет быть осторожным в отношении поспешных и однозначных выводов.
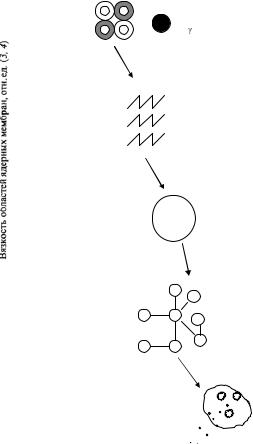
Малые дозы облучения могут «запустить» не до конца еще установленную цепь событий, приводящую к раку или генетическим повреждениям (рис. 8.5). При больших дозах радиация может разрушать клетки, повреждать ткани органов и явиться причиной скорой гибели организма.
234 |
Радиобиология с основами радиоэкологии |
|
|
. . . .
. . . .
Заряженные частицы. Проникающие в ткани организма альфа- и
бетачастицы теряют энергию вследствие электрических взаимодействий с электронами тех атомов, вблизи которых они проходят.
( -излучение и рентгеновские лучи передают свою энергию веществу несколькими способами, которые в конечном счете также приводят к электрическим взаимодействиям).
Электрические взаимодействия. За время порядка десяти трил-
лионных секунды после того, как проникающее излучение достигнет соответствующего атома в ткани организма, от этого атома отрывается электрон. Он заряжен отрицательно, поэтому остальная часть исходно нейтрального атома становится положительно заряженной. Этот процесс называется ионизацией. Оторвавшийся электрон может далее ионизировать другие атомы.
Физико-химические изменения. И свободный электрон, и
ионизированный атом обычно не могут долго пребывать в таком состоянии и в течение следующих десяти миллиардных долей секунды участвуют в сложной цепи реакций, в результате которых образуются новые молекулы, включая и такие чрезвычайно реакционноспособные, как «свободные радикалы».
Химические изменения. В течение следующих миллионных долей секунды образовавшиеся свободные радикалы реагируют как друг с другом, так и с другими молекулами и через цепочку реакций, еще не изученных до конца, могут вызвать химическую модификацию важных в биологическом отношении молекул, необходимых для нормального функционирования клетки.
Биологические эффекты. Биохимические изменения могут произойти как через несколько секунд, так и через десятилетия после облучения и явиться причиной немедленной гибели клеток или таких изменений в них, которые могут привести к раку.
Рис. 8.5. Воздействие ионизирующего излучения на ткани организма
(Радиация..., 1998).
Повреждения, вызываемые большими дозами облучения, обыкновенно проявляются в течение нескольких часов или дней. Раковые заболевания, однако, возникают спустя много лет после облучения – как правило, не ранее чем через однодва десятилетия. А врожденные пороки развития и другие наследственные болезни, вызываемые повреждением генетического аппарата, обнаруживаются лишь в следующем или последующих поколениях: это дети, внуки и более отдаленные потомки индивидуума, подвергшегося облучению.
В то время как идентификация быстро проявляющихся («острых») последствий от действия больших доз облучения не составляет труда, обнаружить отдаленные последствия от малых доз облучения почти всегда очень трудно. Частично это объясняется тем, что для их проявления должно пройти мно-
8. Действие малых доз ионизирующего излучения на живые организмы |
235 |
|
|
го времени. Но даже и обнаружив какие-то эффекты, требуется еще доказать, что они связаны с действием радиации, поскольку и рак, и повреждения генетического аппарата могут быть вызваны не только радиацией, но и множеством других причин.
Чтобы вызвать острое поражение организма, дозы облучения должны превышать определенный уровень, но нет никаких оснований считать, что это правило действует в случае таких последствий, как рак и повреждение генетического аппарата. По крайней мере, теоретически для этого достаточно самой малой дозы. Однако в то же самое время никакая доза облучения не приводит к данным последствиям во всех случаях. Даже при относительно больших дозах облучения далеко не все люди обречены на эти болезни: действующие в организме репарационные механизмы могут ликвидировать повреждения. Точно так же любой человек, подвергшийся действию радиации, совсем не обязательно должен заболеть раком или стать носителем наследственных болезней; однако вероятность или риск наступления таких последствий у него больше, чем у человека, который не был облучен. И риск тем больше, чем выше доза облучения.
Рак – наиболее серьезное из всех последствий облучения человека при малых дозах, по крайней мере, непосредственно для тех людей, которые подверглись облучению. Обширные обследования, охватившие около 100 тыс. человек, переживших атомные бомбардировки Хиросимы и Нагасаки в 1945 г., показали, что пока рак является единственной причиной повышенной смертности в данной группе населения.
Оценки НКДАР ООН риска заболевания раком в значительной мере опираются на результаты обследования людей, переживших атомную бомбардировку. Комитет использует и другие материалы, в том числе сведения о частоте заболевания раком среди жителей островов в Тихом океане, на которых выпали радиоактивные осадки после ядерных испытаний в 1954 г., среди рабочих урановых рудников и среди лиц, прошедших курс лучевой терапии. НКДАР ООН в своих оценках риска населения при малых дозах облучения опирается на два основных допущения. Согласно первому, не существует пороговой дозы, до которой отсутствует риск заболевания раком. Любая сколь угодно малая доза увеличивает вероятность заболевания раком для человека, получившего эту дозу, и всякая дополнительная доза облучения еще более ее увеличивает. Второе допущение заключается в том, что вероятность или риск заболевания возрастает прямо пропорционально дозе облучения: при удвоении дозы риск удваивается, при получении трехкратной дозы – утраивается и т.д. Согласно имеющимся данным, первыми в группе раковых заболеваний, поражающих население в результате облу-
236 |
Радиобиология с основами радиоэкологии |
|
|
чения, стоят лейкозы. Они вызывают гибель людей в среднем через 10 лет с момента облучения – гораздо раньше, чем другие виды раковых заболеваний.
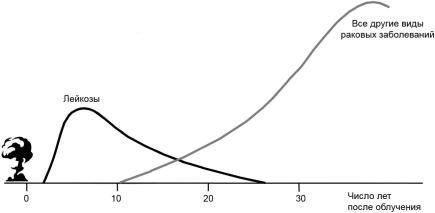
Относительная среднестатистическая вероятность заболевания раком после получения однократной дозы в 1 рад (0.01 Гр) при равномерном облучении всего тела представлена на рис. 8.6. На графике, построенном на основании результатов обследования людей, переживших атомную бомбардировку, показано ориентировочное время появления злокачественных опухолей с момента облучения. Прежде всего, после двухлетнего скрытого периода развиваются лейкозы, достигая максимальной частоты через шесть-семь лет; затем частота плавно уменьшается и через 25 лет становится практически равной нулю. Солидные (твердые) опухоли начинают развиваться через 10 лет после облучения, но исследователи не располагают пока достаточной информацией, позволяющей построить всю кривую.
Смертность от лейкозов среди тех, кто пережил атомные бомбардировки Хиросимы и Нагасаки, стала резко снижаться после 1970 г.; по-видимому, «дань» лейкозам в этом случае уплачена полностью. Таким образом, оценка вероятности умереть от лейкоза в результате облучения надежнее, чем аналогичные оценки для других видов раковых заболеваний. Согласно оценкам НКДАР ООН, от каждой дозы облучения в 1 Гр в среднем два человека из тысячи умрут от лейкозов. Иначе говоря, если кто-либо получит дозу 1 Гр при облучении всего тела, при котором страдают клетки красного костного мозга, то существует один шанс из пятисот, что этот человек умрет в дальнейшем от лейкоза.
Самыми распространенными видами рака, вызванными действием радиации, оказались рак молочной железы и рак щитовидной железы. По оценкам НКДАР, примерно у 10 че-
Рис. 8.6. Вероятность заболевания раком (Радиация..., 1988).
8. Действие малых доз ионизирующего излучения на живые организмы |
237 |
|
|
ловек из тысячи облученных отмечается рак щитовидной железы, а у 10 женщин из тысячи – рак молочной железы. Однако обе разновидности рака в принципе излечимы, а смертность от рака щитовидной железы совсем низка. Поэтому лишь пять женщин из тысячи, по-видимому, умрут от рака молочной железы и лишь один человек из тысячи облученных, повидимому, умрет от рака щитовидной железы. Рак легких тоже принадлежит к распространенным разновидностям раковых заболеваний среди облученных групп населения, которые, как правило, встречаются среди шахтеров урановых рудников. Рак других органов и тканей, как оказалось, встречается среди облученных групп населения реже. Согласно оценкам НКДАР, вероятность умереть от рака желудка, печени или толстой кишки составляет примерно всего лишь 1/1000 на каждый грей средней индивидуальной дозы облучения. Риск возникновения рака костных тканей, пищевода, тонкой и прямой кишки, мочевого пузыря, поджелудочной железы и лимфатических тканей еще меньше и составляет примерно от 0.2 до 0.5 случая на каждую тысячу и на каждый грей средней индивидуальной дозы облучения.
Врадиобиологии, как и в различных сферах хозяйственно полезной деятельности человека, используется вероятностный подход оценки степени риска при действии фактора – в данном случае он получил название «концепция биологического риска воздействия ионизирующего излучения». При оценке вероятностных последствий облучения учитывается не только степень риска, но и биологическая важность вызываемого им нарушения, сравниваемая с возможностью его возникновения при действии других неблагоприятных факторов, с которыми человек постоянно сталкивается в процессе жизнедеятельности. Решение проблемы состоит в оценке оптимального соотношения известной опасности воздействия определенного фактора и преимуществ его использования в интересах человека.
Вповседневной жизни человек постоянно подвергается риску подорвать здоровье и сократить продолжительность жизни.
Сразвитием достижений цивилизации вероятность такого риска, как правило, возрастает. Ведущее место занимают травмы и гибель в транспортных катастрофах, отравление газом и ядовитыми парами, пестицидами. Еще выше вероятность гибели в результате злокачественных новообразований, сердечно-сосу- дистых заболеваний, сосудистых поражений центральной нервной системы, в той или иной степени связанных с научно-тех- ническим прогрессом.
Так, в России ежегодно тонут в водоемах около 25 тыс. чел., т.е. частота случаев на 1 млн. населения, как принято рассчитывать степень риска, составляет 94 случая в год. Ежегодно гибнут в дорожно-транспортных происшествиях около 40 тыс.
238 |
Радиобиология с основами радиоэкологии |
|
|
чел., т.е. на 1 млн. – 150 случаев в год. Для некоторых других стран последний показатель еще выше: для Канады – 175, Австралии – 220, Германии – 233 случая. Для гражданина ка- кой-либо промышленно развитой страны, получающего сполна всю среднюю индивидуальную дозу от облучения как от естественных, так и от техногенных источников радиации, вероятность погибнуть в автомобильной катастрофе в пять раз, а вероятность преждевременной смерти из-за курения (при выкуривании 20 сигарет в день) более чем в 100 раз превышает вероятность умереть от рака вследствие облучения.
Спонтанная частота возникновения опухолей составляет по разным странам СНГ 1–2 тыс. случаев на 1 млн. населения в год, из которых свыше половины приводят к смертельному исходу.
На этом фоне цифры радиационного риска выглядят весьма скромно. Так, частота появления у человека наиболее хорошо изученного заболевания кроветворной системы лейкемии – одного из характерных заболеваний, индуцируемых ионизирующей радиацией из класса злокачественных, при дозе 0.01 Гр равна одному-двум случаям в год при его естественной частоте 50 случаев в год на 1 млн. населения. Суммарный же риск возникновения всех видов опухолей при этой дозе составляет тришесть случаев в год. Следует отметить, что доза 0.01 Гр может быть получена человеком в течение года лишь при 20–50-крат- ном увеличении естественного радиационного фона.
Все это свидетельствует о необычайной сложности и важности проблемы действия на организм малых доз ионизирующей радиации.
Оценки риска возникновения радиогенного рака при малых дозах различаются в 100 раз. В соответствии с линейной моделью МКРЗ, если 100 тыс. чел. облучаются в дозе 0.01 Гр, то за всю жизнь можно ожидать 1.25 случая возникновения рака, который следует выявить на фоне 1500–1700 спонтанных опухолей. Статистическая оценка достоверности превышения канцерогенного риска в результате действия ионизирующей радиации в малых дозах при эпидемиологических исследованиях в небольшой популяции весьма затруднительна.
Однако данные трансформации клеток in vitro с частотой 10–4 в результате облучения в дозе 1 сГр заставляют быть очень внимательными к действию малых доз радиации, так как в организме человека 1012 клеток могут подвергаться злокачественной трансформации. Оценки риска при низких дозах должны рассматриваться в свете всех имеющихся эпидемиологических данных. Так, по некоторым оценкам установлено, что авария на Чернобыльской АЭС может привести к 100–200 случаям смерти от рака в Швеции, если величину фактора риска принять равной 0.02 Зв на 1 чел.
8. Действие малых доз ионизирующего излучения на живые организмы |
239 |
|
|
Согласно концепции нормирования канцерогенов, предложенной В.А. Книжниковым (1983), допустимая доза канцерогена – это доза, обусловливающая величину превышения риска, не выходящего за пределы статистического отклонения значений спонтанного риска и, таким образом, не способная вызвать повреждающий эффект, который обнаруживают существующими методами исследования. Естественный канцерогенный риск (суммарно для всех локализаций) к настоящему времени можно оценить равным для человека около 200×10–5 случаев в год с ошибкой, равной приблизительно 4×10–5 случаев в год. Для риска за всю продолжительность жизни человека эта ошибка будет приблизительно равна 4×10–3, т.е. 0.4%. Таким образом, канцерогенный эффект от дозы, вызывающей риск, равный 4×10–3 за всю продолжительность жизни, не будет выявлен никакими методами исследования. Такая доза канцерогенеза может рассматриваться как допустимая для данного типа эффекта и представляет собой «практический порог».
Отдаленные последствия для здоровья людей, как отмечалось ранее, подвергшихся воздействию ионизирующей радиации в дозах, существенно превышающих фоновые, выявляются спустя годы и десятилетия от начала длительного низкоинтенсивного воздействия. Материалом для изучения и прогнозирования отдаленных биологических и медицинских последствий действия радиации служат данные диспансерного наблюдения за разными группами профессионалов, длительно работающих в сфере действия радиации (медицинские радиологи и рентгенологи; работники АЭС, исследовательских реакторов, гаммадефектоскопических лабораторий, люди, занятые на добыче и транспортировке, переработке ядерных материалов, пострадавшие в результате испытаний ядерного и термоядерного оружия, жители Восточного Казахстана, приполярных районов России, восточного Китая, а также менее значительные по численности группы пострадавших при небольших по масштабам радиационных авариях).
На основании этих исследований можно выделить следующие отдаленные последствия действия ионизирующей радиации:
1.Сокращение общей продолжительности жизни людей как результат наиболее интегральный, являющийся следствием ускоренного старения и повышенной смертности людей, в том числе и от других последствий облучения;
2.Радиационнно-индуцированные лейкозы, лимфомы, миеломная болезнь;
3.Солидные раки щитовидной железы, легких, желудка, костей, печени, рак молочной железы у женщин;
4.Катаракты хрусталика глаза;
5.Нефросклероз, пневмосклероз.
240 |
Радиобиология с основами радиоэкологии |
|
|
Одни из отдаленных биологических эффектов радиации носят стохастический, вероятностный характер, и с увеличением дозы радиации возрастает частота этих событий в клетках, а порог их возникновения, видимо, отсутствует. В основе стохастических эффектов лежит возникновение необратимых, стойких, совместимых с жизнью элементарных повреждений генетического аппарата клеток – мутаций, отражающихся на жизнедеятельности и функции клеток. Если такие повреждения возникают в ядерном аппарате соматических клеток, то образующиеся мутации в итоге длинной последовательности событий приводят к развитию злокачественных новообразований. Соматические мутации клеток медленно обновляющихся тканей (головного и спинного мозга, печени, миокарда, скелетных мышц и т.п.), накапливаясь со временем, ограничивают функциональную активность органов и систем и способствуют более быстрому старению организма. Можно полагать, что стохастические эффекты облучения организма способствуют развитию процессов сокращения продолжительности жизни организма, непосредственно пострадавшего в результате облучения, и формированию тератогенных эффектов, обусловленных воздействием радиации, проявляющихся у потомков первого поколения. Наконец, стохастические эффекты радиационного повреждения генома половых клеток приводят к возникновению генетических последствий облучения, проявляющихся на протяжении нескольких поколений потомков непосредственно облученных лиц.
8.5.2. Генетические и биохимические последствия при облучении в малых дозах
К числу стохастических отдаленных эффектов радиационного воздействия относят генетические эффекты. Изучение генетических последствий облучения связано с еще большими трудностями, чем в случае рака. Во-первых, не все известно о том, какие повреждения возникают в генетическом аппарате человека при облучении; во-вторых, полное выявление всех наследственных дефектов происходит лишь на протяжении многих поколений; в-третьих, как и в случае рака, эти дефекты невозможно отличить от тех, которые возникли совсем по другим причинам.
Около 10% всех живых новорожденных имеют те или иные генетические дефекты (рис. 8.7), начиная от необременительных физических недостатков типа дальтонизма и кончая тяжелыми состояниями, как синдром Дауна, хорея Гентингтона и другие пороки развития.
Генетические нарушения можно отнести к двум основным типам: хромосомные аберрации, включающие изменения числа или структуры хромосом, и мутации в самих генах. Генные
