
Радиобиология с основами радиоэкологии
.pdf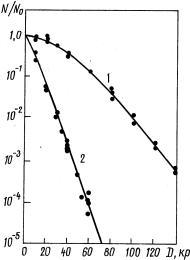
6. Радиационно-химические и радиационно-биохимические процессы... |
181 |
|
|
видно, снижение в воздухе кон- |
|
Таблица 6.1 |
||
центрации кислорода до 5% при- |
Влияние гипоксии на выживае- |
|||
водит к уменьшению количества |
мость облученных крыс |
|||
|
|
|
||
погибших животных при облуче- |
Доза |
Количество выжив- |
||
нии их высокими дозами рентге- |
ших животных , % |
|||
новского излучения. Проявление |
облучения, |
|
|
|
Воздух |
Гипоксия |
|||
кислородного эффекта обнаруже- |
Гр |
(20% О2) |
(5% О2) |
|
но как в модельных системах с |
|
|
|
|
6 |
63 |
100 |
||
макромолекулами, так и в экс- |
8 |
0 |
100 |
|
периментах с клеточными куль- |
||||
10 |
0 |
91 |
||
турами, изолированными тканя- |
||||
12 |
0 |
81 |
||
ми, организмами, популяциями. |
||||
14 |
0 |
29 |
||
С тех пор кислородный эффект |
||||
|
|
|
||
был выявлен многими исследо- |
|
|
|
|
вателями на самых различных объектах, и в настоящее время кислород по праву считается общим из естественных агентов, модифицирующих поражение в сторону его усиления. Это явление универсально и отмечается при воздействии редкоионизирующих излучений почти на все виды живой материи и многие макромолекулы биологического происхождения. На молекулярном уровне исследований при действии ионизирующих излучений обнаружено влияние кислорода в реакциях лучевой инактивации ферментов, вирусов и фагов, деполимеризации нуклеиновых кислот, повреждения углеводов и многих других реакциях. На клеточном уровне при вмешательстве кислорода растет частота индуцируемых генетических повреждений, увеличивается гибель клеток микроорганизмов и различных тканей животных (рис. 6.8).
Представление о возникновении потенциальных скрытых повреждений сформировалось в радиобиологии к концу 1950-х гг. под влиянием работ П. Александера, А. Чарлсби, У. Горди, Т. Альпер, Л.Х. Эйдуса. Согласно этим взглядам, в макромолекулах при их ионизации возникают скрытые повреждения, которые в отсутствие кислорода са-
Рис. 6.8. Кислородный эффект при рентгеновском облучении кишечной палочки (Е.Н. Андерсон, 1951; цит. по Л.Х. Эйдусу, 1972):
1 – облучение в азоте; 2 – облучение в кислороде.
182 |
Радиобиология с основами радиоэкологии |
|
|
ми по себе еще не ведут к потере активности, однако, будучи фиксированы кислородом, переходят в явные повреждения. Как видно, кислород является эффективным радиомодификатором, он обладает радиосенсибилизирующим эффектом.
Количественным выражением повышения радиочувствительности в присутствии кислорода является коэффициент кислородного усиления (ККУ). Значение этого коэффициента показывает, во сколько раз происходит увеличение радиочувствительности (снижение радиоустойчивости) живых обьектов в кислородной среде по сравнению с облучением их в бескислородных условиях. Например, при облучении в анаэробных условиях суспензии бактерий значение LD50 = 1000 Гр. При облучении этого вида бактерий в среде с содержанием кислорода LD50 для них составила всего 500 Гр. Коэффициент кислородного усиления в этом случае будет равен двум.
Экспериментально показано, что участие кислорода в реализации возникающих потенциальных повреждений происходит во время облучения. Так, введение кислорода в суспензию бактерий, культивируемых в условиях аноксии за 20 мс до облучения, усиливает их поражение. Добавление кислорода через 10 мс после облучения не изменяет поражающее действие ионизирующего излучения. Таким образом, сенсибилизирующее действие кислорода при облучении клеток проявляется только тогда, когда он присутствует в тканях в момент облучения.
Внастоящее время нет четких представлений о механизме сенсибилизирующего действия кислорода при облучении. Наиболее общепринятой считается точка зрения о том, что молекулы кислорода, обладая электронноакцепторными свойствами, активно взаимодействуют с образующимися свободными радикалами, в том числе и с радикалами биологических молекул. Вследствие этого происходит появление новых активных свободных радикалов и фиксация возникших в результате облучения потенциальных повреждений молекул. Фиксация повреждений заключается в стабилизации поврежденной структуры молекулы, что делает их недоступными или труднодоступными для системы репарации. Время жизни таких кислородозависимых повреждений может быть длительным. Например, в макромолекулах такие повреждения сохраняются в течение нескольких часов.
Если в растворе присутствуют молекулы-примеси, способные конкурировать с макромолекулами за активные продукты радиолиза воды, например, антиоксиданты, то это приводит к снижению радиационного поражения макромолекул. Справедливость такого положения также доказана экспериментально (рис. 6.9).
Вживых системах учет только содержания кислорода оказывается недостаточным. В этих случаях кислородный эффект,

6. Радиационно-химические и радиационно-биохимические процессы... |
183 |
Рис. 6.9. Поражение сывороточ ного альбумина человека после облучения g-лучами:
А– 1%-ный раствор; Б – то же
вприсутствии b-меркап тоэтиламина
2×10–3 М; В – то же в присутствии ти - омочевины 1×10–3 М (С. Розен и др., 1957).
определяемый, например, по инактивации ДНК или фагов в растворе, или по гибели клеток, проявляется только в присутствии SH-соединений. Последние конкурируют с кислородом за потенциальные повреждения, возникающие в ДНК, определяя их судьбу: при фиксации кислородом они реализуются в явные повреждения – инактивацию, а при взаимодействии с SН-группой исчезают, и молекула возвращается в исходное состояние, т.е. наблюдается так называемый обратный кисло родный эффект. Впервые это явление наблюдала Т. Альпер в 1952–1954 гг., обнаружив защитную роль кислорода при инактивации бактериофага SН. Критерием радиочувствительности в этих опытах послужило появление свободных SН-групп. Аналогичные результаты были получены и на других фагах, а также в растворах химотрипсина, трипсина, пепсина, растворах различных ферментов. Т. Альпер и другие авторы объясняли обратный кислородный эффект тем, что в отличие от большинства других биологических объектов бактериофаг поражается не окислительными (ОН., НО2.), а восстановительными (Н.) радикалами.
В присутствии SH-соединений лучевое поражение макромолекул снижается в результате двух эффектов – защитное соединение конкурирует за свободные радикалы воды и способно репарировать путем переноса водорода SH-группы на радикал макромолекулы. На рис. 6.10 показано, что в анаэробных условиях глутатион в 3.7 раза уменьшает радиочувствительность ДНК
Рис. 6.10. Инактивация трансфор-
мирующей ДНК из Diplococcus pheumonial:
1 – облучение в атмосфере азота ( ) и 2 – кислороде (
) и 2 – кислороде ( ) в присутствии глутатиона 1.4×10–3 М; 3 – облучение в водном растворе в отсутствии радиозащитного агента (Ю.Б. Кудряшов, Б.С. Беренфельд, 1979).
) в присутствии глутатиона 1.4×10–3 М; 3 – облучение в водном растворе в отсутствии радиозащитного агента (Ю.Б. Кудряшов, Б.С. Беренфельд, 1979).
184 |
Радиобиология с основами радиоэкологии |
|
|
(кривая I), вероятно, в результате обоих эффектов. В атмосфере кислорода защитный эффект глутатиона снижается, но все же радиочувствительность ДНК ниже, чем в водном растворе без радиозащитного соединения, даже если облучение проводили в аноксических условиях. Очевидно, кислород конкурирует с восстановительной способностью глутатиона, переводя радикалы ДНК в трудно репарируемую перекисную форму, хотя и в этих условиях эффект глутатиона, как перехватчика радикалов, сохраняется (кривая 2 лежит выше кривой 3).
Итак, модифицирующее действие кислорода на макромолекулы, облученные в водном растворе, определяется многими факторами: присутствием защитного соединения, его родством к кислороду, типом радикала воды, вызывающего данное повреждение макромолекулы, вкладом прямого и непрямого действия в эффект поражения. Во всех случаях кислород не вызывает истинной сенсибилизации или защиты макромолекул,
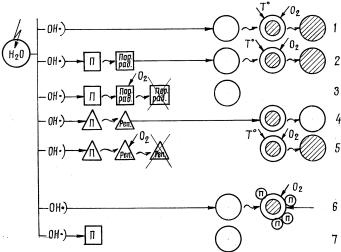
Рис. 6.11. Общая схема физико-химического этапа поражения, защиты
ирепарации макромолекул (Л.Х. Эйдус, 1972):
П– примеси разных видов; Пор. Рад. и Реп. Рад – продукты радиолиза примесей, способные поражать макромолекулы или репарировать в них скрытые повреждения; большие кружки, заштрихованные частично или полностью, – макромолекулы со скрытыми повреждениями или уже инактивированные; перечеркнутые косым крестом – радикалы примесей, дезактивированные кислородом. 1, 2 – поражение с образованием скрытого повреждения кислородного или теплового типа, 3 – защитное действие кислорода путем дезактивации поражающих радикалов примеси, 4 – репарация макромолекулы со скрытым повреждением, 5 – усиление повреждения путем дезактивации кислородом репарирующих радикалов примеси, 6 – защита от реализации скрытых повреждений адсорбционным механизмом, 7 – защита путем перехвата водных радикалов с образованием неактивных продуктов радиолиза примеси.

6. Радиационно-химические и радиационно-биохимические процессы... |
185 |
так как он не влияет на число первичных повреждений. Повидимому, действие кислорода связано с процессами репарации начальных повреждений макромолекул в присутствии защитных веществ. Поэтому кислородный эффект может не наблюдаться в разбавленных водных растворах, не содержащих радиопротектора.
Таким образом, кислород при лучевом поражении биологических объектов выполняет две разные функции. С одной стороны, усиливает первичное поражение, с другой, – облегчает пострадиационное восстановление. Выше приведена общая схема физико-химического этапа поражения, защиты и репарации макромолекул (рис. 6.11). Реальность всех этих физи- ко-химических процессов доказана экспериментально, однако в конкретных условиях, существующих внутри живой клетки, вклад каждого из них может быть различным, а для его установления требуется глубокий анализ, основанный на понимании физической природы рассматриваемых явлений.
6.6. Химические реакции основных молекулярных компонентов клетки
на действие ионизирующего излучения
При описании действия ионизирующей радиации на молекулярные компоненты живой клетки удобно воспользоваться упрощенным представлением о ее строении и химическом составе. Основную массу клетки составляет вода, в которой в растворенном или взвешенном состоянии находятся неорганические ионы, малые органические молекулы, макромолекулы и надмолекулярные структуры различной степени сложности.
Макромолекулы относятся преимущественно к трем типам: полисахариды, белки и нуклеиновые кислоты. Клеточные органеллы построены из двух видов надмолекулярных структур:
–белково-липидных мембран, из которых состоят оболочка клетки и ядра, цитоплазматическая сеть, лизосомы и митохондрии;
–нуклеопротеидов (соединений нуклеиновых кислот с белком), из которых состоят хромосомы и рибосомы.
Входящие в состав клетки тысячи различных химических веществ можно свести к комбинации нескольких достаточно простых видов низкомолекулярных соединений. Это пять видов органических соединений – углеводы, аминокислоты, карбоновые кислоты, азотистые основания и сложные гетероциклические соединения, а также неорганический ион – остаток фосфорной кислоты. Эти комбинации, постепенно усложняясь, образуют высшие ступени организации клетки – макромолекулы и надмолекулярные структуры.
186 |
Радиобиология с основами радиоэкологии |
|
|
Исследованием химических превращений, происходящих при воздействии ионизирующих излучений в химических системах, занимается специальная дисциплина – радиационная биохимия. Реакции и превращения под влиянием ионизирующей радиации таких соединений, как ДНК, РНК, белков, аминокислот, углеводов и липидов играют наиболее важную роль в структуре и функциях живых организмов.
6.6.1. Действие облучения на ДНК и РНК
Среди нуклеиновых кислот наиболее вероятной внутриклеточной мишенью является ДНК – самая большая по размеру
инаиболее биологически значимая молекула. Мономерные составляющие нуклеиновых кислот – нуклеотиды – включают три компонента: азотистое основание (пурин или пиримидин), пентозу (рибозу или дезоксирибозу) и фосфат-ион. При радиолизе нуклеиновых кислот обнаружены основные изменения, происходящие в ДНК при действии ионизирующей радиации, такие как разрыв одной из спиралей, разрыв обеих спиралей, образование «сшивок» оснований и «сшивок» ДНК–белок, разрушение оснований, денатурация, образование перекисей тимидина и цитозина, дезаминирование, освобождение оснований
инекоторые другие, которые приводят к изменению ее физи- ко-химических свойств и, соответственно, нарушению биологи-
Действие ионизирующего излучения на клетку
Видимые радиационные эффекты: задержка роста и развития организма
|
Нарушение синтеза ДНК |
|
|
|
|
|
Возможные причины |
|
Нарушение ионного равно- |
Подавление митозов |
|
весия («натриевый насос») |
|
|
Повреждение биомембран и |
Нарушение процесса окис- |
|
ультраструктур («лучевой |
лительного фосфорилирова- |
|
нож») |
ния |
|
Угнетение синтеза фермен- |
Подавление облучением |
|
тов фосфорилирования |
критических ферментов |
|
предшественников |
синтеза ДНК |
|
Нарушение процесса транс- |
Поражение матрицы ДНК |
|
дукции |
и ДНП |
|
Воздействие радиотоксинов |
Нарушение регуляции |
|
|
синтеза РНК |
|
Рис. 6.12. Возможные причины нарушения синтеза ДНК под влиянием облучения.

6. Радиационно-химические и радиационно-биохимические процессы... |
187 |
ческих функций. Кроме того, происходят одиночные и двойные разрывы тяжей ДНК, разрывы водородных связей между комплементарными основаниями в двойной спирали, ковалентные сшивки. Двойные разрывы тяжей ДНК являются критической реакцией для репродуктивной гибели клеток. На рис. 6.12 представлена схема процессов, которые могут быть ответственными за радиационное поражение функции самовоспроизведения ДНК.
Не прибегая к детальному анализу химической структуры повреждений ДНК (это в большинстве случаев очень сложно, некоторые из повреждений трудно точно охарактеризовать), различают два основных типа – сублетальные и потенциаль но летальные повреждения (табл. 6.2). Сублетальные – это та кие вызванные радиацией изменения, которые сами по себе не ведут к гибели клетки, но облегчают ее при продолжающем ся или последующем облучении. Например, одиночные разрывы обычно не смертельны, но чем больше их возникает в молекуле ДНК, тем выше вероятность их совпадения и образования летального двойного разрыва. Если дозу радиации разделить на две фракции и изменять величину интервала между ними, то с увеличением дозы выживаемость возрастет за счет репарации в период между фракциями части сублетальных повреждений. Эти данные впервые были изучены и описаны М. Элкиндом.
Второй тип – потенциально летальные повреждения – са ми по себе вызывают гибель клетки, но в определенных усло виях могут быть устранены репаративной системой. Пример таких повреждений – двунитевые разрывы молекулы ДНК.
РНК, представленную в клетке рядом форм – матричной, рибосомальной, транспортной – относят к массовым структурам клетки: они повторяются, содержась во многих копиях, и в случае необходимости могут синтезироваться в требуемом количестве. Поэтому радиационное повреждение РНК не столь ответственно за лучевое поражение клетки, как повреждение молекул ДНК. В ранних работах по влиянию радиации на нуклеиновые кислоты утвердилось мнение, что синтез РНК – это радиоустойчивый процесс. Однако в настоящее время доказано, что одним из основных эффектов радиобиологического действия на клетку является неспецифическое нарушение регуляции самых ранних этапов транскрипции РНК. Многочисленные данные свидетельствуют о нарушении под влиянием облучения регуляции синтезирующих видов РНК, остановки синтеза РНК вдоль цепи ДНК. Вполне возможно, что первой причиной нарушения регуляции транскрипции в облученных клетках является радиационная дестабилизация ДНК, вызывающая конформационные перестройки нуклеопротеида вследствие неспеци фической радиационной активности генома. В основном типы радиационных повреждений РНК сходны с таковыми для ДНК.
188 |
Радиобиология с основами радиоэкологии |
|
|
6.6.2. Радиационно-химические изменения белков, аминокислот, углеводов, липидов
Радиочувствительность белков во многом определяется радиочувствительностью входящих в их состав аминокислот. Белки состоят из аминокислот, соединенных пептидной связью между азотом a-аминогруппы – одной и углеродом карбоксильной группы – другой и образующих полипептидную цепочку – первичную структуру: белки делятся на фибриллярные (нитеподобные) и глобулярные. Глобулярными белками являются ферменты, которые играют важную роль в регуляции обмена веществ в клетке и организме. Ряд радиочувствительности аминокислот по мере ее снижения выглядит так: серосодержащие (цистеин, метионин); некоторые циклические (тирозин, триптофан, гистидин); имеющие в остатке азотсодержащие группы (аргинин, аспарагин, глутамин); аминокислоты, не содержащие в остатке присоединенных групп, или содержащие –ОН (фенилаланин, пролин, валин, лейцин, изолейцин, глицин, серин, треонин). Данные по радиочувствительности аминокислот нельзя безоговорочно переносить на белки – их поражаемость зависит от расположения остатков аминокислот, структуры белковой молекулы.
Под воздействием ионизирующей радиации белки, как и многие другие высокополимерные вещества, претерпевают такие нарушения:
1.Конфигурационные видоизменения молекулы, не связанные с изменением молекулярной массы, но отражающиеся на физико-химических и биологических свойствах белка;
2.Образование сшивок между молекулами, агрегация молекул, увеличение молекулярной массы;
3.Деструкция макромолекулы с разрывом пептидных или углеродных связей, уменьшение молекулярной массы;
4.Химические превращения активных групп на поверхности и в глубине белковой молекулы (глобулы), в первую очередь окислительного или восстановительного характера.
Одни из этих изменений (например, химические превращения активных групп) часто бывают тесно связаны с другими (например, с конфигурационными перестройками или образованием сшивок), и все происходящие изменения объединяют под общим названием денатурация белка.
Механизм действия радиации на белковые молекулы в вод ном растворе можно объяснить на примере фермента лизоци-
ма, который облучали в присутствии различных перехватчиков или селективно воздействовали на него радикалами Н. и ОН.. Было показано, что инактивация фермента происходит
врезультате атаки белковой молекулы тремя типами радикалов – Н., ОН. и е–гидр. В результате первичного размена энергии
вмолекуле белка возникают свободнорадикальные формы, ко-

6. Радиационно-химические и радиационно-биохимические процессы... |
189 |
торые принимают участие в дальнейших реакциях. Через промежуточные соединения, образующиеся по центрам локализации свободнорадикальных состояний, белки расщепляются и образуют фрагменты белковых молекул. Вместе с тем, свободные радикалы могут инициировать процессы полимеризации в разных участках белковой молекулы, образовывать амиды и карбонильные соединения; нарушения водородных связей могут сопровождаться денатурацией белков. Неодинаковость радиационного повреждения различных аминокислотных остатков в молекуле белка является причиной нарушения вторичной и третичной структур белка. Кроме того, может нарушаться функционирование активных центров ферментов или же центров аллостерического взаимодействия.
Физико-химический анализ облученной рибонуклеазы в растворе обнаружил следующие структурные повреждения: возникновение агрегатов макромолекул, выявляемых по повышению внутренней вязкости и появлению дополнительных фракций при гельфильтрации, появление свободных SH-групп; селективное разрушение аминокислот метионина, цистина, лизина, тирозина, фенилаланина, гистидина; изменение конформации, определяемое по увеличению перевариваемости молекул трипсином. Все эти структурные изменения выявлены при дозе, близкой к Д37, когда каждая молекула испытала в среднем по одному инактивирующему событию попадания.
В табл. 6.2 представлены выводы некоторых исследователей, изучавших механизм инактивации ферментов ионизирую-
щим излучением в воде.
Таблица 6.2
Предполагаемые причины инактивации ферментов, облученных в водном растворе (С. Окада, 1974)
Исследованный |
Предполагаемая причина |
фермент |
инактивации облученного фермента |
Рибонуклеаза |
Разрушение остатка метионина |
Дезоксирибонуклеаза I |
Разрушение одной молекулы триптофана |
Фосфоглюкомутаза |
Разрушение одной молекулы гистидина |
Каталаза |
Разрушение гематопорфириновой группы |
Лактопероксидаза |
Частичное разрушение одной гематопорфирино- |
|
вой группы |
Фосфоглицеральдегид- |
Деструкция SH-групп (цистеина) или окисление |
дегидрогеназа |
SH-групп |
Аденозинтрифосфатаза |
Окисление SH-групп |
Сукцинатоксидаза |
Окисление SH-групп |
Уреаза |
Окисление SH-групп |
Глутаматдегидрогеназа |
Окисление SH-групп |
Лактатдегидрогеназа |
Окисление SH-групп |
Алкогольдегидрогеназа |
Окисление или деструкция SH-групп |
190 |
Радиобиология с основами радиоэкологии |
|
|
С утратой свойственных неповрежденным белкам конформационных состояний связано ослабление способности белка к молекулярному узнаванию, определяющему самосборку надмолекулярных структур, таких как мультиэнзимные комплексы, хроматин, цитоскелет, электронно-транспортная цепь митохондрий (хлоропластов).
Учитывая множественность молекул отдельных белков, возможность их синтеза de novo в случае дефицита, при умеренных облучениях прямое повреждение белковых молекул не имеет решающего значения для жизнеспособности клеток.
Карбоновые кислоты, в молекуле которых имеется одна или несколько групп NH2, называются аминокислотами. Под влиянием облучения растворов аминокислот можно наблюдать следующие реакции: процессы окислительного дезаминирования с выделением аммиака; окислительное декарбоксилирование с образованием в соответствующие альдегиды; возникновение продуктов конденсации и другие реакции. Радикалы, возникающие в результате отщепления Н (от a-углеродного атома или в остатке Rа), образуются и при радиолизе водных растворов аминокислот в реакциях с Н и ОН.
В безводных и анаэробных условиях основную роль играют реакции радикалов: RaCHCOO–, NH2 CH2RaNH2, в результате которых образуются карбоновые кислоты (амин и аммиак). В присутствии кислорода существенный вклад в радиолиз дают процессы образования перекисного радикала.
Углеводами, или сахаридами называются вещества с общей формулой (CH2O)n. При облучении моносахаридов (водные растворы) образуются как окисленные, так и восстановленные продукты, содержащие либо такое же число атомов углерода, что и исходная молекула, либо являющиеся низкоуглеродными фрагментами, а также высокомолекулярные продукты полимеризации.
Исследования радиолиза дисахаридов показали, что в них происходят радиационно-химические превращения, характерные для моносахаридов и, кроме того, наблюдаются иные процессы, связанные с наличием О-гликозидной связи.
При облучении полисахаридов и в сухом виде, и в растворах наблюдаются сложные изменения, обнаруживаются нарушения структуры отдельных мономерных единиц, разрывы гликозидных связей. Облучение γ-лучами, быстрыми электронами, нейтронами высокомолекулярных углеводов приводит к изменению их физико-химических свойств (вязкости, механической упругости, набухания, растворимости и скорости гидролиза). Опыты с целлюлозой, крахмалом, декстраном, пектином и другими микромолекулами, состоящими из гексоз, связанных эфирными связями, показали, что изменения в них под влиянием облучения вызваны радиационной деполимеризаци-
