
- •Статистична обробка даних аналізу об'єктів навколишнього середовища
- •Теоретичні відомості
- •Значень довірчої вірогідності р
- •Завдання для самостійної роботи
- •Запитання до самоперевірки:
- •Способи вираження концентрацій розчинів і алгоритм розрахунків при приготуванні розчинів заданої концентрації
- •Теоретичні відомості
- •100 Г розчину містить 20 г nh4Cl,
- •80Г розчину містить х г nh4Cl
- •159,6 Г CuSo4 міститься в 249,6 г CuSo4∙5h2o,
- •100Г CuSo4 міститься в х г CuSo4∙5h2o,
- •Завдання для самостійної роботи
- •Запитання до самоперевірки:
- •Методи хімічного аналізу
- •Хід роботи
- •Запитання до самоперевірки:
- •Фотометричне визначення концентрації речовини
- •Реактиви та обладнання:
- •Теоретичні відомості
- •Хід роботи
- •Запитання до самоперевірки:
- •Визначення іонів карбонату та бікарбонату у водній витяжці ґрунту
- •Обладнання та реактиви:
- •Теоретичні відомості
- •Хід роботи
- •Запитання до самоперевірки:
- •Визначення діоксиду карбону карбонатів
- •Обладнання та реактиви:
- •Теоретичні відомості
- •Хід роботи:
- •Теоретичні відомості
- •Хід роботи
- •Запитання до самоперевірки:
- •Визначення обмінної кислотності ґрунту
- •Обладнання та реактиви
- •Теоретичні відомості
- •Хід роботи
- •Запитання до самоперевірки
- •Визначення гідролітичної кислотності за методом Каппена в модифікації цінао
- •Обладнання та реактиви:
- •Хід роботи
- •Запитання до самоперевірки:
- •Визначення і оцінка кислотно-основної буферності ґрунту
- •Реактиви та обладнання
- •Теоретичні відомості
- •За діапазонами значень рН
- •Хід роботи
- •Запитання до самоперевірки:
- •Визначення суми поглинутих основ за методом Каппена та ступеню насичення ґрунту основами
- •Обладнання та реактиви:
- •Теоретичні відомості
- •Хід роботи
- •Запитання до самоперевірки:
- •Визначення хлоридів у ґрунті
- •Обладнання та реактиви:
- •Теоретичні відомості
- •Хід роботи
- •Контрольні питання
- •Визначення вмісту Cu, Zn, Cr, Fe у воді методом атомно-абсорбційної спектрофотометрії
- •Обладнання та реактиви:
- •Хід роботи
- •Запитання до самоперевірки
- •Фотометричне визначення Феруму з сульфосаліциловою кислотою
- •Обладнання та реактиви:
- •Загальні відомості:
- •Хід визначення
- •Запитання до самоперевірки:
- •Визначення вмісту нітратів у сільськогосподарській продукції
- •Обладнання та реактиви:
- •Теоретичні відомості
- •Суть методу
- •Хід роботи
- •Запитання до самоперевірки:
Запитання до самоперевірки:
Пояснити на чому ґрунтується титриметричний аналіз.
Дайте характеристику методів титриметричного аналізу.
На чому заснований титриметричний метод визначення іонів карбонату та бікарбонату?
Напишіть рівняння реакцій, що відбуваються при титруванні карбонат- і бікарбонат-іона сульфатною кислотою.
Як розраховуються кількості еквівалентів карбонат- і бікарбонат-іона?
Як розраховуються масові частки карбонат- і бікарбонат-іона в ґрунті?
Лабораторна робота № 6
Визначення діоксиду карбону карбонатів
Мета роботи: навчитися визначати діоксид Карбону карбонатів грунту титрометричним методом.
Обладнання та реактиви:
Бюкс скляний з притертою пробкою;
Ексикатор лабораторний;
Змішувач магнітний;
Бюретка місткістю 25см3 2-го класу точності за ГОСТ 20292-74;
Терези лабораторні загального призначення типу ВЛР-200г;
Посуд мірний лабораторний за ГОСТ 1770-74;
Папір фільтрувальний «синя стрічка» за ГОСТ 12026-76;
Натрій гідроксид, стандарт-тітр (0,1н.);
Хлоридна кислота, стандарт-титр (0,1н.);
Вода дистильована за ГОСТ 6709-72;
Метиловий червоний, індикатор за ГОСТ 10816-64, розчин з масовою часткою 0,02%;
Лакмусовий папір.
Теоретичні відомості
Карбонати в ґрунтах та донних відкладах визначають гравіметричним або титриметричним методом. Гравіметричний метод полягає у зважуванні маси СО2, який виділяється при розкладанні карбонатів хлоридною кислотою:
СаСО3![]() +2НСl
= СО2
+2НСl
= СО2![]() +
СаСl2
+ Н2О
+
СаСl2
+ Н2О
Карбон (IV) оксид хемосорбують у попередньо зважених поглинальних трубках, які містять розчин КОН. За збільшенням маси поглинальних трубок знаходять вміст СО2 карбонатів.
Більш зручним і придатним для масових аналізів є титриметричний метод, який полягає в обробці твердої проби надлишком розчину хлоридної кислоти з наступним титруванням її залишку розчином лугу.
При
вмісті СО2
карбонатів
![]() 15%
проби обробляють 0,02 моль/дм3
розчином НСl,
при вмісті в межах 16-18% – 0,1 моль/дм3
розчином кислоти, а при вмісті понад
18-20% – 0,2 моль/дм3
хлоридною
кислотою.
15%
проби обробляють 0,02 моль/дм3
розчином НСl,
при вмісті в межах 16-18% – 0,1 моль/дм3
розчином кислоти, а при вмісті понад
18-20% – 0,2 моль/дм3
хлоридною
кислотою.
Хід роботи:
Визначення гігроскопічної води. У висушеному бюксі з притертою кришкою зважують 1-2 г проби повітряно-сухого грунту, поміщають відкритий бюкс в сушильну шафу і висушують пробу при 100-105оС протягом 5 годин до постійної ваги. Бюкс виймають з сушильної шафи, закривають кришкою і поміщають в ексикатор на 20-30 хв. Вміст гігроскопічної води в процентах відносно маси сухої проби розраховують за формулою:
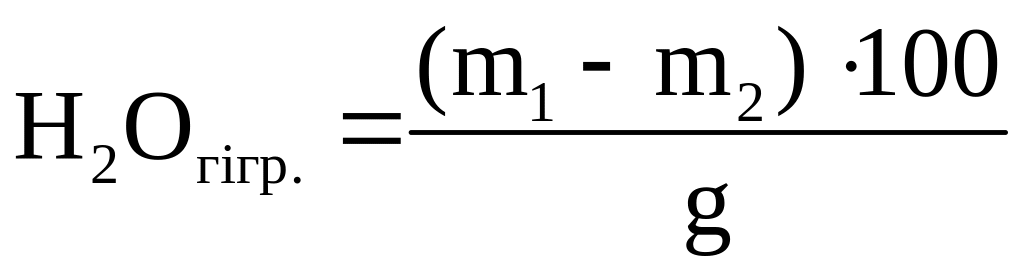
де m1 – маса бюкса з наважкою грунту до висушування, г; m2 – маса бюкса з наважкою грунту після висушування, г; g – маса проби грунту після висушування, г.
Визначення діоксиду Карбону карбонатів. 2-5 г проби повітряно-сухого грунту або сухих донних відкладів вносять у колбу на 1000 см3, додають 500 см3 хлоридної кислоти і залишають протягом доби, періодично збовтуючи. Перевіряють кислотність розчину лакмусовим папірцем і, якщо розчин не є кислим, ще додають хлоридну кислоту і знову витримують. Із відфільтрованої витяжки відбирають 25 см3 розчину, додають 2-3 краплини 0,02% розчину індикатора метилового червоного і титрують розчином NaОН такої ж концентрації, як і хлоридна кислота, що була використана для розкладання карбонатів.
Одночасно проводять холостий дослід без проби ґрунту.
Вміст СО2 карбонатів (%) обчислюють за формулою

де v – об'єм розчину кислоти, взятої для розкладання проби, см3; v1– об'єм аліквоти, взятої для титрування, см3; С1, – концентрація кислоти, моль/дм3; v2 – об'єм лугу, витраченого на титрування аліквоти, см3; С2 – його концентрація, моль/ дм3; g – маса наважки повітряно-сухого грунту, г; М – молярна маса еквівалента СО2, М(1/2СО2) = 22; К – коефіцієнт перерахунку на суху пробу.
При аналізі повітряно-сухого грунту К=100/(100-%Н2Огігр.). При аналізі сухої проби донних відкладів К=1, а g – масі наважки проби.
Запитання до самоперевірки:
Як можна визначити карбонати в ґрунтах та донних відкладах?
На чому заснований титриметричний метод визначення карбонатів грунту?
Дайте характеристику методів титриметричного аналізу.
Який з методів титриметричного аналізу був використаний в роботі?
Як визначається точка еквівалентності?
Як проводиться підготовка проби ґрунту до аналізу?
Лабораторна робота № 7
визначення вмісту Cu, Zn, Cr, Fe у ґрунті методом
атомно-абсорбційної спектрофотометрії
Мета роботи: практично ознайомитись з методом атомно-абсорбційної спектрофотометрії, будовою та принципом роботи атомно-абсорбційного спектрофотометра типу С-115М1 та визначити вміст Na, K, Fe у ґрунті.
Обладнання та реактиви
Спектрофотометр атомно-абсорбційний С-115М1, ТО 2.851.034-04;
Лампа з порожнистим катодом ЛТ-2, ТУ 88-2698934-005-94;
Пропан-бутан побутовий в балоні, ГОСТ15860-84;
Терези лабораторні загального призначення типу ВЛР-200г;
Піпетки 1-го класу точності, ГОСТ 20292-74;
Фільтр знезолений, біла стрічка, діаметром 15 см або папір фільтруючий лабораторний марки ФОС, ГОСТ 12026-76;
Циліндри мірні, ГОСТ 1770-74;
Лійка скляна, ГОСТ 25336-82;
Колби мірні 2-го класу точності, ГОСТ 1770-74;
Колби конусні, ГОСТ 25336-82;
Стакан хімічний, ГОСТ 25336-82;
Вода дистильована, ГОСТ 6709-72;
Кислота сульфатна, ГОСТ 4204-77, ч.д.а.;
Сіль Мора, FeSO4×(NH4)2SO4×6H2O, ГОСТ 4208-72, х.ч.;
Натрій хлорид, ГОСТ 4233-77, х.ч.;
Калій хлорид, ГОСТ 4234-77, х.ч.
